Содержание
- 2. Алюминий – это пластичный и лёгкий металл белого цвета, покрытый серебристой матовой оксидной плёнкой. В периодической
- 3. Строение -Относительная атомная масса алюминия – 27. Электронная конфигурация атома алюминия – 1s22s22p63s23p1, модель распределения электронов
- 4. Химические свойства алюминия 1. Алюминий легко реагирует с простыми веществами-неметаллами: 4Al + 3O2 = 2Al2O3 2Al
- 5. 2. Алюминий реагирует с водой (после удаления защитной оксидной пленки): 2Al + 6H2O = 2Al(OH)3 +
- 6. 4. Алюминий вступает в реакцию со щелочами 2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2
- 7. 5. Алюминий легко растворяется в соляной и разбавленной серной кислотах: 2Al + 6HCl = 2AlCl3 +
- 8. Физические свойства
- 9. Получение 1)Исторический способ: В 1927 году немецкий химик Ф. Велер получил алюминий при нагревании хлорида алюминия
- 10. Нахождение в природе Алюминий занимает третье место по распространенности (8%),после кислорода и кремния. В следствие высокой
- 11. Применение Алюминий применяется в металлургии в качестве основы для сплавов (дуралюмин, силумин) и легирующего элемента (сплавы
- 13. Скачать презентацию










 Броматометрия. (Лекция 10)
Броматометрия. (Лекция 10) Обмен белков. (Лекция 16)
Обмен белков. (Лекция 16) Дидактические игры, умело применяемые педагогами на уроках, позволяют развивать творческие способности учащихся, пробуждают п
Дидактические игры, умело применяемые педагогами на уроках, позволяют развивать творческие способности учащихся, пробуждают п Аттестационная работа. Технология проектной деятельности на уроках химии в подростковой школе (6-9 классы) по системе РО
Аттестационная работа. Технология проектной деятельности на уроках химии в подростковой школе (6-9 классы) по системе РО Золото Aurum
Золото Aurum Производство топлива для реактивных двигателей марки ТС-1 с присадками
Производство топлива для реактивных двигателей марки ТС-1 с присадками Нанокомпозиционный материал на основе фенолоформальдегидной смолы, эпоксидной смолы, полистирола
Нанокомпозиционный материал на основе фенолоформальдегидной смолы, эпоксидной смолы, полистирола Свойства неметаллов и их соединений
Свойства неметаллов и их соединений Когда его называли гением, он морщился: "Какой там гений. Трудился всю жизнь, вот и стал гением". Когда в 26 лет писал курс "
Когда его называли гением, он морщился: "Какой там гений. Трудился всю жизнь, вот и стал гением". Когда в 26 лет писал курс " Гомологи бензола
Гомологи бензола Окислительный стресс
Окислительный стресс Ископаемое сырье органической химии
Ископаемое сырье органической химии Битумы природного происхождения
Битумы природного происхождения Презентация Неорганические и органические основания.
Презентация Неорганические и органические основания. Цикл трикарбоновых кислот (цикл Кребса)
Цикл трикарбоновых кислот (цикл Кребса) Азот
Азот  Неделя химии в МБОУ Андреевская ООШ
Неделя химии в МБОУ Андреевская ООШ Электрический ток в металлах
Электрический ток в металлах КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Обмен белко
КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Обмен белко Начала физической химии
Начала физической химии Презентация по Химии "Алотропія карбону" - скачать смотреть
Презентация по Химии "Алотропія карбону" - скачать смотреть 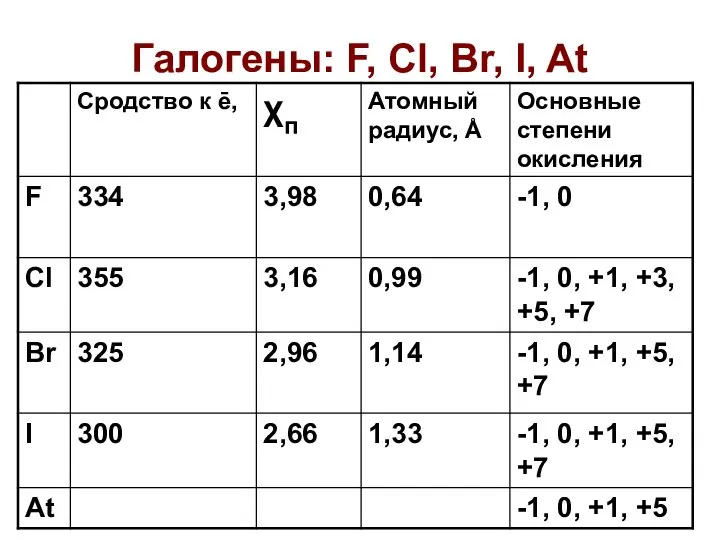 Галогены: F, Cl, Br, I, At
Галогены: F, Cl, Br, I, At Медь и ее сплавы
Медь и ее сплавы Электропроводность растворов электролитов. Числа переноса
Электропроводность растворов электролитов. Числа переноса Материаловедение
Материаловедение Термодинамика. 2 закон термодинамики. Энтропия
Термодинамика. 2 закон термодинамики. Энтропия Щелочные АКБ
Щелочные АКБ Литология. Кремнистые породы
Литология. Кремнистые породы