Содержание
- 2. Положение в Периодической системе. Al Номер элемента Период Группа Подгруппа
- 3. Нахождение в природе. Al Боксит Al2O3 • H2O (с примесями SiO2, Fe2O3, CaCO3) Нефелины KNa3[AlSiO4]4
- 4. Нахождение в природе. Al Глинозем Полевой шпат
- 5. Нахождение в природе. Al Корунд Берилл
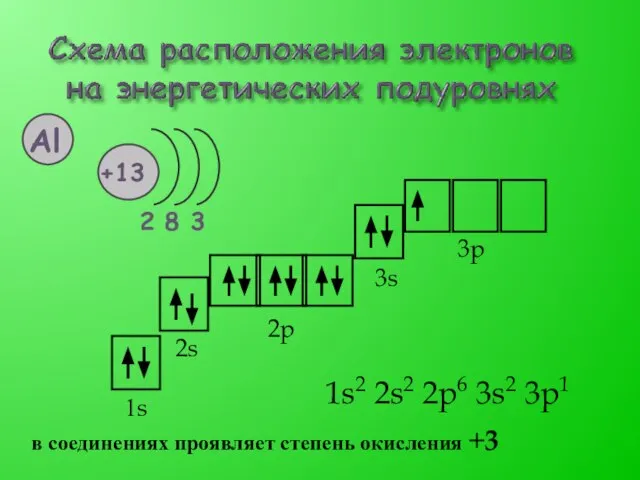
- 6. 1s2 2s2 2p6 3s2 3p1 1s 2s 2p 3s 3p в соединениях проявляет степень окисления +3
- 7. Al – серебристо-белый металл, пластичный, легкий, хорошо проводит тепло и электрический ток, обладает хорошей ковкостью, легко
- 8. Химические свойства. I) Взаимодействие с простыми веществами:
- 9. Химические свойства II) Взаимодействие со сложными веществами. Взаимодействие с водой: Al + H2O = Al(OH)3 +
- 10. Химические свойства II) Взаимодействие со сложными веществами. 3) Взаимодействие с кислотами: Al + H2SO4 = Al2(SO4)3
- 11. Соединения алюминия: Al2O3 – оксид алюминия Корунд - оксид алюминия - наиболее твердое вещество на Земле
- 12. Корунд Мелко кристаллические непрозрачные разновидности серовато-черного цвета называют наждаком и применяется в качестве абразивного материала.
- 13. Корунд Корунд удивительно многолик. В коллекции минералогического музея Санкт-Петербургского горного института хранятся корунды более 40 оттенков:
- 14. Корунд
- 15. Корунд
- 16. Корунд
- 17. Корунд Наиболее драгоценными корундами являются рубины и сапфиры. Их окраска, как и во всех прочих случаях,
- 18. Корунд Ti4+ , Fe2+ , Fe3+ придают синий цвет (сапфир)
- 19. Корунд Эти разновидности благородного корунда наряду с алмазами и изумрудом занимают высшее место в классификации драгоценных
- 20. Сапфир
- 21. Рубин
- 22. Соединения алюминия: Al2O3 – амфотерный оксид Оксид, который одновременно проявляет свойства и основного и кислотного оксидов.
- 24. Al2O3 – амфотерный оксид Основные свойства: Al2O3 + HCl − Кислотные свойства: Al2O3 + NaOH −
- 25. Соединения алюминия: Al(OH)3 – амфотерный гидроксид Гидроксид, который одновременно проявляет свойства и основания и кислоты.
- 26. Al(ОН)3 – амфотерный оксид Основные свойства: Al(ОН)3 + HCl − Кислотные свойства: Al(ОН)3 + NaOH −
- 27. Применение алюминия. Из общемирового объема производимого алюминия 20% идет на строительство. Редкое здание сегодня возводится без
- 28. Применение алюминия. Чтобы создать современное транспортное средство, будь то автомобиль, поезд, океанский лайнер или космический корабль,
- 29. Применение алюминия. Из легкого металла делают вагоны суперскоростных поездов и современные вагоны метро. Транспорт Судостроители настолько
- 30. Применение алюминия. Первая алюминиевая банка для напитков появилась не так давно — в 1972 году. Тара
- 31. Применение алюминия. С 1926 года для усиления действия вакцин используют алюминиевые соли. Фармацевтика На основе алюминия
- 32. Применение алюминия. Алюминий прекрасно проводит электричество. Электрика и машиностроение С 1940-х годов алюминий почти полностью заменил
- 34. Скачать презентацию

![Нахождение в природе. Al Боксит Al2O3 • H2O (с примесями SiO2, Fe2O3, CaCO3) Нефелины KNa3[AlSiO4]4](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/508331/slide-2.jpg)




























 Химические соединения растительного и животного мира - углеводы
Химические соединения растительного и животного мира - углеводы Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Классификация и номенклатура липидов. Жирные кислоты, их классификация и номенклатура
Классификация и номенклатура липидов. Жирные кислоты, их классификация и номенклатура Қазіргі кезде қолданылатын дезинсектицидтер
Қазіргі кезде қолданылатын дезинсектицидтер Ферросплавы. Феррохром
Ферросплавы. Феррохром Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю
Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю Аттестационная работа. Программа элективного курса химия и военное дело. (8-9 класс)
Аттестационная работа. Программа элективного курса химия и военное дело. (8-9 класс) Гидролиз
Гидролиз Презентация по Химии "Химические тайны запаха" - скачать смотреть
Презентация по Химии "Химические тайны запаха" - скачать смотреть  Пластмассы, их классификация и применение
Пластмассы, их классификация и применение Полимерные растворы – условия образования
Полимерные растворы – условия образования Аминокислоты и белки
Аминокислоты и белки Полимеры и биополимеры.
Полимеры и биополимеры.  Полівінілхлорид Підготувала учениця 11-М класу Євграфова Марина
Полівінілхлорид Підготувала учениця 11-М класу Євграфова Марина 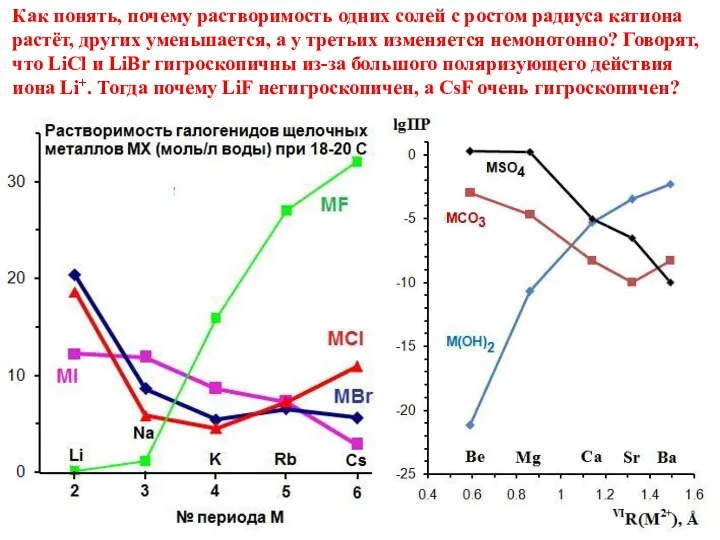 Растворимость галогенидов щелочных металлов
Растворимость галогенидов щелочных металлов The development of nanoporous hydrogen storages
The development of nanoporous hydrogen storages Скорость химической реакции
Скорость химической реакции Целлюлоза Выполнила студентка 11 группы Сыровацкая Лилия
Целлюлоза Выполнила студентка 11 группы Сыровацкая Лилия  Пластмассы. Компоненты
Пластмассы. Компоненты Поліетилен Фенолформальдегідна смола Фторопласт Поліамід Поліметилакрилат Поліпропілен Полівінілхлорид Гетинакс політетра
Поліетилен Фенолформальдегідна смола Фторопласт Поліамід Поліметилакрилат Поліпропілен Полівінілхлорид Гетинакс політетра Кислоты. (8 класс.)
Кислоты. (8 класс.) Единица количества вещества - моль
Единица количества вещества - моль Мессбауэровские исследования легированных атомами магния литиевых фосфатов железа при деинтерколяции лития
Мессбауэровские исследования легированных атомами магния литиевых фосфатов железа при деинтерколяции лития Химические элементы 5-й группы
Химические элементы 5-й группы Купрум. Знаходження в періодичній системі
Купрум. Знаходження в періодичній системі Альдегиды и кетоны
Альдегиды и кетоны Предельные углеводороды
Предельные углеводороды Начала физической химии
Начала физической химии