Содержание
- 2. В состав природных полипептидов и белков входят α-аминокислоты, в молекулах которых амино- и карбоксильная группы связаны
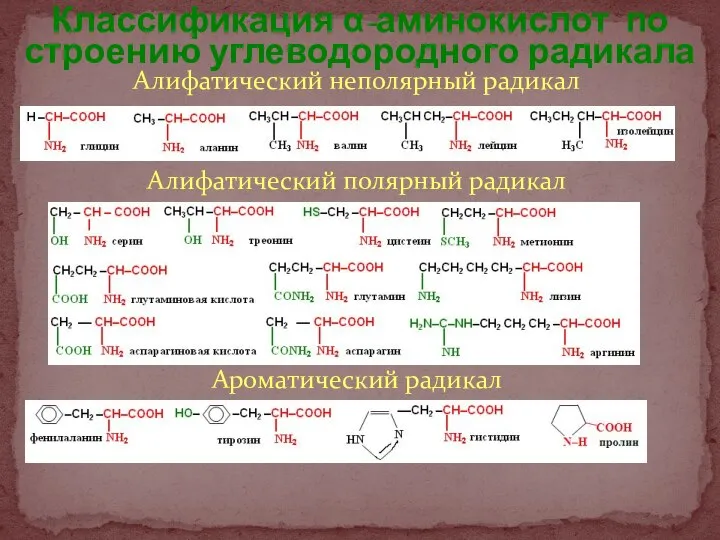
- 3. Алифатический неполярный радикал Алифатический полярный радикал Ароматический радикал Классификация α-аминокислот по строению углеводородного радикала
- 4. Незаменимые α-аминокислоты поступают в организм только из внешней среды, синтез заменимых α-аминокислот происходит в организме. Незаменимые
- 5. В молекулах α-аминокислот (кроме глицина), второй атом углерода является асимметрическим, Молекулы этих кислот несимметричны. Следо- вательно,
- 6. Конфигурация аминокислот определяет пространственную структуру и биологические свойства как самих аминокислот, биополимеров – белков, которые построены
- 7. В водных растворах и твердом состоянии аминокислоты существуют только в виде внутренних солей – цвиттер-ионов или
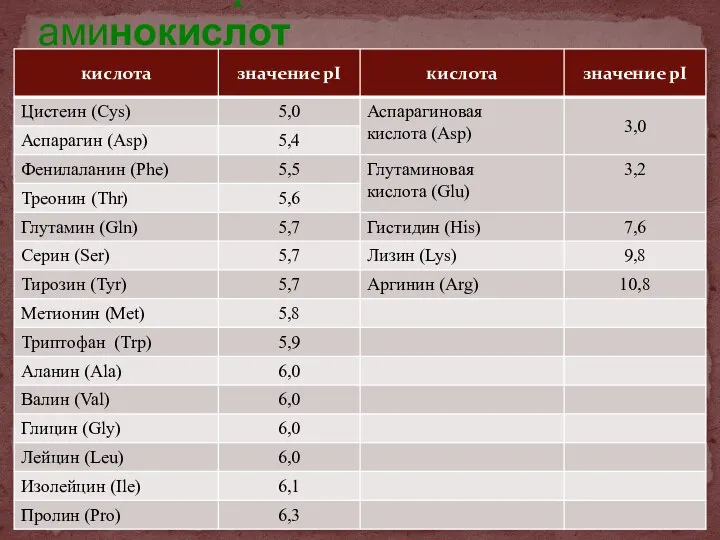
- 8. Значения pI важнейших α-аминокислот
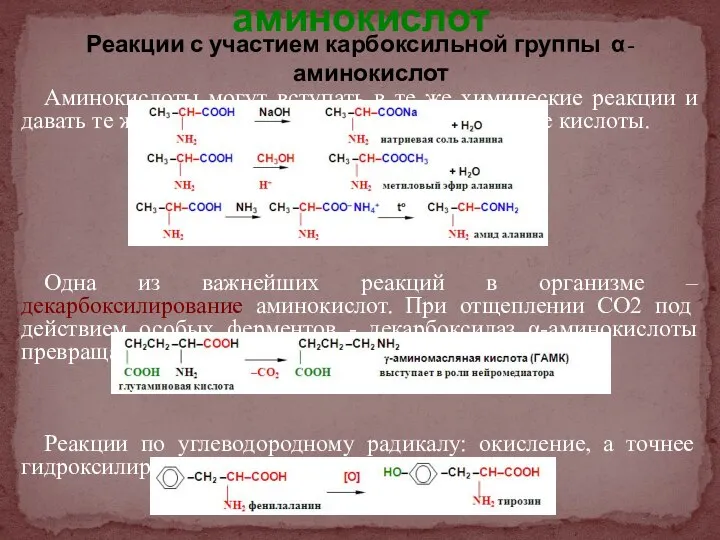
- 9. Реакции с участием карбоксильной группы α-аминокислот Аминокислоты могут вступать в те же химические реакции и давать
- 10. Реакции с участием аминогруппы α-аминокислот Как и другие алифатические амины, аминокислоты могут реагировать с кислотами, ангидридами
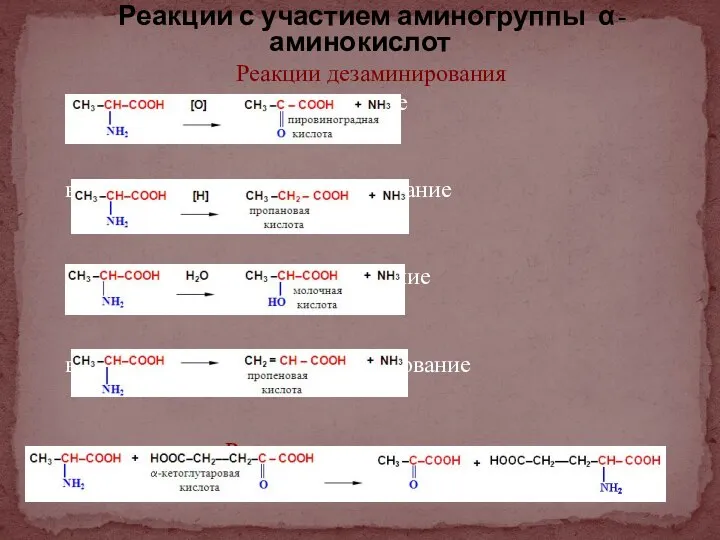
- 11. Реакции с участием аминогруппы α-аминокислот Реакции дезаминирования окислительное дезаминирование восстановительное дезаминирование гидролитическое дезаминирование внутримолекулярное дезаминирование Реакция
- 12. Образование пептидной связи Амино- и карбоксильные группы аминокислот могут реагировать друг с другом. Возникающая при этом
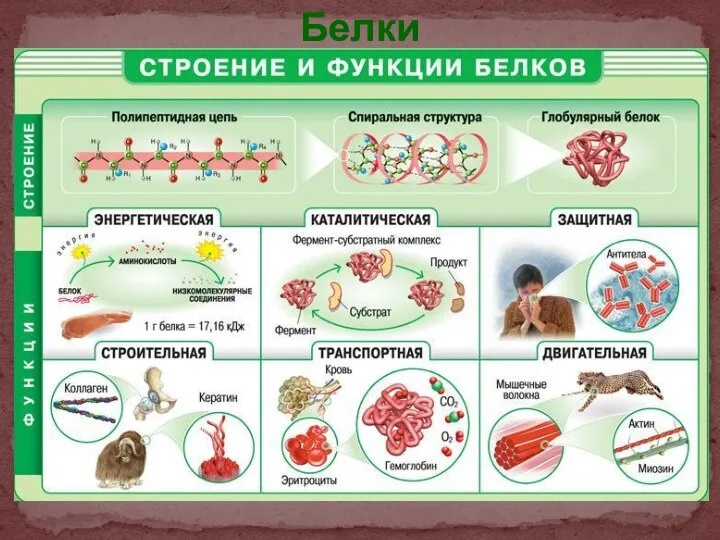
- 13. Белки
- 14. Классификация белков Белки можно классифицировать: – по форме молекул (глобулярные и фибриллярные); – по молекулярной массе
- 15. Функции белков
- 16. Альбумины. Примерно 75-80% осмотического давления белков сыворотки крови приходится на альбумины; еще одна функция – транспорт
- 17. Классификация сложных белков
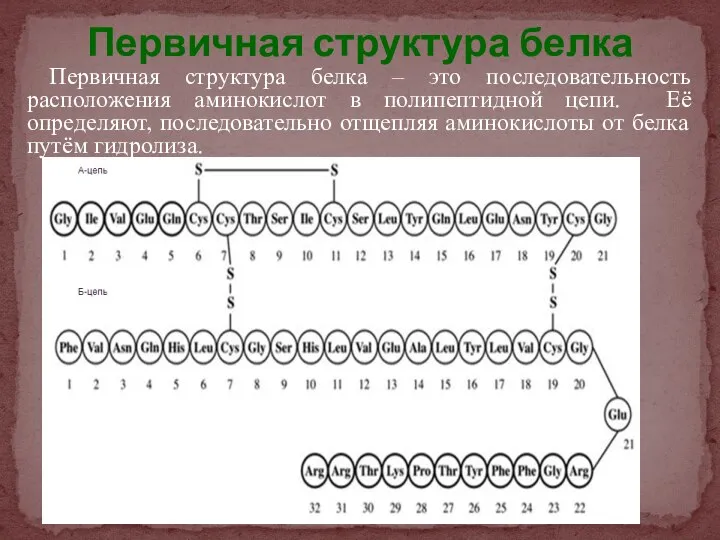
- 18. Первичная структура белка Первичная структура белка – это последовательность расположения аминокислот в полипептидной цепи. Её определяют,
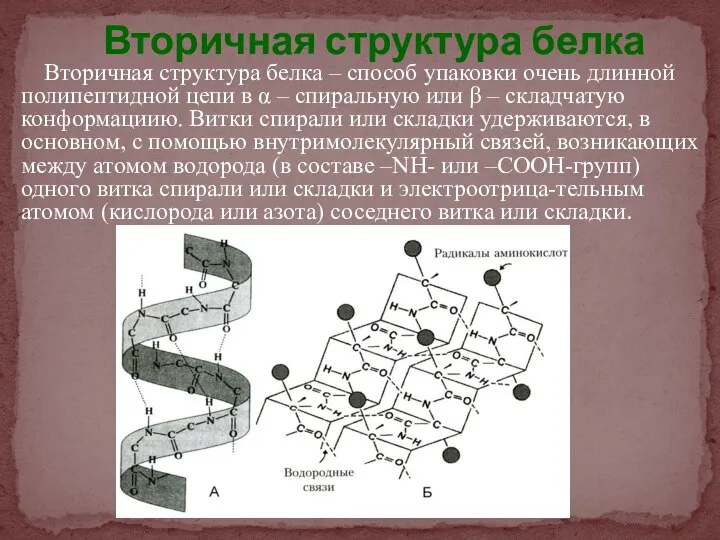
- 19. Вторичная структура белка Вторичная структура белка – способ упаковки очень длинной полипептидной цепи в α –
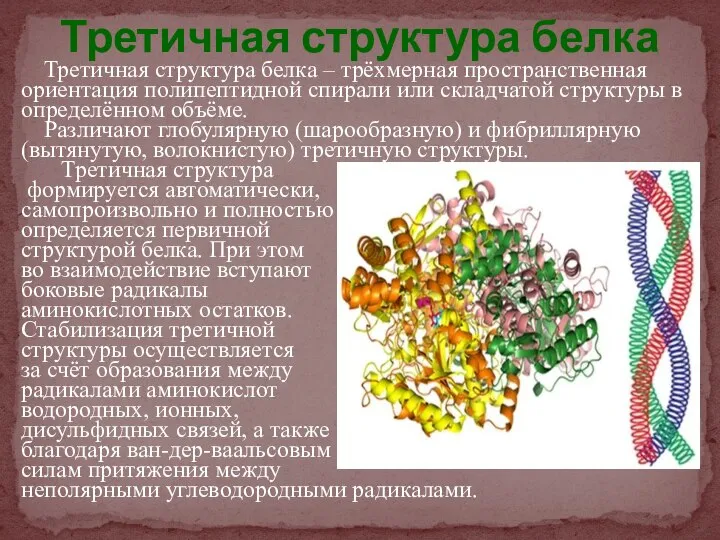
- 20. Третичная структура белка Третичная структура белка – трёхмерная пространственная ориентация полипептидной спирали или складчатой структуры в
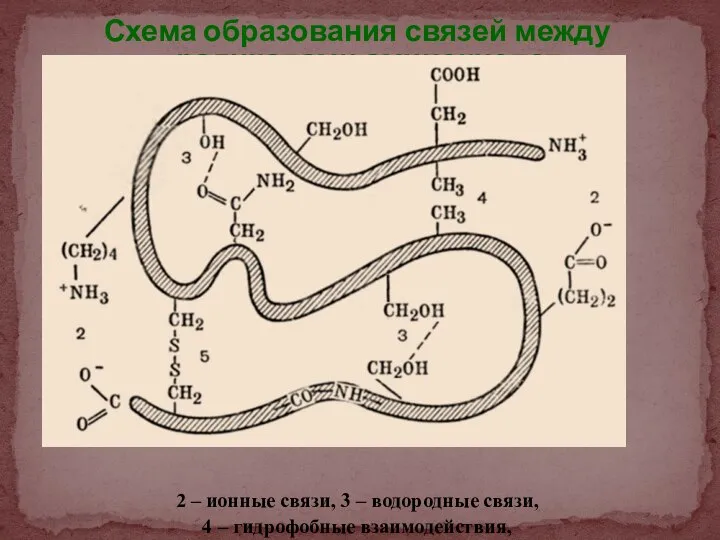
- 21. Схема образования связей между радикалами аминокислот 2 – ионные связи, 3 – водородные связи, 4 –
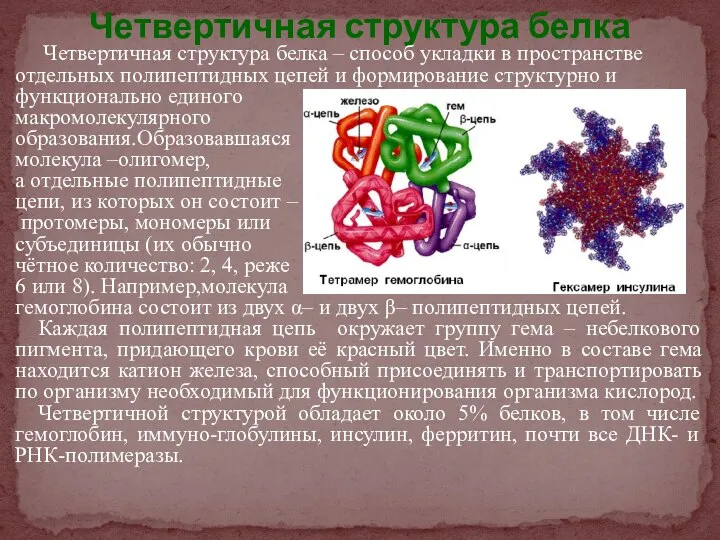
- 22. Четвертичная структура белка Четвертичная структура белка – способ укладки в пространстве отдельных полипептидных цепей и формирование
- 23. Цветные реакции для обнаружения белков и аминокислот Для идентификации пептидов, белков и отдельных аминокислот используют так
- 24. Общая скорость химической реакции определяется (лимитируется) скоростью ее наиболее медленной стадии, а скорость составляющих элементарных реакций
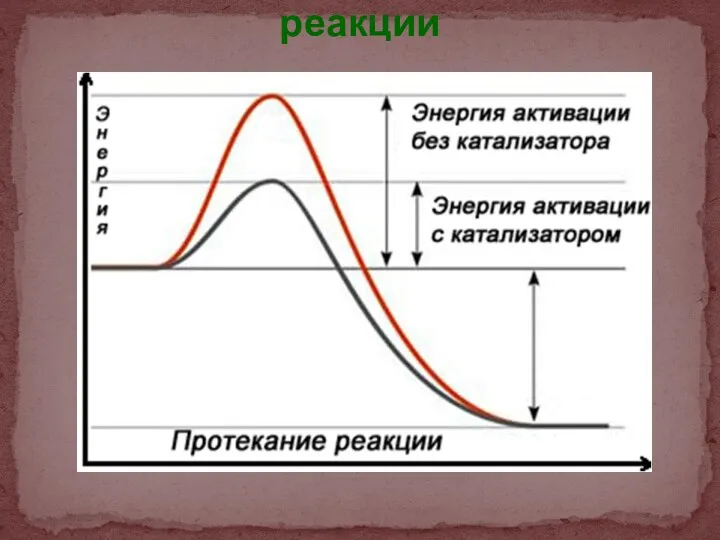
- 25. Влияние катализатора на скорость реакции
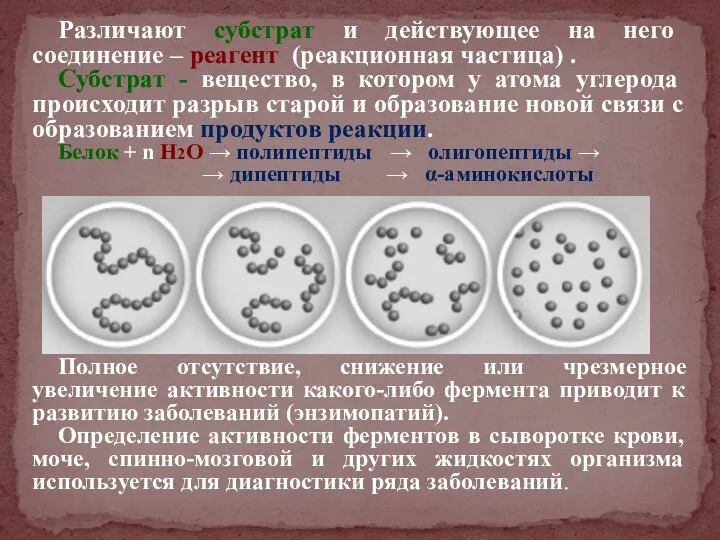
- 26. Различают субстрат и действующее на него соединение – реагент (реакционная частица) . Субстрат - вещество, в
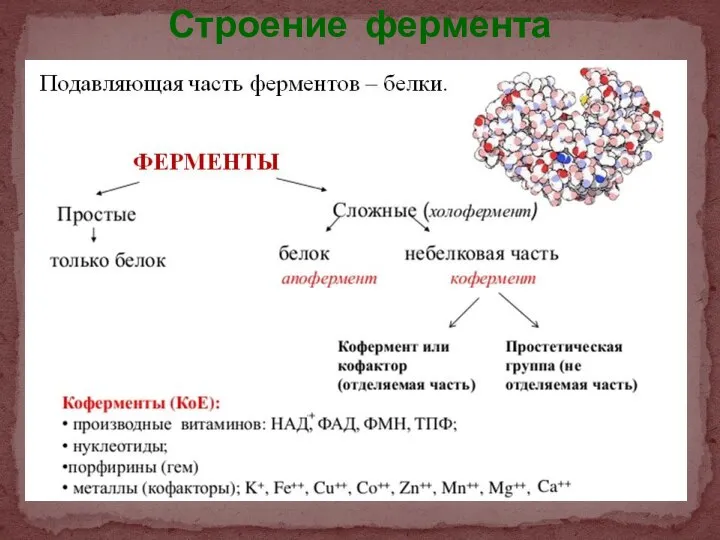
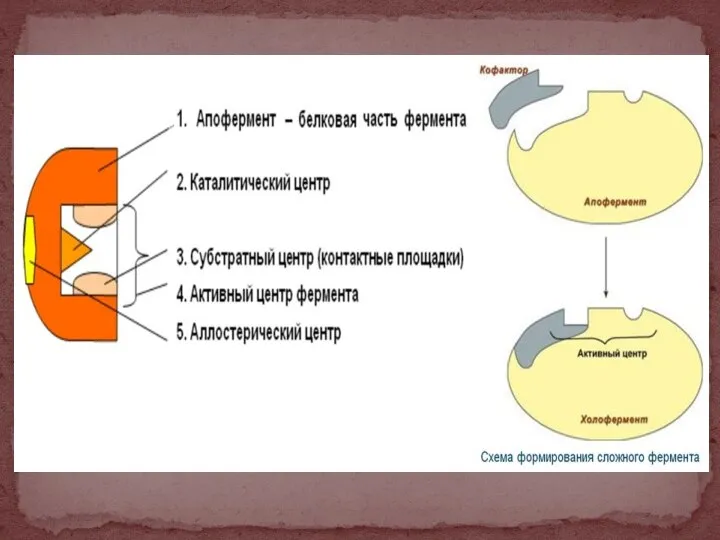
- 27. Строение фермента
- 29. Абсолютная специфичность – фермент катализирует превращение только одного вещества. Например, расщепление мочевины уреазой. Групповая (относительная) специфичность
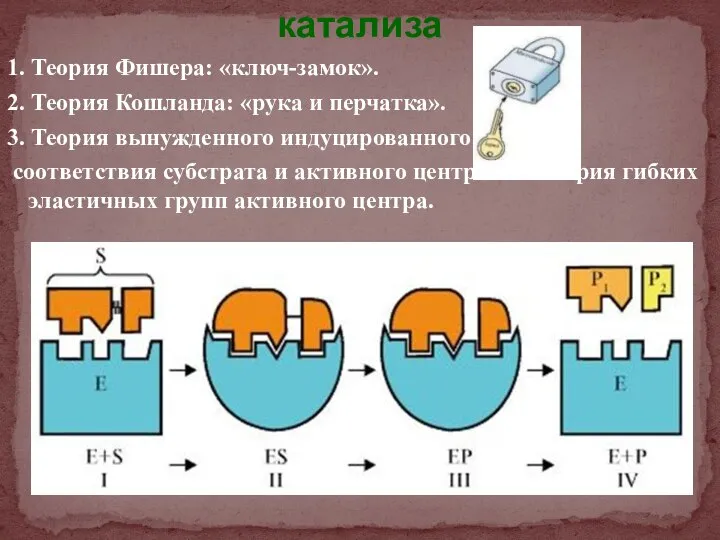
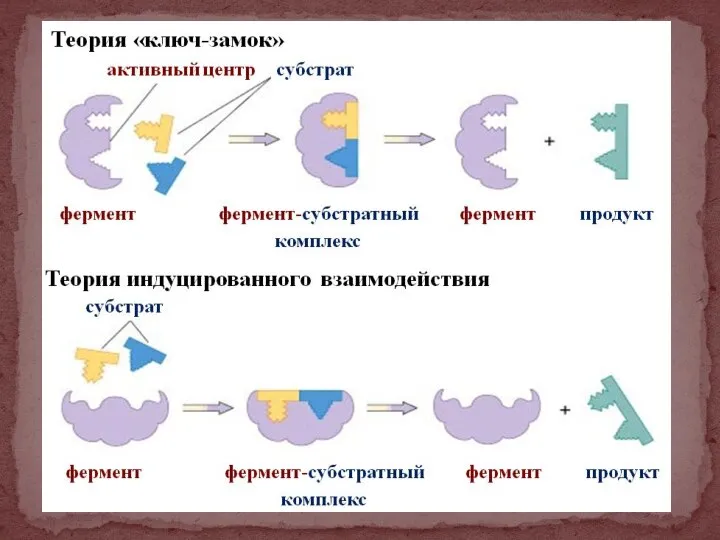
- 30. 1. Теория Фишера: «ключ-замок». 2. Теория Кошланда: «рука и перчатка». 3. Теория вынужденного индуцированного соответствия субстрата
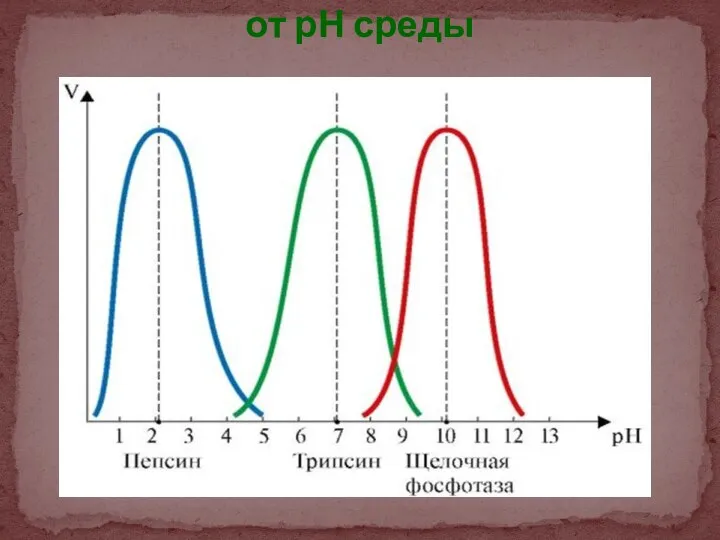
- 32. Зависимость активности фермента от рН среды
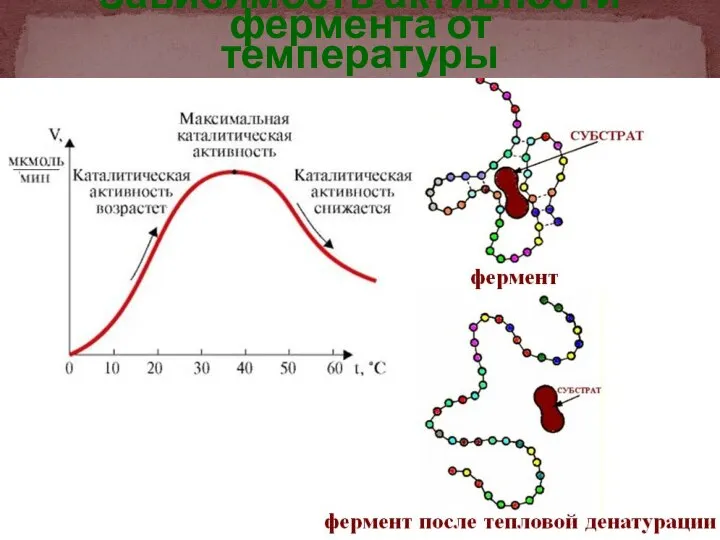
- 33. Зависимость активности фермента от температуры
- 34. Согласно современной классификации, выделяют шесть классов ферментов: оксидоредуктазы трансферазы гидролазы лиазы изомеразы лигазы Классификация ферментов
- 35. Оксидоредуктазы – катализируют окислительно-восстановительные реакции: Трансферазы – катализируют реакции межмолекулярного переноса различных атомов, групп атомов и
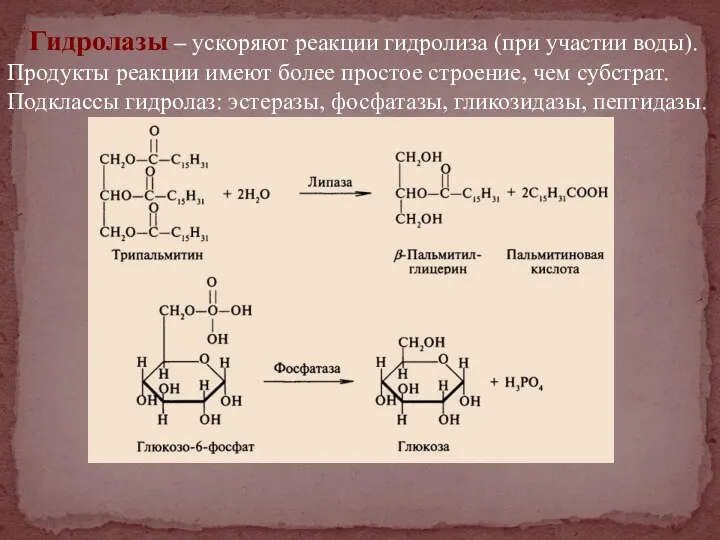
- 36. Гидролазы – ускоряют реакции гидролиза (при участии воды). Продукты реакции имеют более простое строение, чем субстрат.
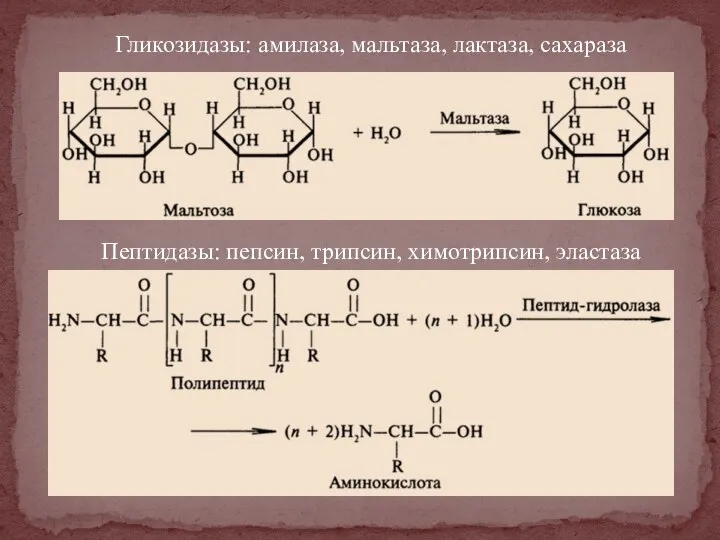
- 37. Гликозидазы: амилаза, мальтаза, лактаза, сахараза Пептидазы: пепсин, трипсин, химотрипсин, эластаза
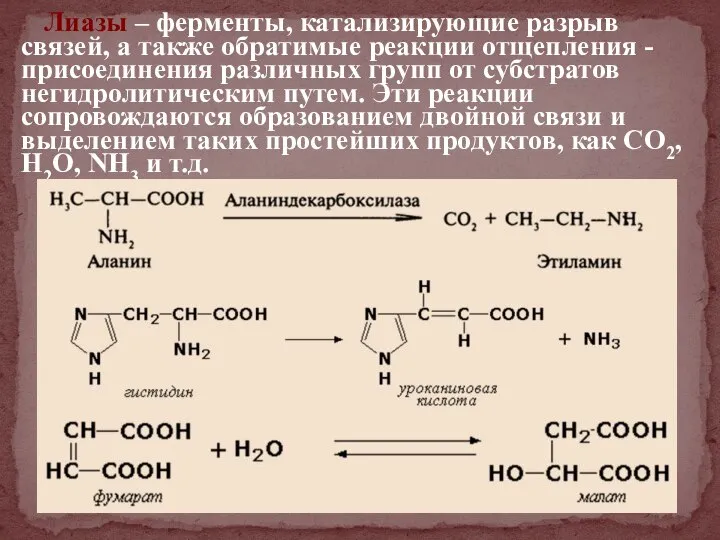
- 38. Лиазы – ферменты, катализирующие разрыв связей, а также обратимые реакции отщепления - присоединения различных групп от
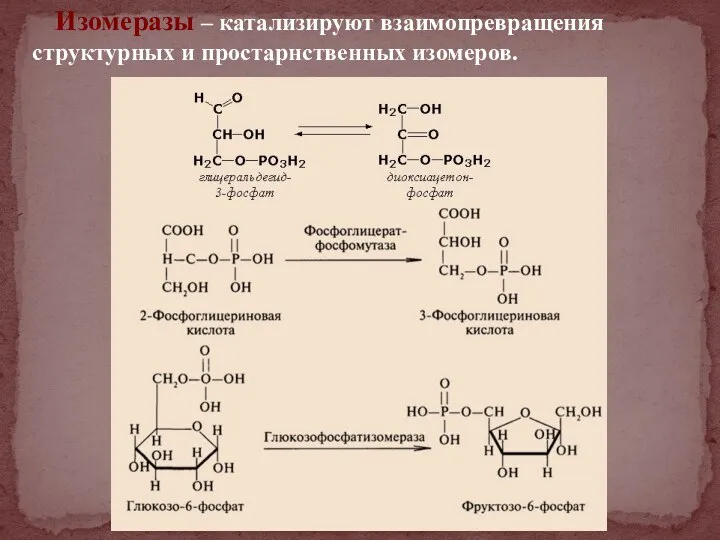
- 39. Изомеразы – катализируют взаимопревращения структурных и простарнственных изомеров.
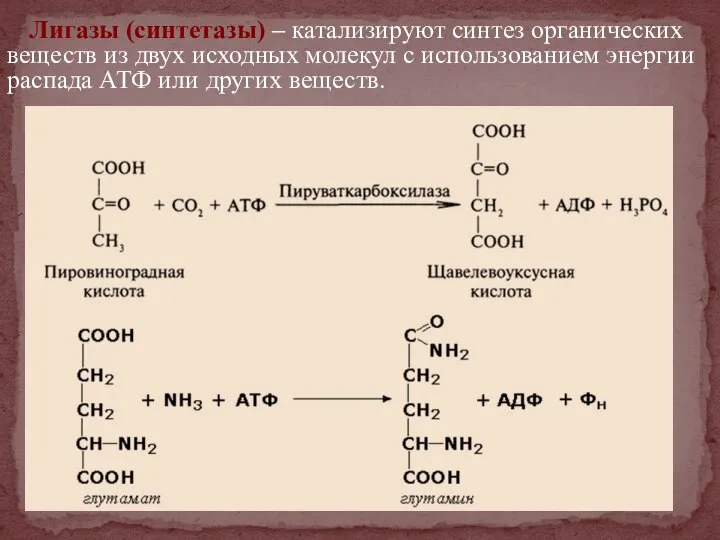
- 40. Лигазы (синтетазы) – катализируют синтез органических веществ из двух исходных молекул с использованием энергии распада АТФ
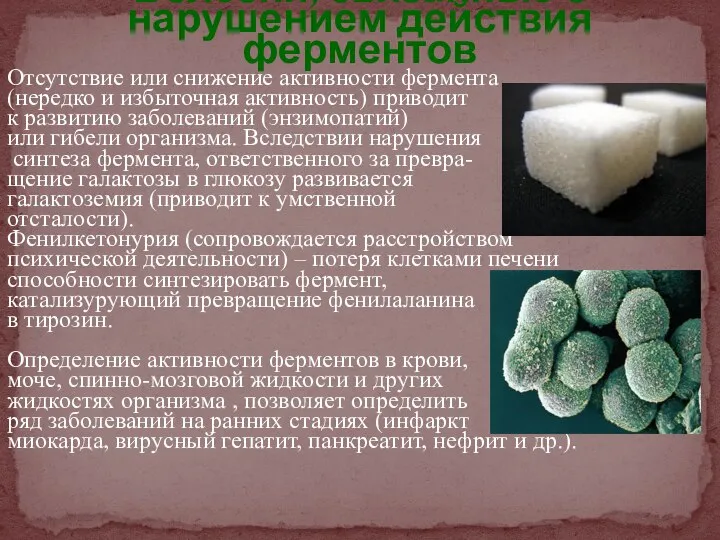
- 41. Отсутствие или снижение активности фермента (нередко и избыточная активность) приводит к развитию заболеваний (энзимопатий) или гибели
- 42. Кое-что интересное о белках Белки являются основой разного рода биологических клеев. Так, ловчие сети пауков состоят
- 43. У метилового эфира L-α-аспартил-L-фенилаланина очень сладкий вкус. СН3ООС—СН(СН2С6Н5)—NH—СО— СH(NН2)—СН2—СООН. Вещество известно под торговым названием «аспартам». Аспартам
- 44. Химические и физические свойства кожи и волос определяются свойствами кератинов. У каждого вида животных кератин имеет
- 45. Волос имеет неоднородную структуру в поперечном сечении. С точки зрения химии все слои волоса идентичны и
- 47. Скачать презентацию




















 Практическое применение метанола
Практическое применение метанола Теория создание стекла, оптические кристаллы
Теория создание стекла, оптические кристаллы Нитраты в сельскохозяйственной продукции
Нитраты в сельскохозяйственной продукции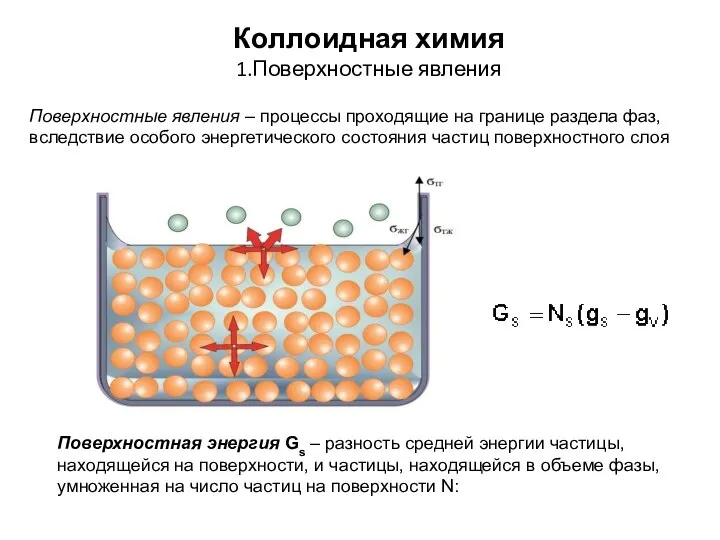 Коллоидная химия. Поверхностные явления
Коллоидная химия. Поверхностные явления Функциональные производные с простой связью C-“Э”. Часть 4 …окси-производные
Функциональные производные с простой связью C-“Э”. Часть 4 …окси-производные Презентация по Химии "«Геометрия молекул»" - скачать смотреть
Презентация по Химии "«Геометрия молекул»" - скачать смотреть  Презентация по Химии "Мыла и моющие средства" - скачать смотреть бесплатно
Презентация по Химии "Мыла и моющие средства" - скачать смотреть бесплатно Положение азота и фосфора в периодической системе химических элементов, строение их атомов. Азот: свойства и применение
Положение азота и фосфора в периодической системе химических элементов, строение их атомов. Азот: свойства и применение Нуклеофильное замещение галогена и других функциональных групп
Нуклеофильное замещение галогена и других функциональных групп Научно – исследовательская работа «Газированная вода - вред или польза?»
Научно – исследовательская работа «Газированная вода - вред или польза?» Азот. Кислородные соединения
Азот. Кислородные соединения Оценка химической обстановки при авариях на химически опасных объектах
Оценка химической обстановки при авариях на химически опасных объектах Практическая работа «Получение и свойства этилена» Автор: Алла Александровна Бочкарева, учитель химии г.Кириши Ленинградской обл
Практическая работа «Получение и свойства этилена» Автор: Алла Александровна Бочкарева, учитель химии г.Кириши Ленинградской обл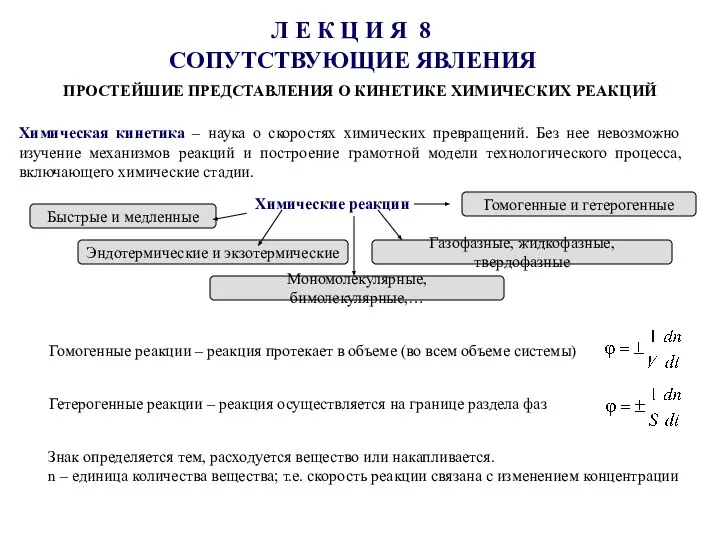 Простейшие представления о кинетике химических реакций
Простейшие представления о кинетике химических реакций Колообіг карбону у природі. Виконали: учениці 10-А класу Кирлейза Софія Мустіпан Вікторія
Колообіг карбону у природі. Виконали: учениці 10-А класу Кирлейза Софія Мустіпан Вікторія  Волшебница вода
Волшебница вода Карбонильные соединения (оксосоединения). 10 класс
Карбонильные соединения (оксосоединения). 10 класс Конструкционные материалы. Пластмассы
Конструкционные материалы. Пластмассы Энергетика химических процессов. Основы термохимии
Энергетика химических процессов. Основы термохимии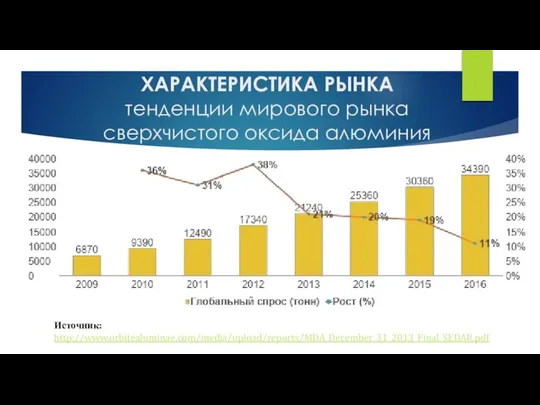 Характеристика рынка. Тенденции мирового рынка сверхчистого оксида алюминия
Характеристика рынка. Тенденции мирового рынка сверхчистого оксида алюминия Химическое равновесие
Химическое равновесие Iodine
Iodine Драгоценные камни
Драгоценные камни Учитель: Мельникова И.В.
Учитель: Мельникова И.В.  Физика древесины
Физика древесины Презентация по Химии "Способы получения металлов" - скачать смотреть
Презентация по Химии "Способы получения металлов" - скачать смотреть  Авторы: Ученики МБОУ «Клетская СОШ» Горбачева Ксения, Харитонова Мария Руководитель: Еманов Владимир Васильевич
Авторы: Ученики МБОУ «Клетская СОШ» Горбачева Ксения, Харитонова Мария Руководитель: Еманов Владимир Васильевич Оксиды. Классификация. Номенклатура. Физические и химические свойства. Получение. Применение
Оксиды. Классификация. Номенклатура. Физические и химические свойства. Получение. Применение