Содержание
- 2. Какие функциональные группы входят в состав молекул аминокислот? Конечно, это карбоксильная группа -COOH(кислотные свойства) и аминогруппа
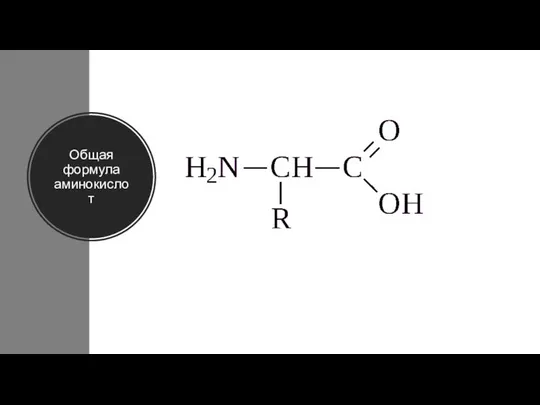
- 3. Общая формула аминокислот
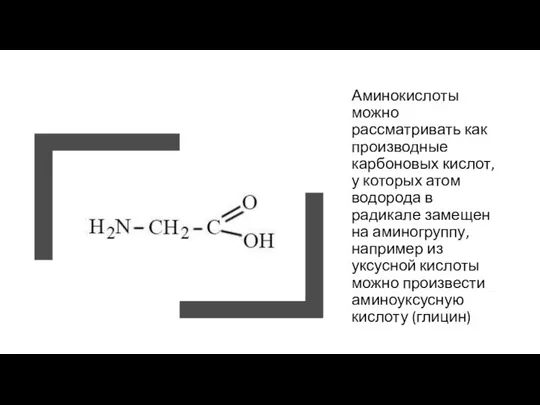
- 4. Аминокислоты можно рассматривать как производные карбоновых кислот, у которых атом водорода в радикале замещен на аминогруппу,
- 5. Еще один пример - это формула аланина (аминопропионовая кислота, или 2-аминопропановая кислота)
- 6. В природе обнаружено несколько десятков аминокислот. Некоторые же из аминокислот синтезированы человеком, поэтому аминокислоты можно разделить
- 7. Аминокислоты, как амфотерные соединения, сочетают свойства карбоновых кислот и органических оснований. Как кислоты, они взаимодействуют с
- 8. Как карбоновые кислоты, они взаимодействуют со спиртами, образуя сложные эфиры:
- 9. Как основания, аминокислоты реагируют с кислотами, образуя соли:
- 10. Важнейшим свойством аминокислот является их способность вступать в реакцию поликонденсации друг с другом:
- 11. Пептидная связь повторяется в полимере много раз, поэтому полимер соответственно называют полипептидом.
- 12. Реакция поликонденсации аминокислот имеет не только большое биологическое значение (она лежит в основе биосинтеза белков), но
- 13. В 1806 г. французские химики Луи Никола Воклен и Пьер Жан Робике исследовали состав сока некоторых
- 14. Из белка, содержащегося в зернах пшеницы, была выделена очень похожая по строению на аспарагиновую кислота, названная
- 15. Еще одно неожиданное свойство аминокислот. Предприимчивые японцы давно заметили, что добавление в пищу, приправы из сушеных
- 16. Аминокислоты и их производные используют в качестве лекарственных средств в медицине. В аптеке можно купить глицин
- 17. Существует около 20 протеиногенных аминокислот, а белков (протеинов) — великое множество. Каждый живой организм на Земле
- 18. Аналогично и в молекулах белков порядок чередования остатков аминокислот в полипептидной цепи определяет структуру белка. Эту
- 19. Рассмотрим химические свойства белков. При нагревании, под действием сильных кислот или оснований, солей тяжелых металлов и
- 20. Денатурация имеет не только отрицательные стороны. Вспомните хотя бы сваренные вкрутую яйца (свертывание белка). Похожим образом
- 21. Под действием ферментов, а также водных растворов кислот или щелочей происходит разрушение первичной структуры белка в
- 22. Белки дают две качественные реакции. Биуретовая реакция. При действии на белки свежеполученного осадка гидроксида меди (II)
- 23. Качественное определение серы в белках. При горении белков ощущается характерный запах «жженого рога». В этом легко
- 24. Рассмотрим биологическое значение белков Ферментативная функция. Большинство химических реакций в организме протекают в присутствии биологических катализаторов
- 25. Структурная функция. Белки — это строительный материал почти всех тканей: мышечных, опорных, покровных. Транспортная функция. Белковые
- 26. Защитная функция. Особые белки — антитела (своеобразные «наручники» для проникающих в клетку «преступников» - бактерий, так
- 27. Запасающая, или энергетическая, функция. Эту функцию в клетках живых организмов выполняют особые белки, например белки семян
- 29. Скачать презентацию
























 Распределение электронов в атомах. Энергетические уровни
Распределение электронов в атомах. Энергетические уровни Химические реакции
Химические реакции Периодический закон и периодическая система Д.И.Менделеева. Лекция 4
Периодический закон и периодическая система Д.И.Менделеева. Лекция 4 Медицинская химия, введение. (Лекция 1)
Медицинская химия, введение. (Лекция 1) Весы. Камни Весов
Весы. Камни Весов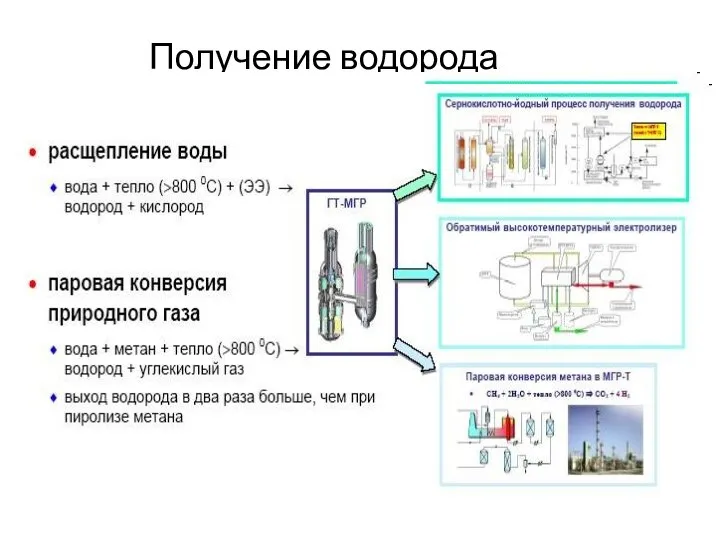 Получение водорода
Получение водорода Химический элемент фосфор
Химический элемент фосфор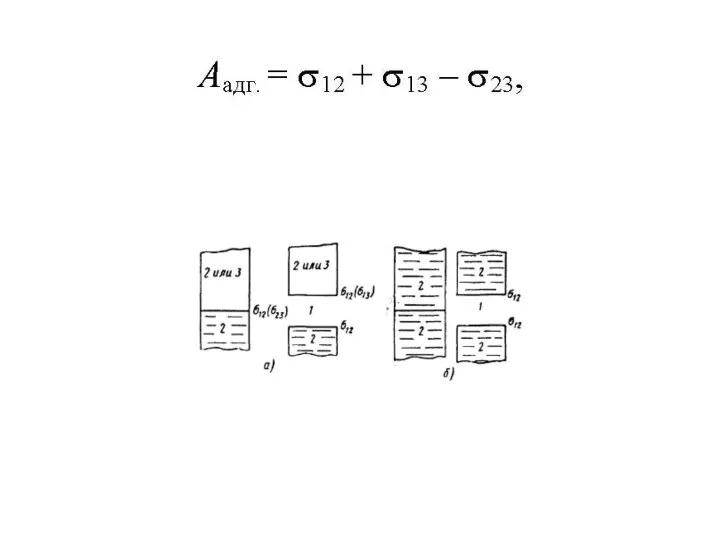 Характер затвердевания
Характер затвердевания Методы выделения и очистки продуктов биотехнологических производств
Методы выделения и очистки продуктов биотехнологических производств Соли
Соли Аэробное окисление углеводов. (Часть 2)
Аэробное окисление углеводов. (Часть 2) История мыла
История мыла  Водные растворы в условиях промышленного производства и их стандартизация
Водные растворы в условиях промышленного производства и их стандартизация 6-я группа элементов. 9 класс
6-я группа элементов. 9 класс Ковалентная неполярная химическая связь.
Ковалентная неполярная химическая связь.  Количество вещества. Моль. Молярная масса
Количество вещества. Моль. Молярная масса Вода и минеральные вещества. (Лекция 2)
Вода и минеральные вещества. (Лекция 2) Сплавы металлов
Сплавы металлов  Презентация по Химии "Исследование качества молока коровьего" - скачать смотреть бесплатно
Презентация по Химии "Исследование качества молока коровьего" - скачать смотреть бесплатно Вуглеводи прості і складні
Вуглеводи прості і складні Полимерные материалы и изделия. (Лекция 16)
Полимерные материалы и изделия. (Лекция 16) Cвойства цементного камня с введением кольматирующей добавки системы «Пенетрон-Адмикс»
Cвойства цементного камня с введением кольматирующей добавки системы «Пенетрон-Адмикс» Составление уравнений окислительно-восстановительных реакций
Составление уравнений окислительно-восстановительных реакций Оптические свойства коллоидных растворов
Оптические свойства коллоидных растворов Електрофорез
Електрофорез Химический процесс. Практические занятия
Химический процесс. Практические занятия Физико-диагностические свойства минералов
Физико-диагностические свойства минералов Решение экспериментальных задач по теме металлы
Решение экспериментальных задач по теме металлы