Содержание
- 3. Создание и эволюция Периодической системы 8 элементов известны с древности – Fe, Ag, Au, Hg, Pb,
- 4. 1829 г. ТРИАДЫ И. Деберейнера: группы из трех элементов со сходными химическими свойствами ( Cl, Br,
- 5. в периоде не более 8 элементов????? -Разграничение понятий атомная и молекулярная масса, разработка методик их точного
- 6. - 1864 г. классификация Олдинга : элементы располагаются в порядке возрастания их атомных масс и валентности
- 7. Недостатки таблицы Л. Мейера: некоторые элементы расположены неверно, цель работы – формальная классификация известных к тому
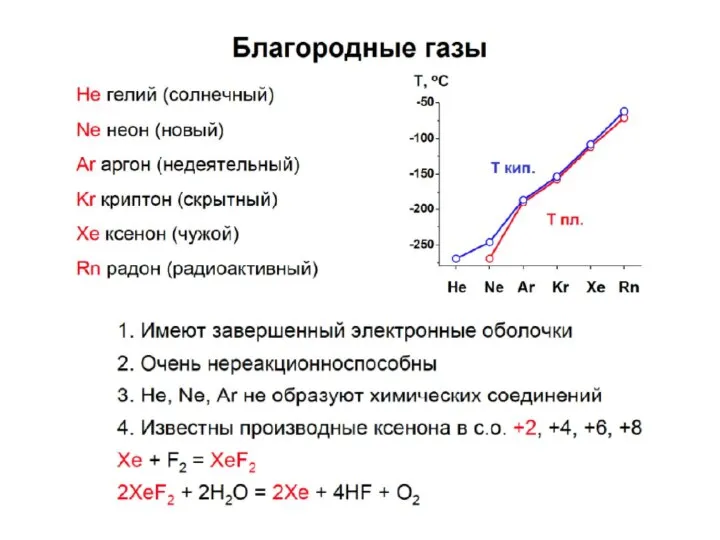
- 10. 1894-1900 гг. открытие благородных газов (Д.Рэлей, У. Рамзай, В. Дорн) привело к появлению новой VIII группы
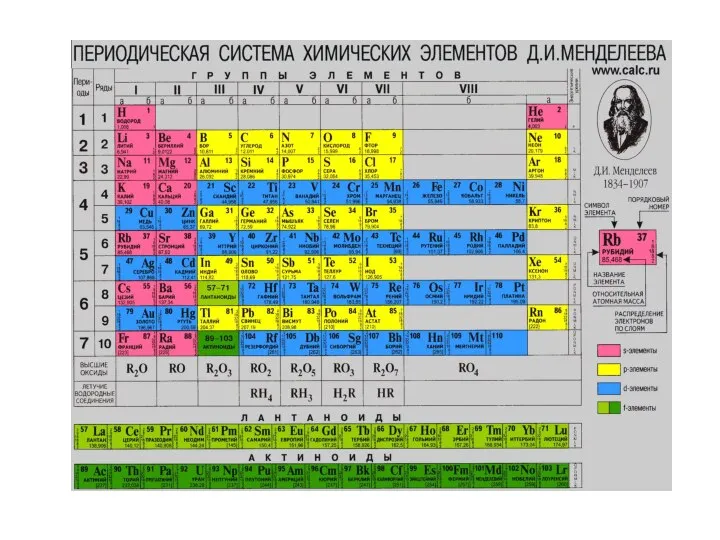
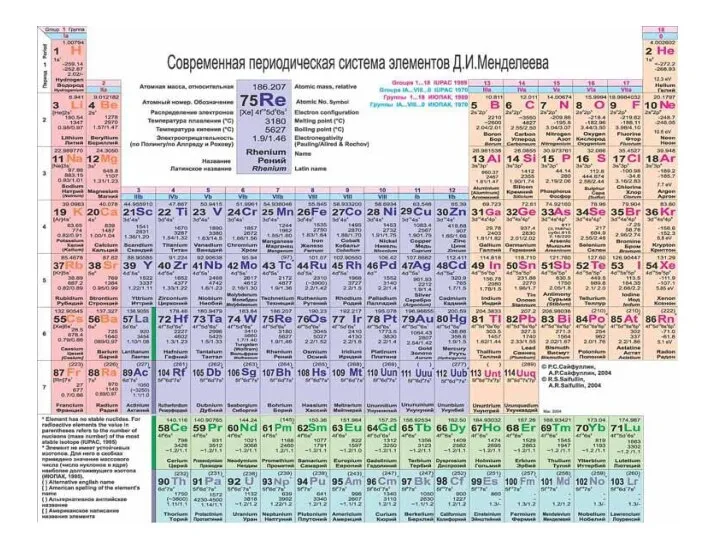
- 12. СТРУКТУРА ПЕРИОДИЧЕСКОЙ ТАБЛИЦЫ (короткая форма) Горизонтальные ряды – ПЕРИОДЫ (1-7) Малые (короткие) периоды (1,3) – 8
- 14. Электронное строение атома и периодичность свойств химических элементов Номер периода = числу энергетических уровней в атоме
- 17. Электронные аналоги – атомы и ионы с однотипным распределением внешних электронов Li 1s22s1 и Na 1s22s22p63s1
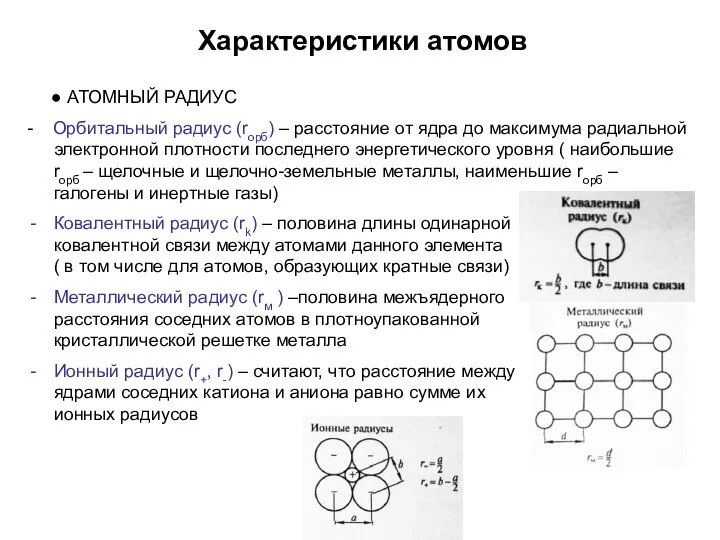
- 18. Характеристики атомов ● АТОМНЫЙ РАДИУС - Орбитальный радиус (rорб) – расстояние от ядра до максимума радиальной
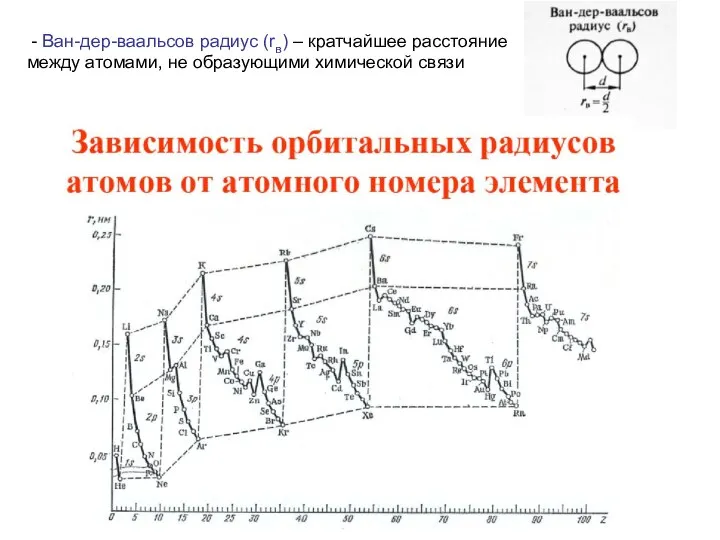
- 19. - Ван-дер-ваальсов радиус (rв) – кратчайшее расстояние между атомами, не образующими химической связи
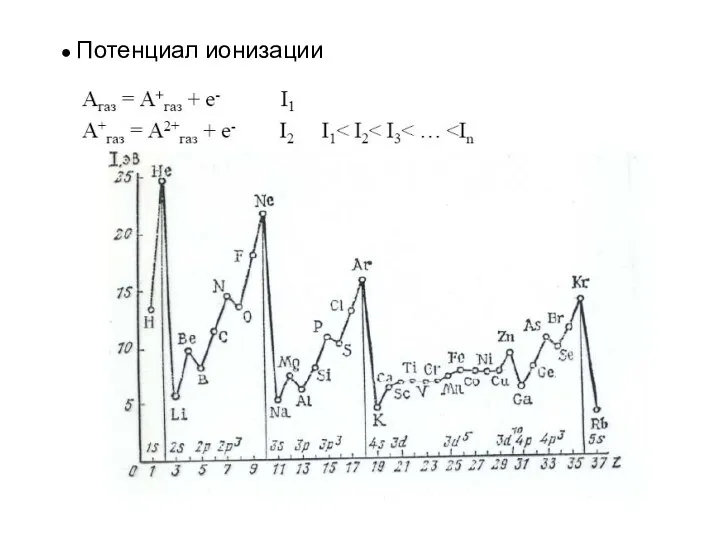
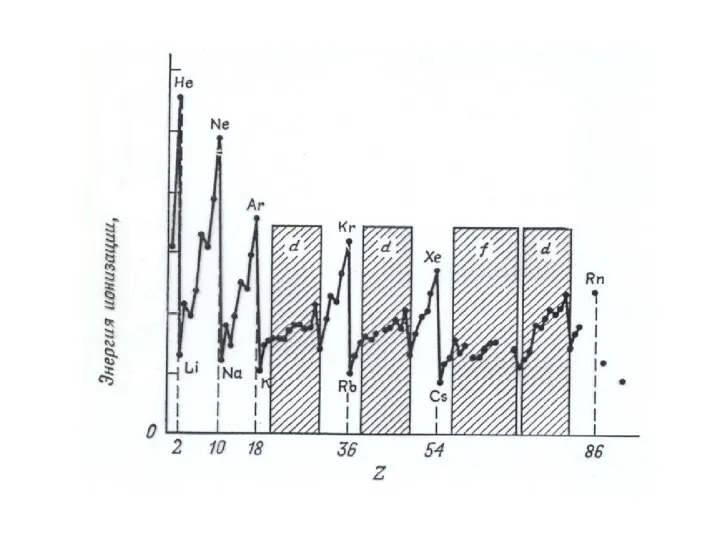
- 20. ● Потенциал ионизации
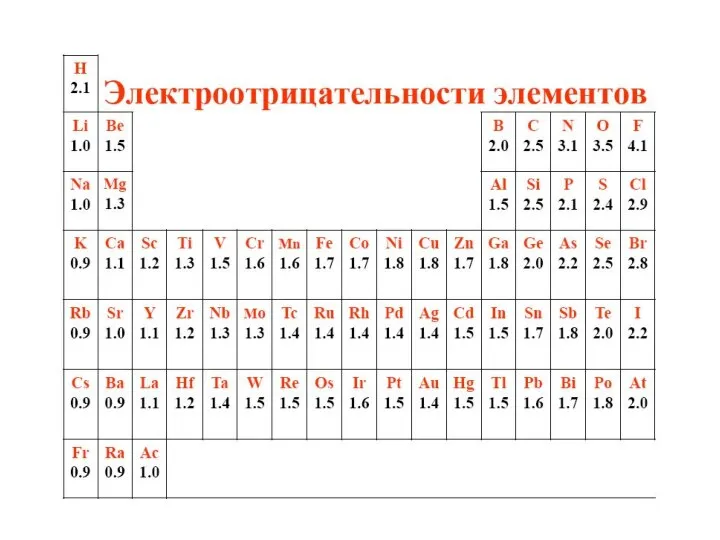
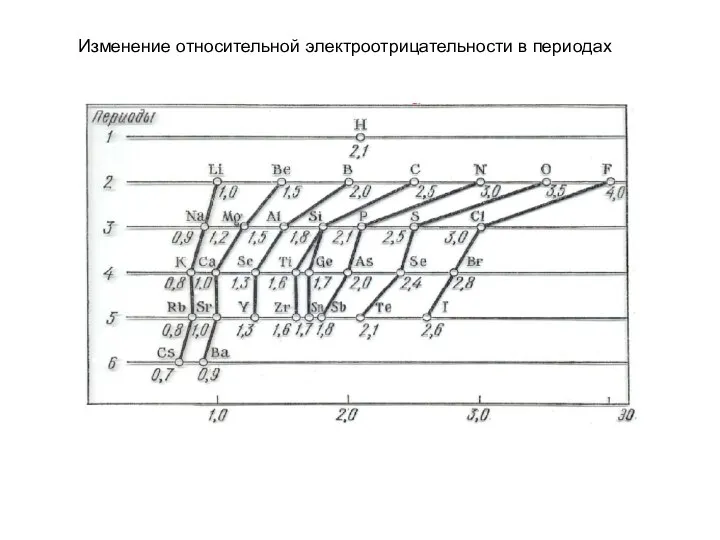
- 24. Изменение относительной электроотрицательности в периодах
- 34. Скачать презентацию
















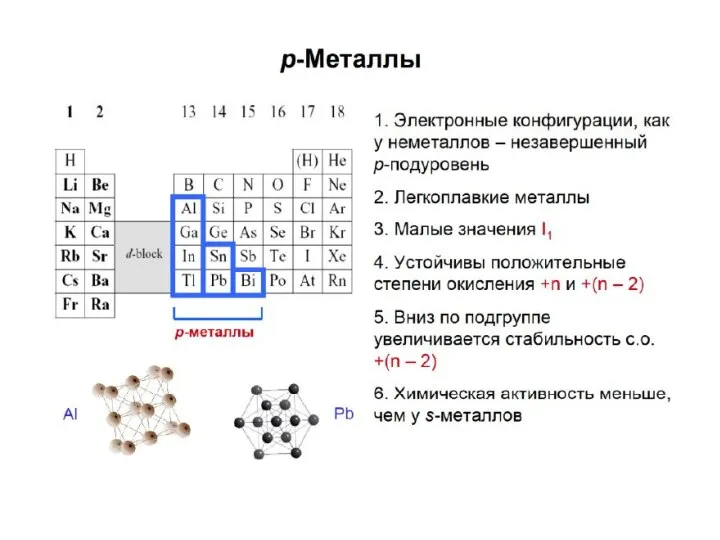
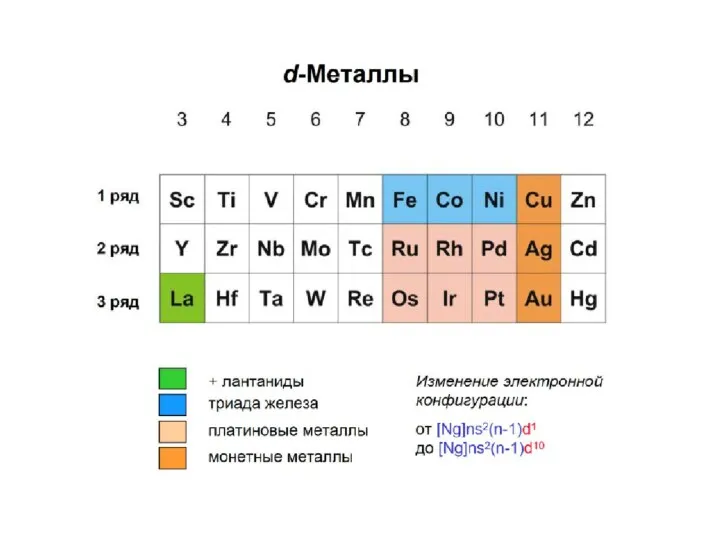

 Химический брейн-ринг
Химический брейн-ринг Вольфра́м — химический элемент с атомным номером 74 в Периодической системе химических элементов Д. И. Менделеева
Вольфра́м — химический элемент с атомным номером 74 в Периодической системе химических элементов Д. И. Менделеева Характеристика и технология производства основных катализаторов нефтепереработки
Характеристика и технология производства основных катализаторов нефтепереработки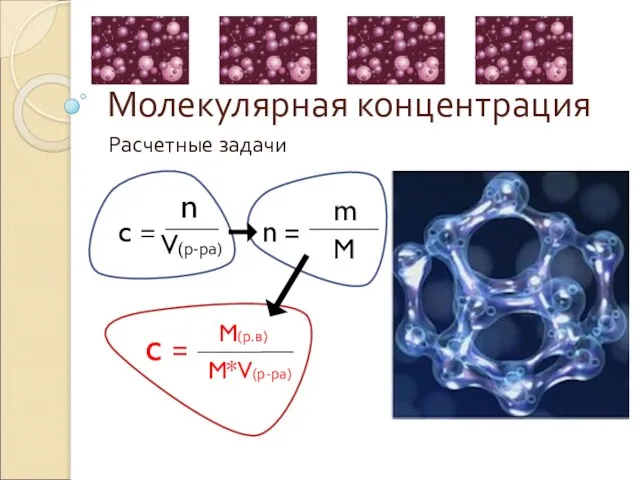 Молекулярная концентрация Расчетные задачи
Молекулярная концентрация Расчетные задачи Презентация по Химии "Мир кристаллов медного купороса" - скачать смотреть
Презентация по Химии "Мир кристаллов медного купороса" - скачать смотреть  Основные химические понятия
Основные химические понятия Закон действующих масс и его использование в расчетах. (Лекциии 4-6)
Закон действующих масс и его использование в расчетах. (Лекциии 4-6) XIII конференция ИХТРЭМС «Научно-практические проблемы в области химии и химических технологий»
XIII конференция ИХТРЭМС «Научно-практические проблемы в области химии и химических технологий» Презентация по Химии "Основные классы неогранических соединений" - скачать смотреть
Презентация по Химии "Основные классы неогранических соединений" - скачать смотреть  Переработка нефти. (10 класс)
Переработка нефти. (10 класс) Классификация элементов. Электрохимическая цепь
Классификация элементов. Электрохимическая цепь История получения алюминия и его применение
История получения алюминия и его применение Поняття ПРО СИНТЕТИЧНІ ЛІКАРСЬКІ ЗАСОБИ НА ПРИКЛАДІ АСПІРИНУ
Поняття ПРО СИНТЕТИЧНІ ЛІКАРСЬКІ ЗАСОБИ НА ПРИКЛАДІ АСПІРИНУ Введение в органическую химию. 10 класс
Введение в органическую химию. 10 класс Green chemistry application to intermolecular forces
Green chemistry application to intermolecular forces Основы химической термодинамики
Основы химической термодинамики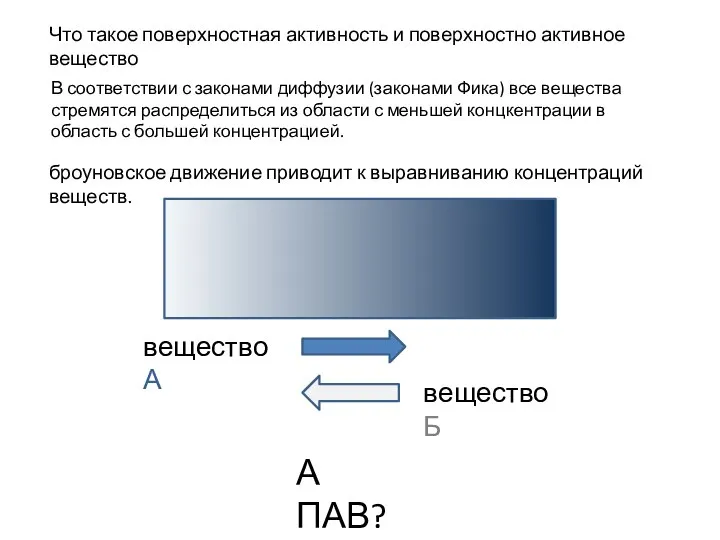 Поверхностная активность и поверхностно активное вещество
Поверхностная активность и поверхностно активное вещество Титан. История открытия титана
Титан. История открытия титана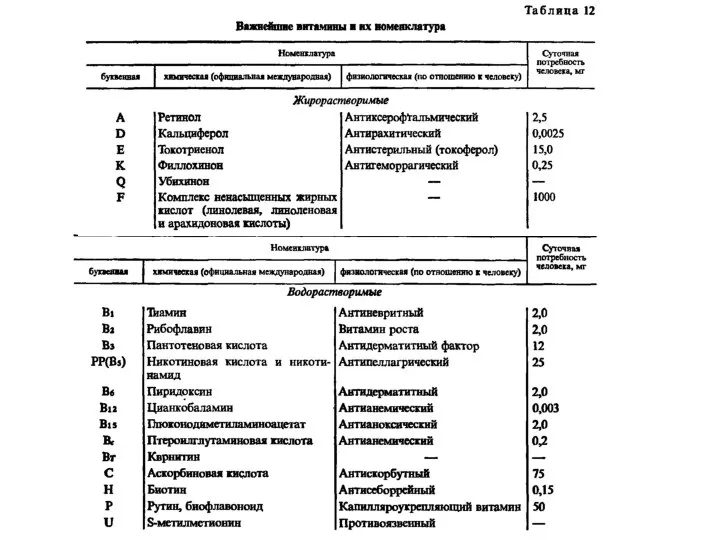 Важнейшие витамины и их номенклатура
Важнейшие витамины и их номенклатура Галогены. Химические свойства. Применение
Галогены. Химические свойства. Применение Железоуглеродистый сплав чугун
Железоуглеродистый сплав чугун Презентация для класса Способы получения натрия
Презентация для класса Способы получения натрия  Презентация по Химии "Белки" - скачать смотреть бесплатно_
Презентация по Химии "Белки" - скачать смотреть бесплатно_ Понятие синтетических лекарственных препаратов
Понятие синтетических лекарственных препаратов  Фосфор в природе
Фосфор в природе Циклічна обернено-похідна хронопотенціометрія пірокатехіну та його похідних
Циклічна обернено-похідна хронопотенціометрія пірокатехіну та його похідних Презентация по Химии "Теория строения химических соединений А.М. Бутлерова" - скачать смотреть
Презентация по Химии "Теория строения химических соединений А.М. Бутлерова" - скачать смотреть  Электролиз Цель: изучить сущность процесса электролиза Задачи: раскрыть принцип работы электролизёра суть катодных и анодных
Электролиз Цель: изучить сущность процесса электролиза Задачи: раскрыть принцип работы электролизёра суть катодных и анодных