БИОГЕННЫЕ S–ЭЛЕМЕНТЫ s-Элементы – это элементы, в атомах которых заполняется электронами s-подуровень внешнего электронного уров
Содержание
- 2. Общая характеристика
- 3. Натрий, химические свойства Электронная формула: 11Na 1s22s22p63s1; c.o.+1, комплексообразование не характерно. 2Na+Cl2=2NaCl хлорид натрия 2Na+S=Na2S сульфид
- 4. Натрий, химические свойства Для регенерации воздуха в замкнутых помещениях используется реакция: 2Na2O2+2CO2=2Na2CO3+O2 Na2O2+Na=2Na2O оксид натрия, основный
- 5. Топография ω(Na) в организме=0,08%, макроэлемент, при массе тела 70 кг масса натрия 60г. Топография натрия: Na+-
- 6. Биороль натрия: 1. Поддерживает постоянное осмотическое давление в 7,7 атм. (осмотический гомеостаз). 2. Поддерживает постоянное значение
- 7. Избыток и дефицит Na: Избыток Na+ в клетках головного мозга угнетает ЦНС, вызывает депрессию. Недостаток Na+
- 8. Лекарственные препараты: 1. NaCl - 0,9%-ный раствор, физиологический раствор, изотонический раствор. Внутривенно при интоксикациях и обезвоживании,
- 9. Лекарственные препараты: б) при повышенной кислотности желудочного сока: NaHCO3+HCl=NaCl+H2O+CO2↑ в) слабый антисептик, т.к. в результате гидролиза
- 10. Калий Электронная формула: 19К 1s22s22p63s23p64s1, с.о.=+1, комплексообразование не характерно. ω(К) в организме=0,23%, макроэлемент, масса калия в
- 11. Биороль К: Участвует в сокращении мышц, способствует мышечному расслаблению. Участвует в проведении нервных импульсов (совместно с
- 12. Избыток и недостаток: Избыток K+ ведет к снижению содержания Na+, внеклеточная среда становится гипотонической и происходит
- 13. Гипокалиемия
- 14. Лекарственные препараты: KCl – при гипокалиемии, аритмии, рвоте. KI – при эндемическом зобе. KMnO4 – сильный
- 15. Кальций Электронная формула: 20Ca 1s22s22p63s23p64s2, с.о.=+2, координационное число в комплексных соединений 6,7,8. Кальций образует несимметричные комплексы
- 16. Химические свойства: Ca+S=CaS сульфид кальция Ca+Cl2=CaCl2 хлорид кальция 3Ca+N2=Ca3N2 нитрид кальция Ca+H2=CaH2 гидрид кальция Ca+2H2O=Ca(OH)2+H2↑ гидроксид
- 17. Химические свойства: CaO+CO2=CaCO3 карбонат кальция, мел CaO+H2O=Ca(OH)2 Ca(OH)2+2CO2=Ca(HCO3)2 гидрокарбонат кальция Ca(HCO3)2→CaCO3↓+H2O+CO2↑ Ca(OH)2+2HCl=CaCl2+2H2O Ca(OH)2+H2SO4=CaSO4↓+2H2O сульфат кальция
- 18. Са in vivo ω (Ca) в организме = 1, 4%, макроэлемент, масса кальция ~ 1,5 кг.
- 19. Биороль кальция: 1. Является основным минеральным компонентом костной и зубной ткани в виде гидроксил- и фторапатитов
- 20. Избыток и недостаток: Суточная потребность ~ 1г. При недостатке Ca2+ : снижение свертываемости крови, судороги, конвульсии,
- 21. Дефицит кальция. Тонические судороги мышц кисти руки.
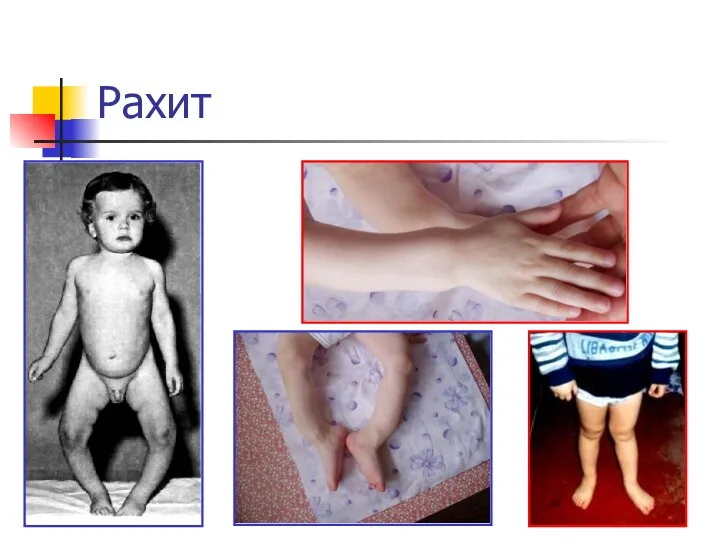
- 22. Рахит
- 23. Остеопороз
- 24. Артроз
- 25. Лекарственные препараты кальция: 1. CaCO3 – мел осажденный, антацидное средство, применяется для уменьшения кислотности желудочного сока:
- 26. Магний Электронная формула: 12Mg 1s22s22p63s2, с.о.=+2, координационное число 6, магний образует комплексы с биолигандами, в составе
- 27. Биороль магния: 1. Регулирует артериальное давление. 2. Уменьшает спазм сосудов. 3. Регулирует работу сердца ( при
- 28. Mg in vivo ω(Mg)в организме=0,027%, макроэлемент, масса магния в организме 20г. Топография: дентин и эмаль зубов,
- 29. Избыток и недостаток Mg: В организм поступает с пищей: рыба, морская капуста, соя, какао, грецкие орехи,
- 30. Лекарственные препараты: MgO - жженая магнезия, антацидное средство без побочного действия: MgO+2HCl=MgCl2+H2O. MgO+MgO2 – «магний перекись»,
- 32. Скачать презентацию




























 Тема: Химическая связь и ее типы Урок химии в 11 классе
Тема: Химическая связь и ее типы Урок химии в 11 классе Методы защиты металлов от электрохимической коррозии. Классификация методов защиты
Методы защиты металлов от электрохимической коррозии. Классификация методов защиты Строение и переваривание липидов. Классификация и роль жирных кислот. Нутриомика. Липофильных соединений
Строение и переваривание липидов. Классификация и роль жирных кислот. Нутриомика. Липофильных соединений Презентация по Химии "Глюкоза. Строение. Физические и химические свойства" - скачать смотреть
Презентация по Химии "Глюкоза. Строение. Физические и химические свойства" - скачать смотреть  Строение атома. Периодическая таблица Менделеева. Химическая связь
Строение атома. Периодическая таблица Менделеева. Химическая связь Alkanes. A “family” of hydrocarbons
Alkanes. A “family” of hydrocarbons Фенол Подготовил Ежов Сергей
Фенол Подготовил Ежов Сергей Орагническая химия. Теория А.М. Бутлерова
Орагническая химия. Теория А.М. Бутлерова Продолжение лекции «Химическая связь»
Продолжение лекции «Химическая связь»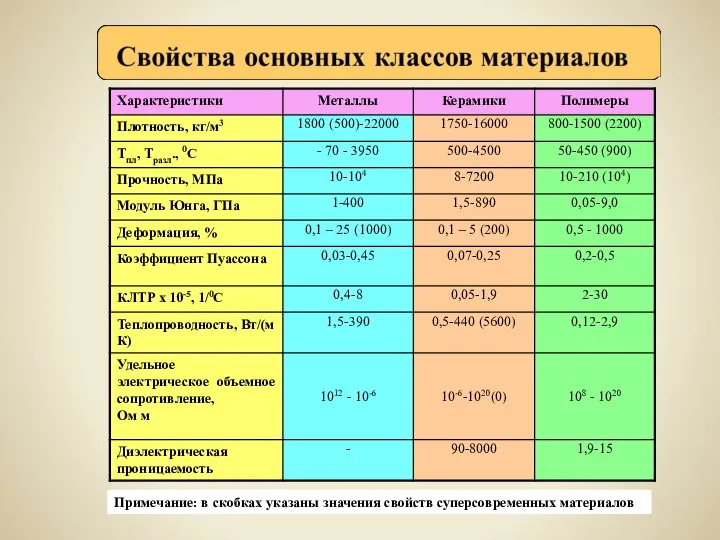 Свойства основных классов материалов
Свойства основных классов материалов Алканы и алкены
Алканы и алкены Физические, химические свойства предельных и непредельных карбоновых кислот, получение
Физические, химические свойства предельных и непредельных карбоновых кислот, получение Логическая структура модуля по дисциплине Аналитическая химия
Логическая структура модуля по дисциплине Аналитическая химия Аммофос өндірісі. Алыну әдісі
Аммофос өндірісі. Алыну әдісі Лабораторные занятия по теме: Методы защиты электрооборудования от коррозии
Лабораторные занятия по теме: Методы защиты электрооборудования от коррозии Мұнайды өңдеудің химиялық процестерінің теориялық негіздері
Мұнайды өңдеудің химиялық процестерінің теориялық негіздері Гидролиз солей. Составила: Рудчинкова Л.Ю., учитель химии и биологии МОУ «СОШ им. М.М. Рудченко с. Перелюб Перелюбского района Сарато
Гидролиз солей. Составила: Рудчинкова Л.Ю., учитель химии и биологии МОУ «СОШ им. М.М. Рудченко с. Перелюб Перелюбского района Сарато Скорость реакции и температура. (Лекция 10)
Скорость реакции и температура. (Лекция 10) Межкристаллитная коррозия МКК
Межкристаллитная коррозия МКК Механизмы двухсубстатных реакций
Механизмы двухсубстатных реакций Начала физической химии
Начала физической химии Альдегиды и кетоны: свойства, получение, применение
Альдегиды и кетоны: свойства, получение, применение Исследование фазовых и структурных превращений в железе и его сплавах магнитным методом
Исследование фазовых и структурных превращений в железе и его сплавах магнитным методом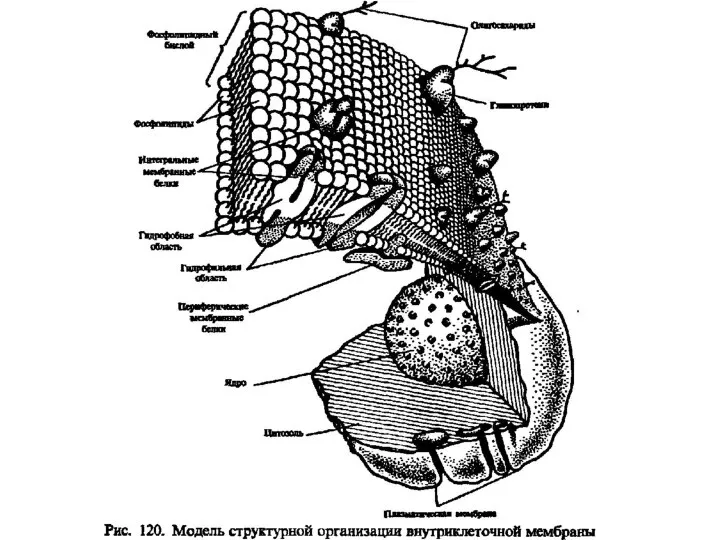 Липиды. Классификация липидов
Липиды. Классификация липидов Орбитали и связи
Орбитали и связи Общая и медицинская химия
Общая и медицинская химия Циклоалканы. Строение, изомерия, получение и свойства
Циклоалканы. Строение, изомерия, получение и свойства Белки. Структуры белков
Белки. Структуры белков