Содержание
- 2. Основные минералы кернит Na2B4O7·4H2O бура Na2B4O7·10H2O колеманит Ca2B6O11·5H2O датолит 2CaO·B2O3·2SiO2·H2O индерит 2MgO·3B2O3·15H2O улексит Na2O·2CaO·5B2O3·16H2O
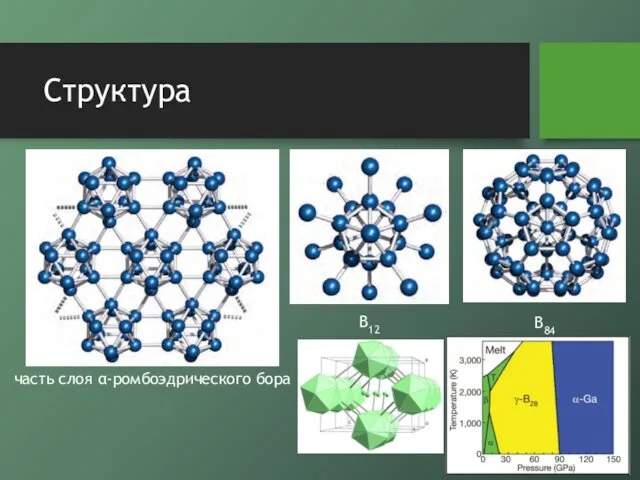
- 3. Структура часть слоя α-ромбоэдрического бора B84 B12
- 4. Получение металлотермия (чистота 95—98 %) электролитическое восстановление боратов в расплаве KCl/KF при 800°С (чистота 95%) восстановление
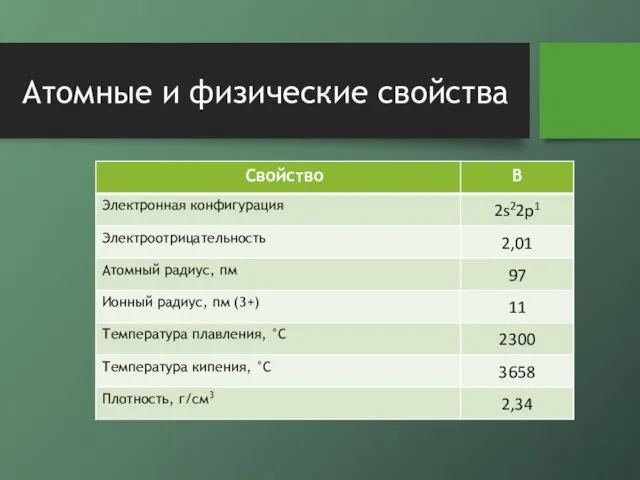
- 5. Атомные и физические свойства
- 6. Простое вещество при комнатной температуре довольно инертен и взаимодействует только с фтором при нагревании реагирует с
- 7. Бораны общие формулы BnHn+4 и BnHn+6, анионы BnHn2- имеют 3-хмерные кластерные структуры, в которых КЧ бора
- 8. Бораны номенклатура 2,3-диметил-1-станна-2,3-дикарба-клозо-додекаборан(12) клозо-2,3-(CH3)-1,2,3-SnC2B9H9 тридекагидро-арахно-нонаборат(2-) арахно-[B9H13]2−
- 9. Бораны получение метод Штока метод Шора взаимодействие гидроборатов с б/в ортофосфорной кислотой или иодом в диглиме
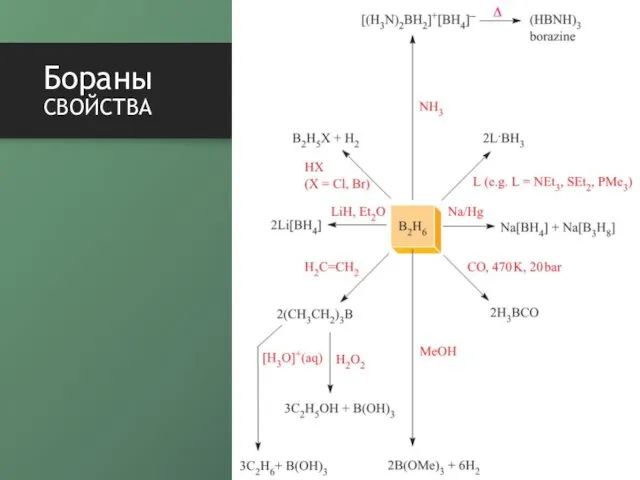
- 10. Бораны свойства
- 11. Галогениды бора делятся на две категории: тригалогениды и субгалогениды наиболее устойчивы мономерные тригалогениды хлор, бром и
- 12. Галогениды бора получение фторирование оксида бора, борной к-ты или буры реакция борной к-ты с фторсульфоновой к-той
- 13. Галогениды бора свойства галогениды реакционноспособны, в большинство реакций вступают в качестве к-т Льюиса образуют комплексы с
- 14. Галогениды бора субгалогениды при соконденсировании паров BCl3 и меди на поверхности, охлаждаемой жидким азотом получается бесцветная
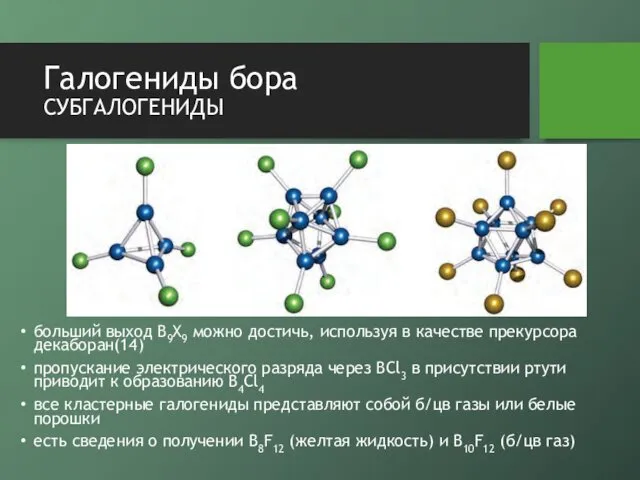
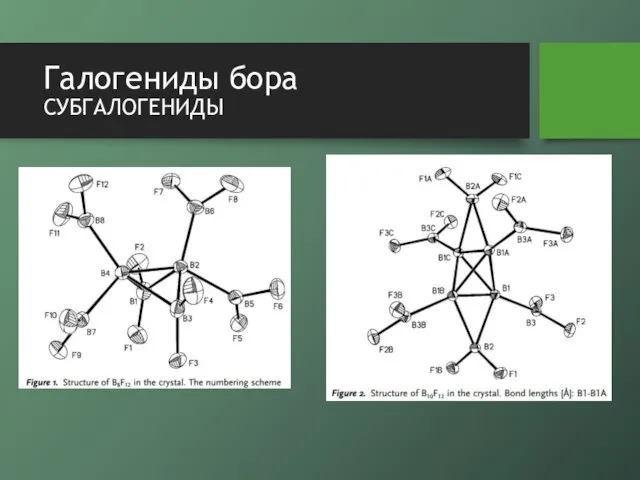
- 15. Галогениды бора субгалогениды больший выход B9X9 можно достичь, используя в качестве прекурсора декаборан(14) пропускание электрического разряда
- 16. Галогениды бора субгалогениды
- 17. Соединения бора с азотом нитриды группа B—N изоэлектронна группе C—C, эл-ть С равна среднему арифм. от
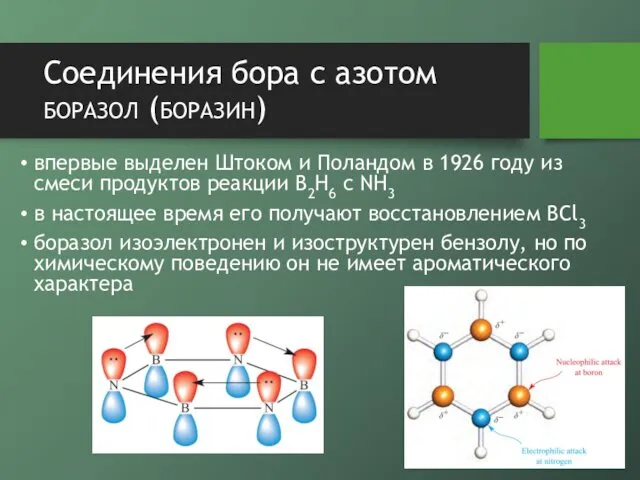
- 18. Соединения бора с азотом боразол (боразин) впервые выделен Штоком и Поландом в 1926 году из смеси
- 19. Соединения бора с азотом боразол
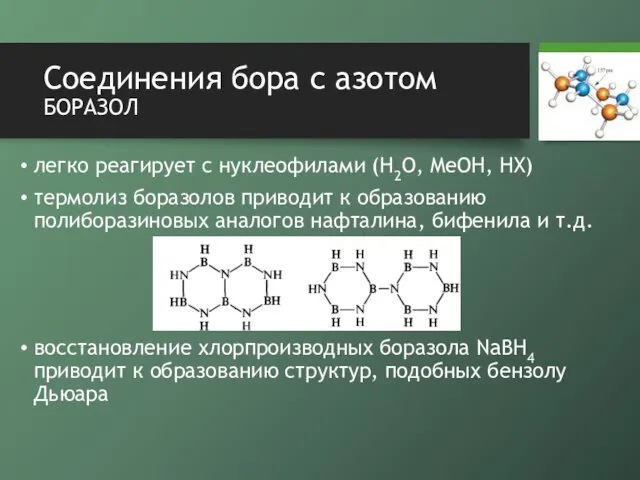
- 20. Соединения бора с азотом боразол легко реагирует с нуклеофилами (H2O, MeOH, HX) термолиз боразолов приводит к
- 21. Соединения бора с азотом боразол 1,3,5-трис(трет-бутил)-2,4,6-трифенил-1λ4,3λ4,5-триазо-2λ4,4λ4,6-триборабицикло[2.2.0]гексен-2
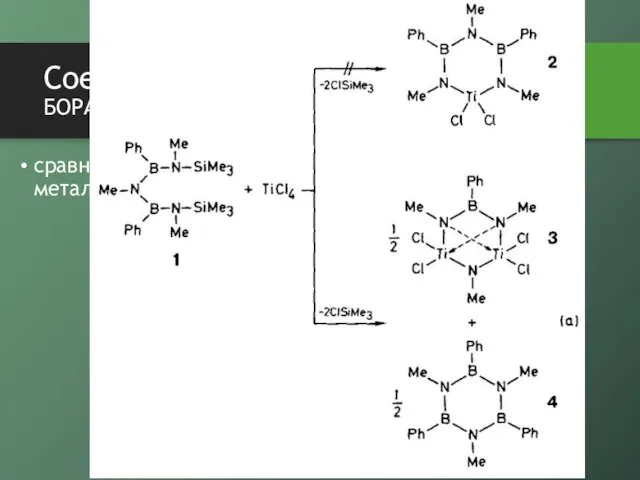
- 22. Соединения бора с азотом боразол сравнительно недавно (1992) получено несколько металлоборазинов
- 23. Оксид бора оксид бора получают осторожной дегидратацией борной к-ты, которую, в свою очередь, получают из буры
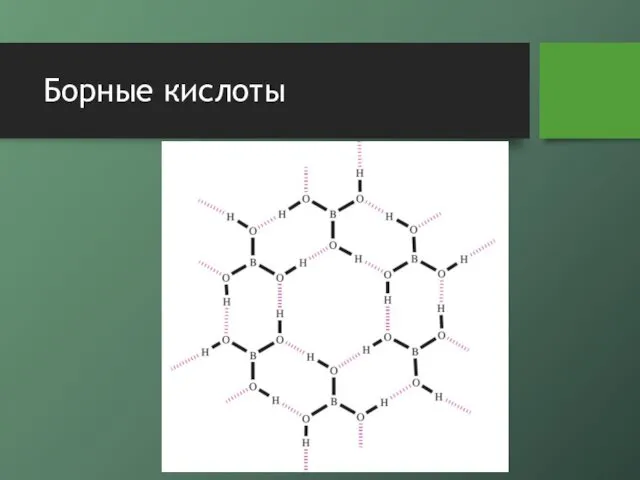
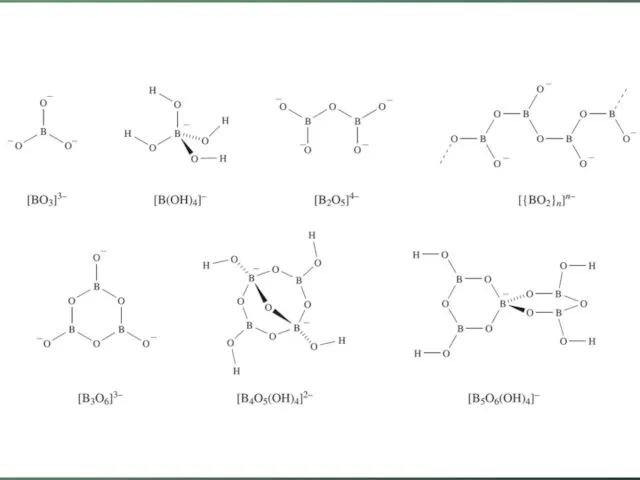
- 24. Борные кислоты метаборная кислота существует в нескольких модификациях, в зависимости от способа получения твердая ортоборная к-та
- 25. Борные кислоты
- 26. Борные кислоты
- 27. Применение
- 29. Скачать презентацию




![Бораны номенклатура 2,3-диметил-1-станна-2,3-дикарба-клозо-додекаборан(12) клозо-2,3-(CH3)-1,2,3-SnC2B9H9 тридекагидро-арахно-нонаборат(2-) арахно-[B9H13]2−](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/479149/slide-7.jpg)







![Соединения бора с азотом боразол 1,3,5-трис(трет-бутил)-2,4,6-трифенил-1λ4,3λ4,5-триазо-2λ4,4λ4,6-триборабицикло[2.2.0]гексен-2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/479149/slide-20.jpg)



 Комплексы хлорида и иодида цинка (II) с карбамидом: синтез, характеристика и биологическая активность
Комплексы хлорида и иодида цинка (II) с карбамидом: синтез, характеристика и биологическая активность Аттестационная работа. Рабочая программа курса внеурочной деятельности «Химия. Мои первые опыты»
Аттестационная работа. Рабочая программа курса внеурочной деятельности «Химия. Мои первые опыты» Презентация по Химии "Д. И. Менделеев и Искусство" - скачать смотреть
Презентация по Химии "Д. И. Менделеев и Искусство" - скачать смотреть  Пропиновые кислоты
Пропиновые кислоты Железо как химический элемент
Железо как химический элемент Коэффициент концентрации меди
Коэффициент концентрации меди Презентация по Химии "Презентация Дисперсия света" - скачать смотреть
Презентация по Химии "Презентация Дисперсия света" - скачать смотреть  Углеводороды: классификация
Углеводороды: классификация Непредельные углероды. Алкены
Непредельные углероды. Алкены Изомерия органических соединений
Изомерия органических соединений Азолы. Гетероциклы с двумя гетероатомами
Азолы. Гетероциклы с двумя гетероатомами Эндогенная серия. Альбитит-грейзеновая группа
Эндогенная серия. Альбитит-грейзеновая группа Углерод и его соединения
Углерод и его соединения Электрохимические процессы
Электрохимические процессы Конструкционные функциональные волокнистые композиты
Конструкционные функциональные волокнистые композиты Презентация по Химии "В мире веществ и реакций" - скачать смотреть
Презентация по Химии "В мире веществ и реакций" - скачать смотреть  Аттестационная работа. Методразработка по проведению исследовательской работы Выращивание кристаллов в домашних условиях
Аттестационная работа. Методразработка по проведению исследовательской работы Выращивание кристаллов в домашних условиях Углеводы
Углеводы Неорганические соединения. Тест
Неорганические соединения. Тест Загальна характеристика галогенів. (Тема 7)
Загальна характеристика галогенів. (Тема 7) Хімічні добавки. Е-числа
Хімічні добавки. Е-числа Поняття про валентність. Ребус
Поняття про валентність. Ребус Химия p-элементов
Химия p-элементов Рафинирование металлических расплавов
Рафинирование металлических расплавов Химическая посуда и лабораторное оборудование
Химическая посуда и лабораторное оборудование Gmp – тиісті өндірістік тәжірибе
Gmp – тиісті өндірістік тәжірибе Производные ненасыщенных полиокси-γ-лактонов
Производные ненасыщенных полиокси-γ-лактонов Клиническая биохимия азотистого обмена. (Лекция 7)
Клиническая биохимия азотистого обмена. (Лекция 7)