Содержание
- 2. Актуальность Сохранение постоянства кислотности жидких сред имеет для жизнедеятельности человеческого организма первостепенное значение Даже небольшие изменения
- 3. Актуальность Кроме того, в медицинской практике часто возникает необходимость в приготовлении буферных растворов, способных поддерживать постоянное
- 4. Цель лекции Рассмотреть теоретические основы протолитического гомеостаза в организме и причины его нарушения Показать теоретические подходы
- 5. План лекции Актуальность темы Понятия и типы буферных растворов, механизм их действия Приготовление буферных растворов Буферная
- 6. ПОНЯТИЕ БУФЕРА БУФЕРНЫЕ РАСТВОРЫ – ЭТО РАСТВОРЫ, рН которых мало меняется при добавлении сильных кислот или
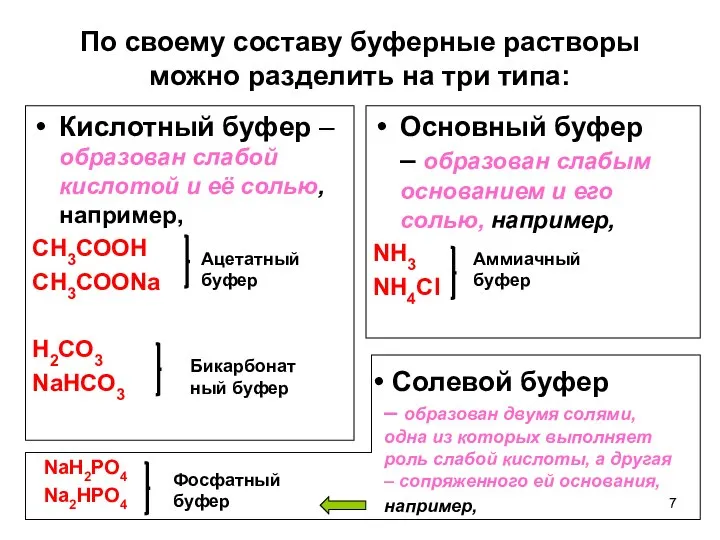
- 7. По своему составу буферные растворы можно разделить на три типа: Кислотный буфер – образован слабой кислотой
- 8. Приготовить такие буферные растворы можно просто путём сливания двух соответствующих растворов. При этом будут совмещаться два
- 9. Благодаря совмещению равновесий ДОБАВЛЕНИЕ РАСТВОРА СОЛИ к буферу не приведет к смещению равновесия реакции диссоциации уксусной
- 10. Понятие буфера (продолжение) Если пренебречь диссоциацией слабой кислоты и гидролизом соли, то буфер будет представлять собой
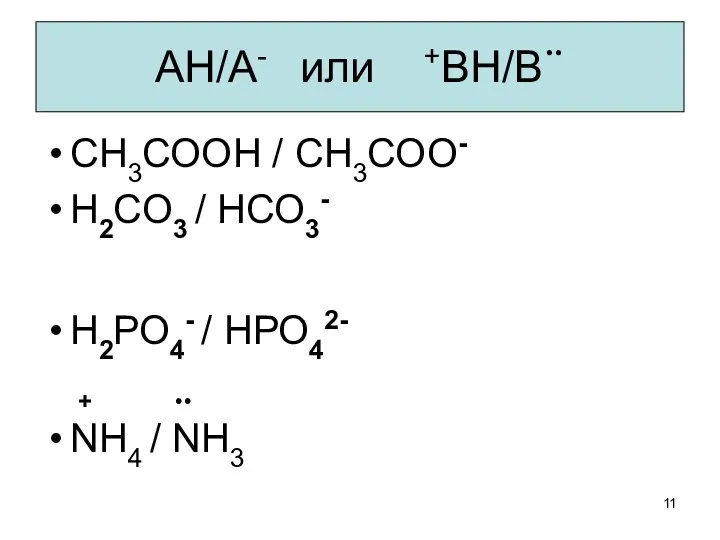
- 11. СН3СООН / СН3СОО- Н2СО3 / НСО3- Н2РО4- / НРО42- NН4 / NН3 АН/А- или +ВН/В¨
- 12. Ограничения, накладываемые на буферную систему: Кислота в ней не должна быть слишком сильной (рКа Кислота в
- 13. рН буфера (уравнение Гендерсона-Гассельбаха) рНб = рКа(к-та/осн.) + ℓg # Это обобщенное уравнение для любого буфера,
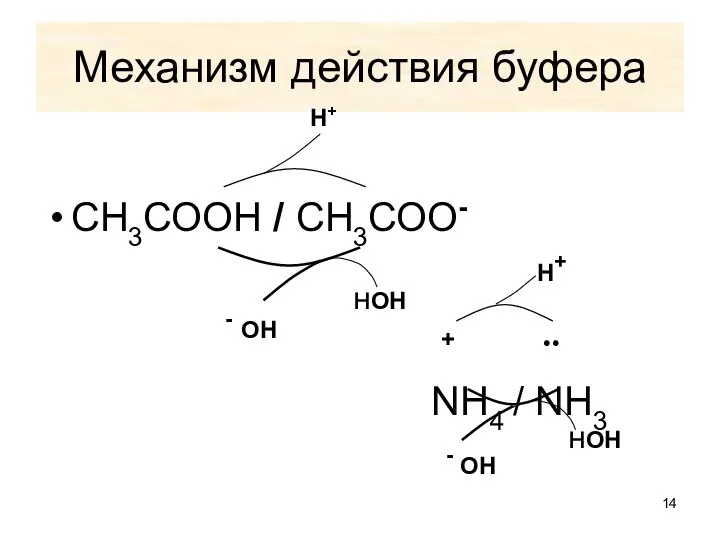
- 14. СН3СООН / СН3СОО- NН4 / NН3 Механизм действия буфера - ОН Н+ - ОН нОН нОН
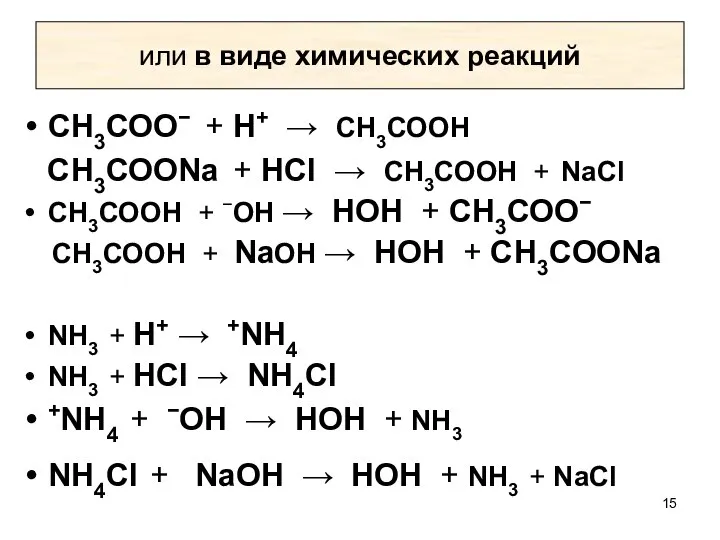
- 15. или в виде химических реакций СН3СОО− + Н+ → СН3СООН СН3СООNa + НCl → СН3СООН +
- 16. Приготовление буферного раствора (по заданному рН) Используется уравнение Гендерсона –Гассельбаха, где равновесные молярные концентрации компонентов буфера
- 17. Отсюда можно вычислить отношение объемов компонентов буфера рН – рКа = ℓg Δ рН Остается научиться
- 18. Как определить объемы компонентов буфера ? Если знаем отношение объемов компонентов и объём всего буфера, то
- 19. Решим задачу Приготовить 50 мл аммиачного буфера с рН 8,8 из растворов двух его компонентов равной
- 20. Можно это вычислять по-другому: аℓg -0,44 =10-0,44=10-1∙100,56=3,6∙10-1 V(NH4) = = 36,76 мл V(NH3) = 50 –
- 21. Буферная емкость Ёмкость по основанию: Ёмкость по кислоте: моль / л моль / л # Указывает
- 22. Для нормальной сыворотки крови Вк =0,029 моль/л или 29 ммоль/л Во =0,012 моль/л или 12 ммоль/л
- 23. Буферные растворы организма Постоянство рН крови (7,36±0,04) обеспечивается буферными системами крови сопряженно с работой легких и
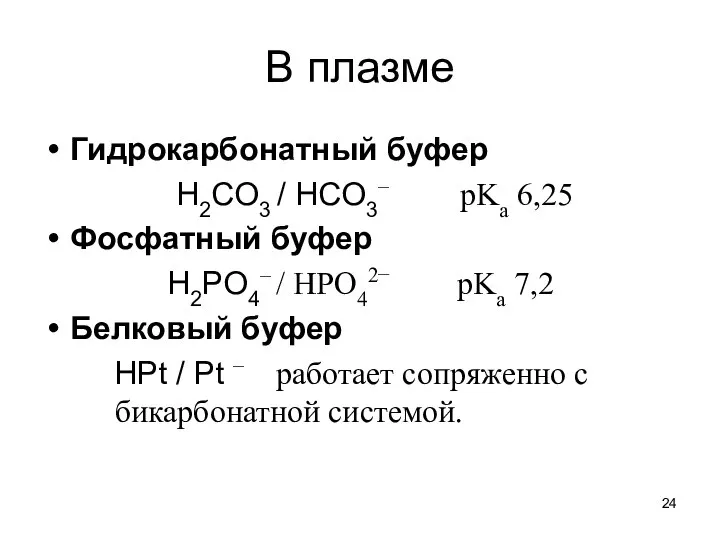
- 24. В плазме Гидрокарбонатный буфер H2CO3 / HCO3– pKa 6,25 Фосфатный буфер H2PO4– / HPO42− pKa 7,2
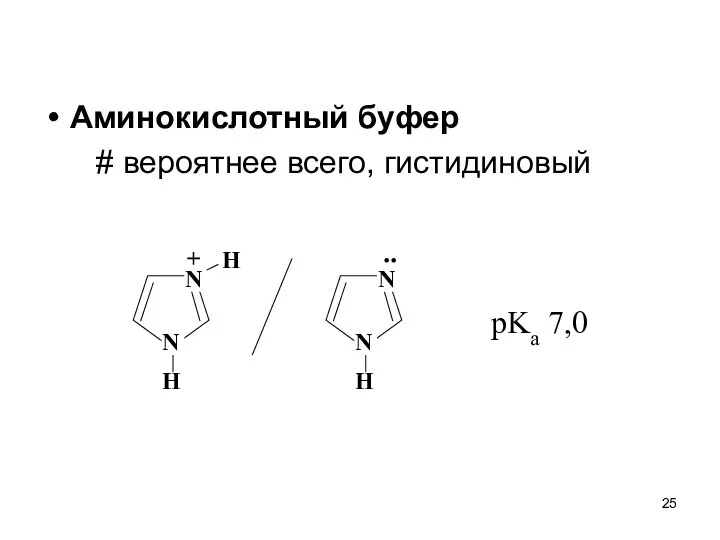
- 25. Аминокислотный буфер # вероятнее всего, гистидиновый N H N H + .. pKa 7,0
- 26. В эритроцитах Гемоглобиновый буфер в двух вариантах: НHb / Hb – рКа 8,2 НHb∙О2 / Hb∙О2
- 27. В эритроцитах Гидрокарбонатный буфер # работает сопряженно с гемоглобиновым Фосфатный буфер (незначительная буферная емкость) # здесь
- 28. В других тканях организма В моче, межклеточной жидкости фосфатная буферная система будет играть более важную роль,
- 29. Гидрокарбонатная буферная система Согласно уравнению Гендерсона-Гассельбаха, рН = рКа(Н2СО3 / НСО3–) + ℓg = = 6,1
- 30. Знание этого уравнения совершенно необходимо для понимания того, как будут развиваться ацидозы и алкалозы. На основе
- 31. 7,4 – 6,1 = ℓg и отсюда = antiℓg 1,3 = 101 ∙ 2 = 20
- 32. Понятно, что емкость по кислоте Вк такой буферной системы будет больше, чем емкость по основанию Во
- 33. Этим же способом можно было показать, что в эритроцитах (где рН 7,2) отношение = 12,6 =
- 34. И таким образом, в венозной крови преобладает кислотная форма гемоглобина НHb, а в артериальной – основная
- 35. Вентиляция легких сдвигает равновесие вправо. Таким образом, легкие помогают удалять протоны Н+ Гидрокарбонатная система – это
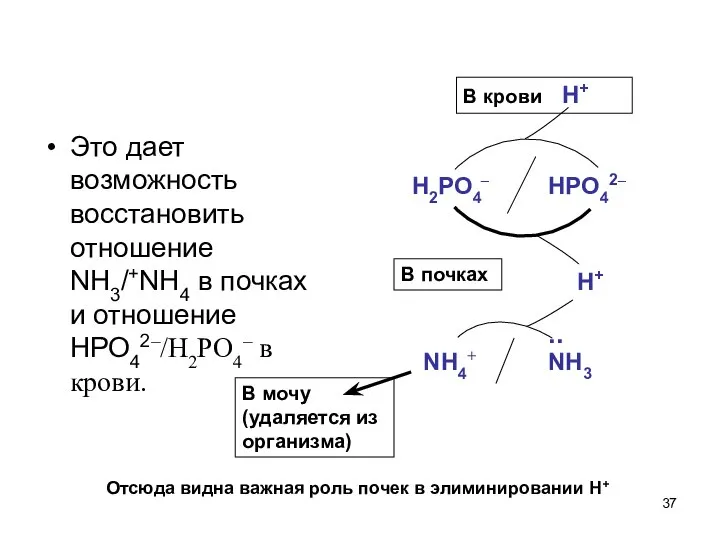
- 36. Работа аммиачной буферной системы в сопряжении с фосфатной в почках В почках есть ферментативные системы, производящие
- 37. Это дает возможность восстановить отношение NH3/+NH4 в почках и отношение НРО42–/Н2РО4– в крови. Отсюда видна важная
- 38. Нарушения кислотно-основного равновесия Изменение рН на 0,2 – 0,3 единицы приводит к серьезным патологическим нарушениям Сдвиг
- 39. Включение буферных систем в компенсацию возникших сдвигов в концентрации Н+ самое быстрое (10 – 15 мин).
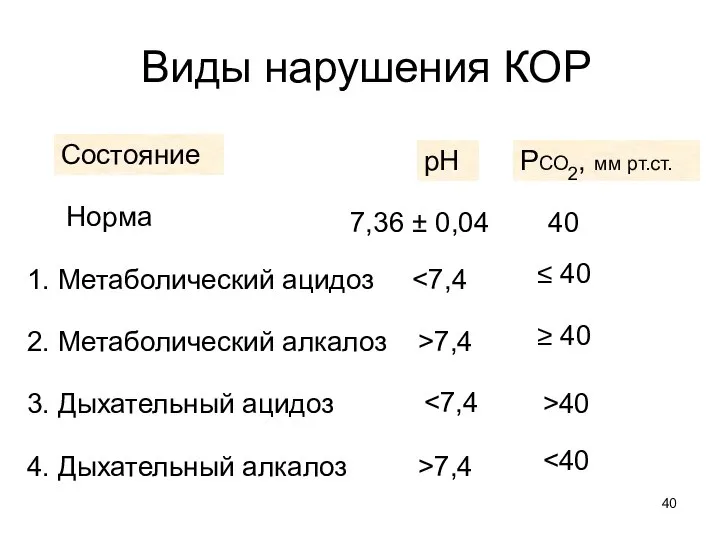
- 40. Виды нарушения КОР Состояние рН РСО2, мм рт.ст. 1. Метаболический ацидоз Норма 7,36 ± 0,04 40
- 41. Метаболический ацидоз Характеризуется относительным избытком нелетучей кислоты H2CO3 или относительным дефицитом НСО3– Причины Нарушение кровообращения, Кислородное
- 42. Метаболический алкалоз Характеризуется удалением молекул кислот или накоплением буферных оснований, включая содержание НСО3– Причины Неукротимая рвота,
- 43. Респираторный (газовый) ацидоз Характеризуется пониженной скоростью вентиляции легких по сравнению со скоростью образования СО2. Причины Заболевания
- 44. Характеризуется повышенной скоростью вентиляции легких по сравнению со скоростью образования метаболического СО2. Причины Вдыхание разреженного воздуха
- 45. Коррекция нарушений КОР Прежде всего выясняются причины: нарушение процессов дыхания (при респираторном ацидозе или алкалозе) или
- 46. При ацидозе в качестве экстренной мере используют в/в вливание 4-8 % растворов гидрокарбоната натрия, но лучше
- 47. Литература Основная: Слесарев В.И. – Химия: Основы химии живого: Учебник для вузов. – 3-е изд., испр.
- 48. Литература Электронные ресурсы: Электронный каталог Крас ГМУ Электронная библиотека по дисциплине химия: общая и неорганическая.-/ гл.
- 50. Скачать презентацию







































 Классификация, свойства и биологическая роль углеводов. (Тема 1)
Классификация, свойства и биологическая роль углеводов. (Тема 1) Классификация минералов
Классификация минералов Структуры в сталях
Структуры в сталях Атомовиты. Анатомо-физиологические свойства
Атомовиты. Анатомо-физиологические свойства Комплексные соединения
Комплексные соединения Металдар дың химиялық қасиеттері. Бейметалдардың химиялық қасиеттері
Металдар дың химиялық қасиеттері. Бейметалдардың химиялық қасиеттері Белки. Аминокислоты
Белки. Аминокислоты Хлор 11 класс - Презентация
Хлор 11 класс - Презентация Деревянова Елена Васильевна – учитель химии МБОУ Мучкапской сош
Деревянова Елена Васильевна – учитель химии МБОУ Мучкапской сош Современные представления о происхождении нефти и газа
Современные представления о происхождении нефти и газа ХИМИЧЕСКИЕ ВЕЩЕСТВА И ОПАСНЫЕ ОБЪЕКТЫ.
ХИМИЧЕСКИЕ ВЕЩЕСТВА И ОПАСНЫЕ ОБЪЕКТЫ. Физические методы исследования в химии
Физические методы исследования в химии Autoionization of water Hydrolysis of salts
Autoionization of water Hydrolysis of salts Химические элементы в быту
Химические элементы в быту Механические свойства минералов
Механические свойства минералов Аттестационная работа. Задачи на смеси и сплавы
Аттестационная работа. Задачи на смеси и сплавы Физические и химические свойства алканов
Физические и химические свойства алканов Презентация по Химии "Алкины" - скачать смотреть бесплатно
Презентация по Химии "Алкины" - скачать смотреть бесплатно Высокомолекулярные вещества
Высокомолекулярные вещества Адсорбционные равновесия. Межмолекулярные взаимодействия при адсорбции
Адсорбционные равновесия. Межмолекулярные взаимодействия при адсорбции IndustrialAlpinism (Средства для мытья фасадов)
IndustrialAlpinism (Средства для мытья фасадов) ЧИСТЫЕ ВЕЩЕСТВА СМЕСИ
ЧИСТЫЕ ВЕЩЕСТВА СМЕСИ Al – металл Подготовили ученицы 10 класса Пилипенко Екатерина Черненко Екатерина
Al – металл Подготовили ученицы 10 класса Пилипенко Екатерина Черненко Екатерина  Применение композиционных угольно-цеолитных адсорбентов для очистки промышленных сточных вод
Применение композиционных угольно-цеолитных адсорбентов для очистки промышленных сточных вод Расчет и построение кривых титрования в методе кислотно-основного титрования
Расчет и построение кривых титрования в методе кислотно-основного титрования Коллоидная химия
Коллоидная химия Ионы. Проверочная работа
Ионы. Проверочная работа Дисперсные системы
Дисперсные системы