Содержание
- 2. Медико-билогическое значение темы
- 3. Медико-билогическое значение темы
- 4. Основные понятия. Классификация Размеры молекул ВМВ в вытянутом состоянии могут достигать 1000 нм. Высокомолекулярные вещества (полимеры)
- 5. Классификация ВМВ Природные Искусственные Синтетические Синтетические (каучук, полиэтилен, синтетические смолы) и искусственные ВМВ получаются в результате
- 6. В качестве исходных веществ для получения полимеров используют низкомолекулярные, ненасыщенные или полифункциональные соединения – мономеры. Методы
- 7. Степенью полимеризации n называется число повторяющихся звеньев в макромолекуле. Любой синтетический полимер состоит из макромолекул разной
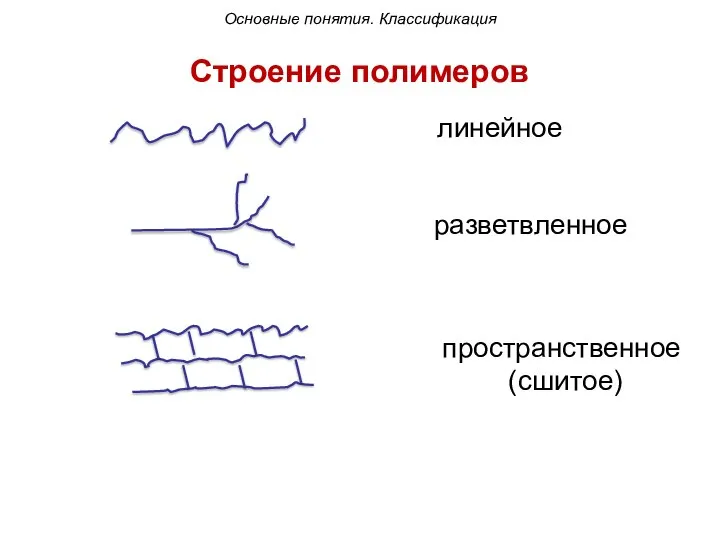
- 8. линейное разветвленное пространственное (сшитое) Строение полимеров Основные понятия. Классификация
- 9. Например, целлюлоза (растительный полисахарид) – имеет линейную структуру, гликоген (животный полисахарид) – имеет разветвленную структуру, фенопласты
- 10. По способности к электролитической диссоциации ВМВ делятся на: неэлектролиты, полиэлектролиты. Полиэлектролиты подразделяются на поликислоты, полиоснования и
- 11. Из-за электрического заряда белки разделяются на фракции при электрофорезе. Это можно использовать в диагностических целях. Основные
- 12. Полимеры имеют две особенности строения молекул: Существование двух типов связи: химические связи (энергия связи порядка десятков
- 13. Гибкость свободно-сочлененной цепи Гибкость реальной цепи Благодаря гибкости макромолекула ВМВ может принимать различные конформации. Основные понятия.
- 14. Конформация – пространственная форма макромолекул, соответствующая максимуму энтропии. Конформации и различные состояния объясняются стремлением к самопроизвольному
- 15. В результате конформационных изменений макромолекулы могут принимать различную форму: линейную, клубка, глобул. глобула статистический клубок стержень
- 16. Низкое сродство к кислороду Высокое сродство к кислороду Конформации гемоглобина Основные понятия. Классификация
- 17. Конформационными переходами можно объяснить многие процессы, происходящие в организме, например, регуляцию активности ферментов. Гибкость молекул ВМВ
- 18. Растворы ВМВ являются лиофильными коллоидными системами. Для них характерны свойства как общие с растворами низкомолекулярных веществ
- 19. I. Растворы ВМВ с истиннымы растворами низкомолекулярных веществ имеют ряд общих свойств: Образуются самопроизвольно. Являются термодинамически
- 20. II. С коллоидными гидрофобными системами растворы ВМВ объединяют: Близкие размеры частиц (d = 10-5-10-7 см). Растворы
- 21. Специфические свойства растворов ВМВ К специфическим свойствам растворов ВМВ относят: набухание, вязкость, осмотическое давление.
- 22. Набухание При набухании молекулы растворителя заполняют пространство между макромолекулами, проникая в петли структур. Набухание – это
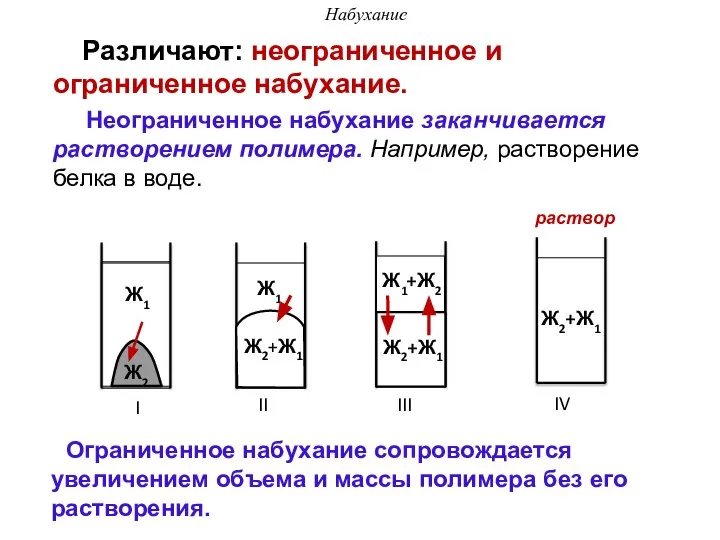
- 23. Различают: неограниченное и ограниченное набухание. Неограниченное набухание заканчивается растворением полимера. Например, растворение белка в воде. Набухание
- 24. Набухание Ограниченное набухание характеризуется степенью набухания (α). Степень набухания показывает отношение приращения объема или массы набухшего
- 25. Набухание На степень набухания влияют: Природа полимера и растворителя. Полярные ВМВ лучше набухают в полярных растворителях
- 26. 2) Температура Процесс набухания осуществляется в 2 стадии: Сольватация молекул полимера. Это экзотермический процесс, ∆H Поэтому
- 27. Набухание 3) Присутствие электролитов. По способности увеличивать степень набухания составлены лиотропные ряды: SCN- > I- >
- 28. Набухание 4) pH среды Наименьшая степень набухания полимера, в частности белков, наблюдается в их изоэлектрической точке.
- 29. ВЯЗКОСТЬ РАСТВОРОВ ВМВ Вязкотекучее состояние
- 30. Вязкотекучее состояние Вязкость
- 31. Вязкость Вязкотекучее состояние
- 32. Вязкость Вязкотекучее состояние
- 33. Вязкотекучее состояние Вязкость
- 34. Вязкость Это обусловлено следующими причинами: 1) Силами сцепления гидрофильных макромолекул ВМВ (белков или полисахаридов) с молекулами
- 35. 2) Образованием ассоциатов при взаимодействии макромолекул между собой. При этом, чем выше концентрация раствора, тем больше
- 36. 3) На аномально-высокую вязкость оказывает влияние форма и гибкость макромолекул полимера. Линейные частицы, особенно если они
- 37. 4) При протекании жидкости через сосуд отдельные части могут перемещаться с различными скоростями (у стенок молекул
- 38. Вязкость Различают вязкость: относительную, удельную, приведенную, характеристическую.
- 39. Относительная вязкость ηотн. – это отношение вязкости раствора к вязкости растворителя. Её определяют экспериментально при помощи
- 40. В широкое колено наливают жидкость, затем заполняют узкое колено, дают вытекать жидкости, при этом по секундомеру
- 41. Удельная вязкость ηуд - относительное приращение вязкости растворителя при введении в него полимера. η – вязкость
- 42. Для линейной формы макромолекул удельную вязкость рассчитывают по уравнению Штаудингера: М (X)– молярная масса полимера [г
- 43. Вязкость
- 44. Приведенная вязкость ηпр – зависимость удельной вязкости от концентрации. Она выражается уравнением Хаггинса: [η] – характеристическая
- 45. Характеристическая вязкость [η] отражает гидродинамическое сопротивление молекул полимера потоку жидкости, выражается эмпирическим уравнением Штаудингера: [η] =
- 46. Осмотическое давление растворов ВМВ Оно невелико: около 0,04 атм, но играет важную роль в биологических процессах.
- 47. Осмотическое давление растворов ВМВ Это учитывает уравнение Галлера, где b-коэффициент, учитывающий гибкость и форму макромолекулы в
- 48. Факторы, влияющие на осмотическое давление ВМВ: Концентрация – с повышением концентрации ВМВ осмотическое давление возрастает. Температура
- 49. Агрегативная устойчивость белков. Высаливание. Денатурация. Коацервация Агрегативная устойчивость – это способность системы сохранять определенную степень дисперсности,
- 50. Агрегативная устойчивость белков Агрегативная устойчивость определяется: наличием дзета-потенциала; плотностью гидратной оболочки. Нарушить агрегативную устойчивость можно: нейтрализацией
- 51. Высаливание При этом используют растворы Na2SO4, (NH4)2SO4, соли магния, фосфаты. Наиболее эффективно высаливание проходит в изоэлектрической
- 52. Ионы солей притягивают молекулы воды, нарушая таким образом гидратную оболочку белка, что уменьшает растворимость белка и
- 53. Если концентрация соли мала, то осаждаются наиболее крупные и тяжелые частицы, обладающие наименьшим зарядом, если концентрация
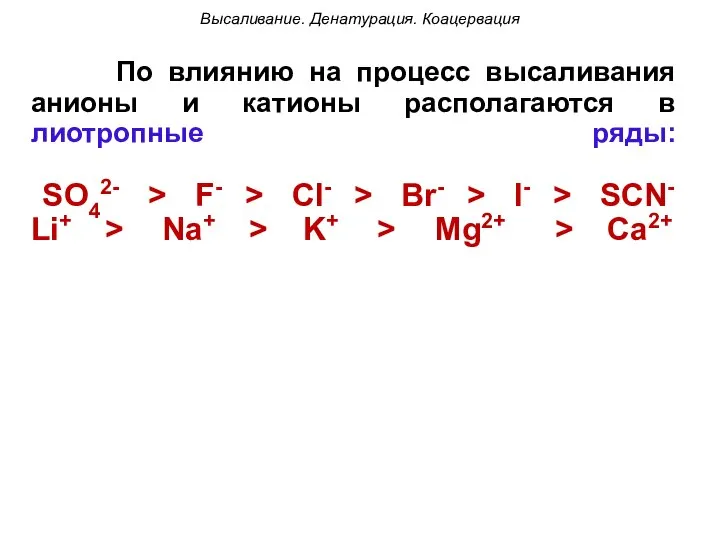
- 54. По влиянию на процесс высаливания анионы и катионы располагаются в лиотропные ряды: SO42- > F- >
- 55. Высаливание белков проводят в мягких условиях при пониженных температурах, без нарушения нативной природы белка, чтобы не
- 56. Денатурация белка – это нарушение первоначальных свойств белка, вызванное изменением пространственной структуры его макромолекулы и сопровождающееся
- 57. Белки в процессе денатурации: теряют гидрофильные свойства, нарушаются форма и размеры макромолекул, увеличивается вязкость растворов, уменьшается
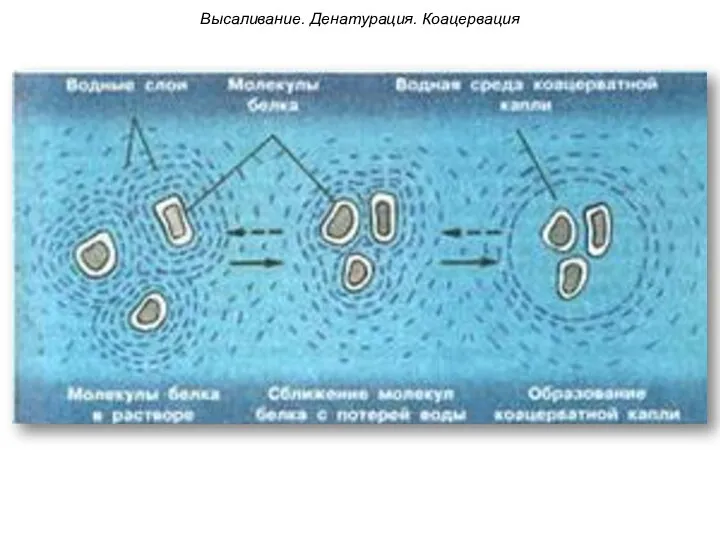
- 58. Высаливание. Денатурация. Коацервация
- 59. Коацервация Коацервация – это аномальное явление в процессе высаливания – слияние водных оболочек нескольких частиц без
- 60. Высаливание. Денатурация. Коацервация
- 61. Высаливание. Денатурация. Коацервация
- 63. Скачать презентацию








































![Характеристическая вязкость [η] отражает гидродинамическое сопротивление молекул полимера потоку жидкости, выражается](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/778668/slide-44.jpg)














 Электролиз воды
Электролиз воды Классификация электродов. (Лекция 4)
Классификация электродов. (Лекция 4) Аминокислоты. Белки. Пептиды
Аминокислоты. Белки. Пептиды ГИДРОЛИЗ СОЛЕЙ 9 класс
ГИДРОЛИЗ СОЛЕЙ 9 класс  Свойство металлов и сплавов
Свойство металлов и сплавов Задания на ЕГЭ
Задания на ЕГЭ Презентация по химии Угарный газ
Презентация по химии Угарный газ  Изучение химической природы кислорода, углекислого газа и гемоглобина
Изучение химической природы кислорода, углекислого газа и гемоглобина Дифузія у побуті
Дифузія у побуті Алканы
Алканы Негізгі топша элементтерінің химиясы
Негізгі топша элементтерінің химиясы Направление окислительно-восстановительного процесса
Направление окислительно-восстановительного процесса Каучук и резиновые материалы
Каучук и резиновые материалы Строение атома
Строение атома Презентация по Химии "Химия – наука о веществах" - скачать смотреть
Презентация по Химии "Химия – наука о веществах" - скачать смотреть  Каучук, резина, латекс
Каучук, резина, латекс Технология производства хлорбензола
Технология производства хлорбензола Презентация Окислительно-восстановительные реакции
Презентация Окислительно-восстановительные реакции Алкалоиды ряда пирролидина, тропана, хинолина, хинукледина. (Лекция 11)
Алкалоиды ряда пирролидина, тропана, хинолина, хинукледина. (Лекция 11) Презентация Коллоидная химия
Презентация Коллоидная химия  Нуклеїнові кислоти
Нуклеїнові кислоти Пестицидтердің жіктелуі
Пестицидтердің жіктелуі Волокнистые наполнители. (Тема 5)
Волокнистые наполнители. (Тема 5) Урок химии на тему: «Типы химических реакций»
Урок химии на тему: «Типы химических реакций»  EdExcel Unit C2 – Discovering Chemistry
EdExcel Unit C2 – Discovering Chemistry Рубидий, цезий, франций
Рубидий, цезий, франций Общая и неорганическая химия
Общая и неорганическая химия Химическая посуда
Химическая посуда