Содержание
- 2. Дисперсные системы – гетерогенные системы с высокой степенью дисперсности (раздробленности) одной из фаз. Признаки: гетерогенность дисперсность
- 3. Классификация ДС по агрегатному состоянию фаз
- 4. Классификация ДС по взаимодействию между частицами Свободнодисперсные - частицы дисперсной фазы свободны, могут перемещаться независимо друг
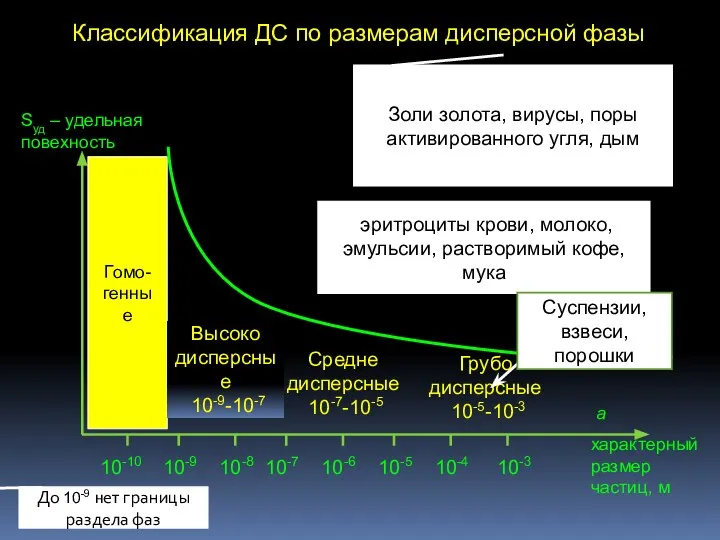
- 5. Классификация ДС по размерам дисперсной фазы 10-9 10-10 10-8 10-7 10-6 10-5 10-4 10-3 a характерный
- 6. Классификация ДС по интенсивности взаимодействия между д. фазой и жидкой д. средой лиофобные лиофильные (золи, эмульсии
- 7. Характерные размеры - размеры дисперсной фазы, которые отражают раздробленность. трехмерные двумерные одномерные порошки нити пленки эмульсии
- 8. Дисперсность D — величина, обратная характерному размеру: размерность м-1. Удельная поверхность Sуд — площадь границы раздела
- 10. различные виды мельниц - помол до 1-10 мкм Механизм диспергирования Под действием деформирующих сил (давление, удар,
- 11. (для твердых тел и жидкостей) Кавитации -локальные быстро чередующиеся сжатия и расширения вещества, приводящие к образованию
- 12. Ультразвуковое диспергирование твердого тела
- 13. Ультразвуковой ингалятор Ультразвуковое диспергирование жидкости
- 14. Методы конденсации – образование новой фазы из отдельных атомов или молекул Метод замены растворителя Конденсация из
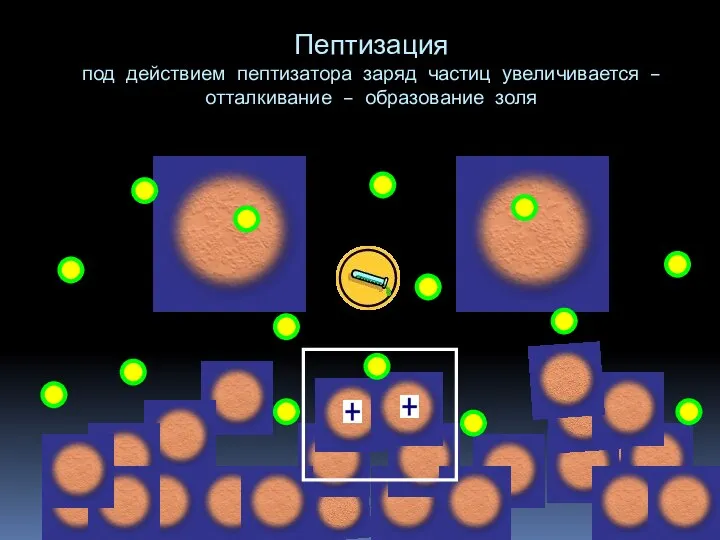
- 15. Пептизация — процесс перехода вещества из геля(осадка) в золь под влиянием диспергирующих веществ (пептизаторов). При пептизации
- 16. Пептизация под действием пептизатора заряд частиц увеличивается – отталкивание – образование золя
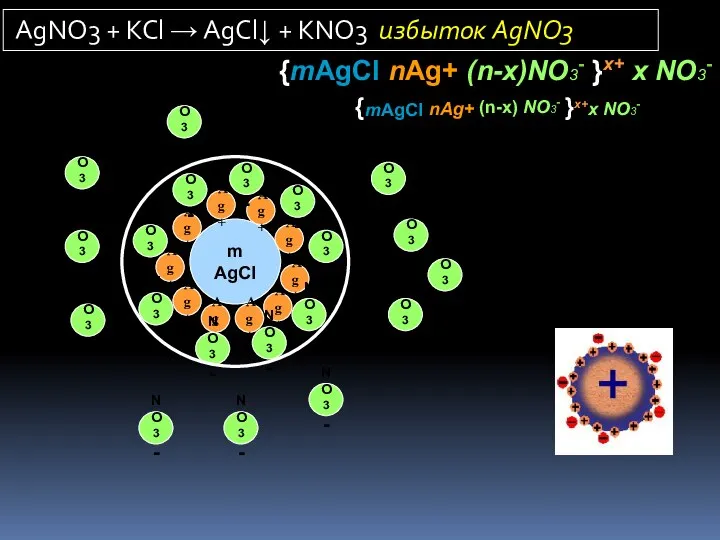
- 17. Золи - лиофобные высокодисперсные системы Т/Ж. как правило, получают методом химической конденсации. Реакции обмена, восстановления, окисления,
- 18. m AgCl Ag+ Ag+ Ag+ Ag+ Ag+ Ag+ Ag+ Ag+ Ag+ Ag+ NO3- NO3- NO3- NO3-
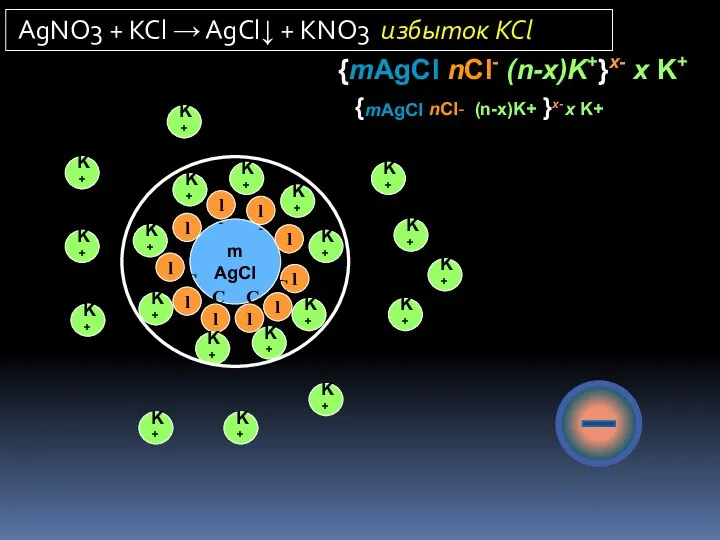
- 19. m AgCl Cl- Cl- Cl- Cl- Cl- Cl- Cl- Cl- Cl- Cl- K+ K+ K+ K+
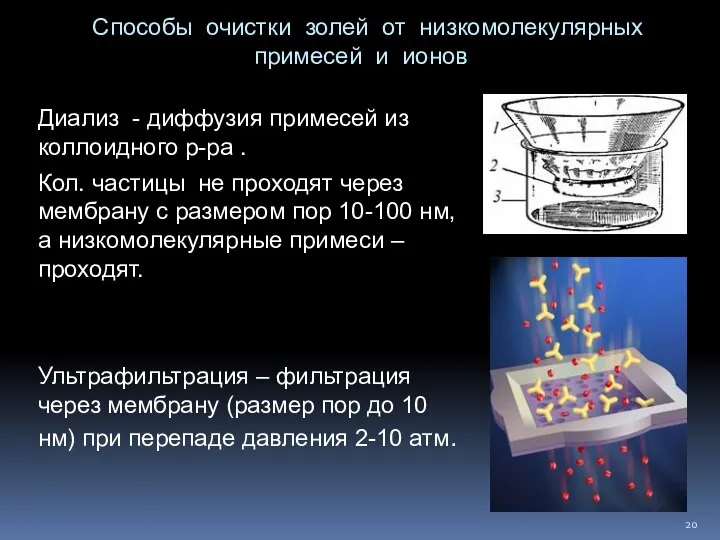
- 20. Способы очистки золей от низкомолекулярных примесей и ионов Диализ - диффузия примесей из коллоидного р-ра .
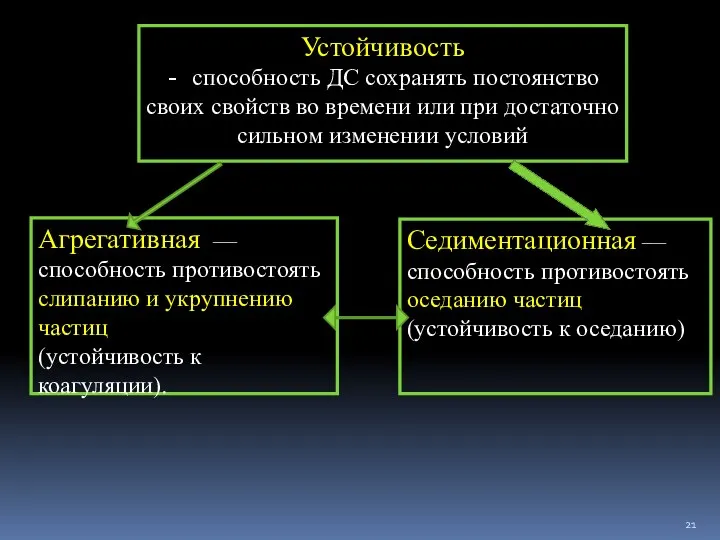
- 21. Устойчивость - способность ДС сохранять постоянство своих свойств во времени или при достаточно сильном изменении условий
- 22. h расстояние между частицами Е от Е пр Суммарная Е «Ближний минимум» «Дальний минимум» «Энергетический (потенциальный)
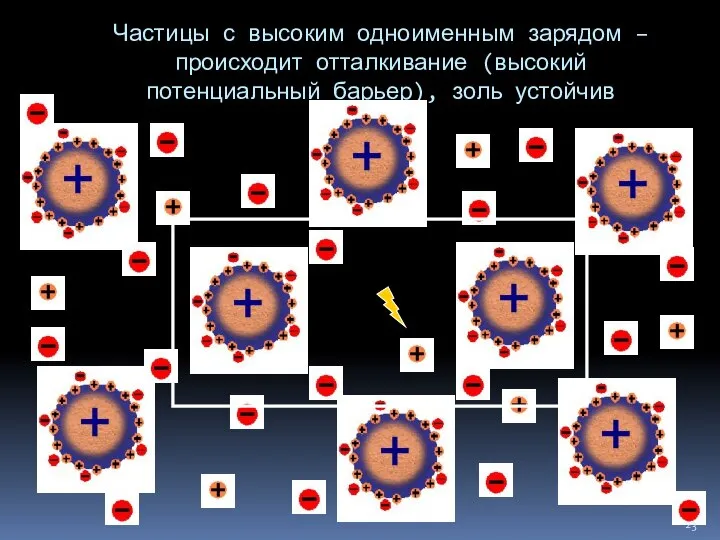
- 23. Частицы с высоким одноименным зарядом – происходит отталкивание (высокий потенциальный барьер), золь устойчив
- 24. Коагуляция - самопроизвольное укрупнение частиц твердой дисперсной фазы в золях (чаще - под действием электролита). Порог
- 25. Добавление электролита – заряд частиц уменьшается, потенциальный барьер становится ниже, частицы сближаются
- 26. Частицы притягиваются - КОАГУЛЯЦИЯ
- 27. (изоэлектрическое состояние: {mAgI ∙nI – ∙ nK+}. Li+, Na+, K+, Rb+, Cs+, F–, Сl–, Вr–, NO3–,
- 28. 3. Коагуляция золей электролитами, содержащими многозарядный ион может произойти перезарядка золя {mAg · n I– ·(n
- 29. Правило Шульце — Гарди: коагулирующая способность иона тем больше, чем больше его заряд: Ск1: Ск2 :Ск3
- 30. Гетерокоагуляция – взаимодействие частиц, различных по заряду и величине. Взаимная коагуляция происходит при смешивании золей с
- 32. Скачать презентацию






















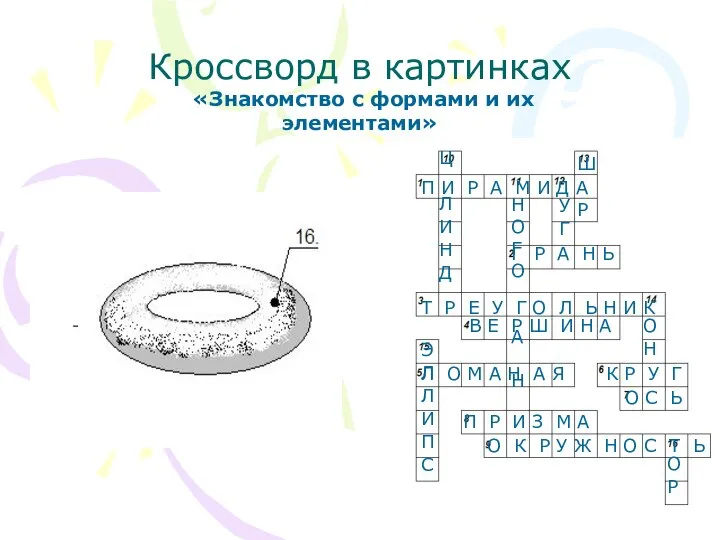 Кроссворд в картинках. Знакомство с формами и их элементами
Кроссворд в картинках. Знакомство с формами и их элементами Презентация к уроку по теме: «Алканы» Учитель химии Колесникова Г.Т.
Презентация к уроку по теме: «Алканы» Учитель химии Колесникова Г.Т. IVA группа С, Si, Ge, Sn, Pb (подгруппа титана)
IVA группа С, Si, Ge, Sn, Pb (подгруппа титана) Зависимость свойств веществ от их строения. Химическая связь. Основные виды химической связи
Зависимость свойств веществ от их строения. Химическая связь. Основные виды химической связи Определение химического состава почвы пришкольного участка
Определение химического состава почвы пришкольного участка Илік заттар. Тітіркендіруші заттар. Қапталғыш заттар, адсорбциялаушы заттар
Илік заттар. Тітіркендіруші заттар. Қапталғыш заттар, адсорбциялаушы заттар Алкены. Пропилен
Алкены. Пропилен Каталіз: каталітичне гідрування
Каталіз: каталітичне гідрування Класифікація, будова та номенклатура органічних сполук
Класифікація, будова та номенклатура органічних сполук Газификация тяжёлых нефтяных остатков. Конверсия природного газа
Газификация тяжёлых нефтяных остатков. Конверсия природного газа Основы химической термодинамики
Основы химической термодинамики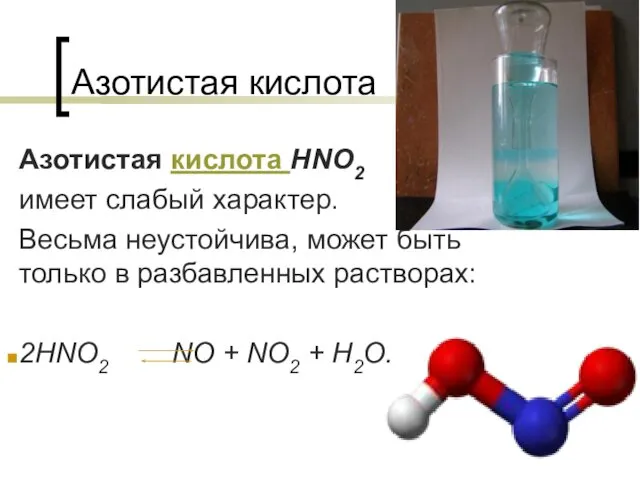 Азотистая кислота
Азотистая кислота Кислоты, основания, соли в свете ТЭД подготовила: Мартынова Е.Ю._
Кислоты, основания, соли в свете ТЭД подготовила: Мартынова Е.Ю._ Непредельные углеводороды: этилен
Непредельные углеводороды: этилен Понятие об адсорбционной влаге
Понятие об адсорбционной влаге Пиримидин (шестичленный гетероцикл с двумя атомами азота)
Пиримидин (шестичленный гетероцикл с двумя атомами азота) Викторина на тему: «Щелочные и щелочноземельные металлы в гомеопатии»
Викторина на тему: «Щелочные и щелочноземельные металлы в гомеопатии» Коллоидная химия
Коллоидная химия Изоморфизм, изоморфизмнің түрлері. Полиморфизм. Сульфидтер класының жалпы сипаттамасы
Изоморфизм, изоморфизмнің түрлері. Полиморфизм. Сульфидтер класының жалпы сипаттамасы Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки
Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки Полимеры и их использование
Полимеры и их использование Важнейшие минералы
Важнейшие минералы Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химическая кинетика
Химическая кинетика Презентация по Химии "Изотопы" - скачать смотреть
Презентация по Химии "Изотопы" - скачать смотреть  Презентация по Химии "Д.И. Менделеев – основоположник русской агрохимии" - скачать смотреть
Презентация по Химии "Д.И. Менделеев – основоположник русской агрохимии" - скачать смотреть  Кристалічні та аморфні тіла. Рідкі кристали та їх властивості. Підготувала учениця 10 класу Стрельчук Катерина
Кристалічні та аморфні тіла. Рідкі кристали та їх властивості. Підготувала учениця 10 класу Стрельчук Катерина  Полипропилен
Полипропилен