Единый государственный экзамен по ХИМИИ (консультация 2) О.П. Костенко, проректор ГОУ РК «ИПК РО» по НМР
Содержание
- 2. ТЕМЫ: Современные представления о строении атомов Закономерности изменения химических свойств элементов и их соединений по периодам
- 3. Строение атома Задание А1: число нейтронов в ядре атома изотопа углерода с относительной атомной массой равной
- 4. Строение атома Атом (от греч. atomos - неделимый) - наименьшая химическая частица, состоящая из массивного положительно
- 5. Атомные частицы и их свойства Атом состоит из трёх видов частиц: Электрон - (е) - заряд
- 6. Строение атома Ядро атома - образование из протонов и нейтронов, находящееся в центральной части атома. Содержит
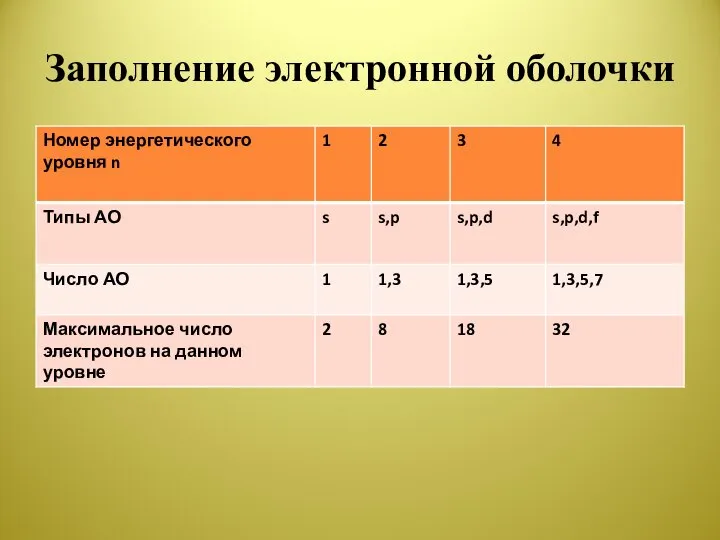
- 7. Заполнение электронной оболочки
- 8. Строение атома Задание А1: число нейтронов в ядре атома изотопа углерода с относительной атомной массой равной
- 9. Строение атома Ядро любого химического элемента состоит из нуклонов. 2. Относительная масса одного нуклона равна 1
- 10. Строение атома Составьте электронную формулу химического элемента № 17
- 11. Строение атома 1. Элемент № 17 называется хлор и имеет химический символ Cl. 2. Элемент хлор
- 12. Строение атома 11. На втором энергетическом уровне атома хлора находится 8 электронов. 17 - (2 +
- 13. Строение атома 18. На третьем энергетическом уровне в атоме хлора имеется три подуровня s, р, d.
- 14. Строение атома электронная формула иона Br- 1)… 2)…. 3)… 4)…
- 15. Строение атома электронная формула атома брома Br0 1s22s22p63s23p63d104s24p5 атома брома Br0 превращается в ион брома Br
- 16. Строение атома Атом металла имеет электронную конфигурацию 1s2 2s2 2p6 3s2, формула оксида, гидроксида и сульфата
- 17. Строение атома 1s2 2s2 2p6 3s2 Э+2 1)Э+2О-2; Э+2 (ОН)-2;Э+2SO4-2
- 18. ХИМИЧЕСКАЯ СВЯЗЬ Задание :Укажите соединение с ионной связью 1) CaCl2; 2)SO2; 3)Br2 4)H2O
- 19. Окислительно-восстановительные процессы Используя метод электронного баланса, составьте уравнение реакции: Cr2O3 + … + KOH → KNO2+
- 20. Окислительно-восстановительные процессы Cr2O3 + KNO3+ KOH → KNO2+ K2CrO4 + H2O
- 21. Окислительно-восстановительные процессы 1) Составлен электронный баланс: N+5 + 2ē → N+3 3 2Cr+3– 6ē → 2Cr+6
- 23. Скачать презентацию



















 Производство водорода
Производство водорода Хімічні добавки. Е-числа
Хімічні добавки. Е-числа Получение водорода в промышленности и его применение Химия 8 класс
Получение водорода в промышленности и его применение Химия 8 класс Экспертиза шоколада
Экспертиза шоколада Электролиз растворов электролитов урок по химии в 10 классе
Электролиз растворов электролитов урок по химии в 10 классе  Побочная подгруппа VI группы периодической системы
Побочная подгруппа VI группы периодической системы Серная кислота Михалева Татьяна Сергеевна Учитель химии БОУ г. Омска СОШ №61 2014
Серная кислота Михалева Татьяна Сергеевна Учитель химии БОУ г. Омска СОШ №61 2014  Методы разделения белковых смесей. Электрофорез
Методы разделения белковых смесей. Электрофорез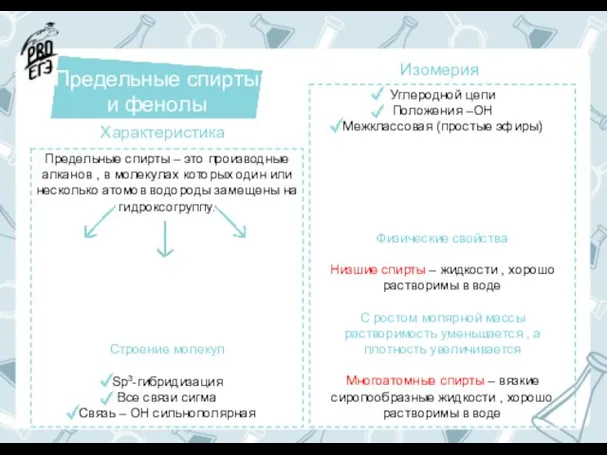 Предельные спирты и фенолы
Предельные спирты и фенолы Причина отказа повреждений технологического оборудования и принятия мер по их устранению установки производства газовой серы
Причина отказа повреждений технологического оборудования и принятия мер по их устранению установки производства газовой серы Структура електронної оболонки атома
Структура електронної оболонки атома Химический состав молока
Химический состав молока Любимый Алюминий
Любимый Алюминий Атомы и молекулы. Простые и сложные вещества. 8 класс
Атомы и молекулы. Простые и сложные вещества. 8 класс Использование уксусной кислоты в жизни
Использование уксусной кислоты в жизни Алкиндер. Номенклатурасы, табиғатта кездесуі, физикалық және химиялық қасиеттері, алыну жолдары
Алкиндер. Номенклатурасы, табиғатта кездесуі, физикалық және химиялық қасиеттері, алыну жолдары Презентация по Химии "Вода для жизни!" - скачать смотреть бесплатно
Презентация по Химии "Вода для жизни!" - скачать смотреть бесплатно Стекло и его разновидности
Стекло и его разновидности Водные свойства и водный режим почв
Водные свойства и водный режим почв Стан, роль і місце органічної хімії в сучасній хімічній освіті.
Стан, роль і місце органічної хімії в сучасній хімічній освіті.  Электролиз. Электролиз хлорида натрия
Электролиз. Электролиз хлорида натрия Методы трансформации карбоновых кислот и их производных
Методы трансформации карбоновых кислот и их производных Цветные металлы и сплавы
Цветные металлы и сплавы Задачи к экзамену по дисциплине «ИПР и ОП»
Задачи к экзамену по дисциплине «ИПР и ОП» Периодическая Система Д. И. Менделеева в свете учения о строении атома
Периодическая Система Д. И. Менделеева в свете учения о строении атома ОСНОВНЫЕ ПОНЯТИЯ ХИМИИ 1 полугодие 8 класс Л.И.Настина, учитель химии
ОСНОВНЫЕ ПОНЯТИЯ ХИМИИ 1 полугодие 8 класс Л.И.Настина, учитель химии  Полимеры. Функции полимеров
Полимеры. Функции полимеров Презентация по Химии "Алкены" - скачать смотреть бесплатно__
Презентация по Химии "Алкены" - скачать смотреть бесплатно__