Содержание
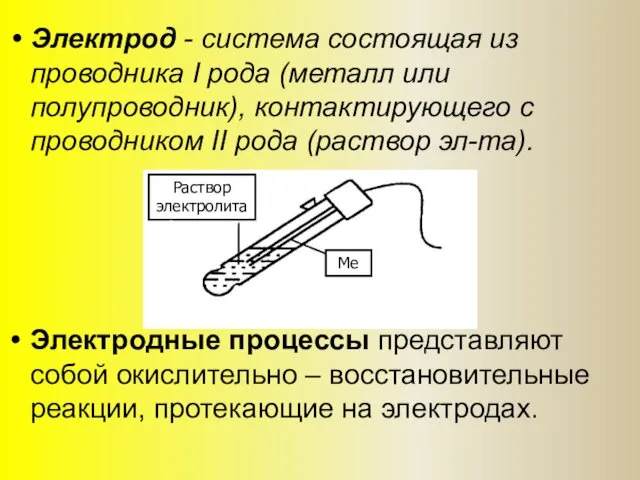
- 2. Электрод - система состоящая из проводника I рода (металл или полупроводник), контактирующего с проводником II рода
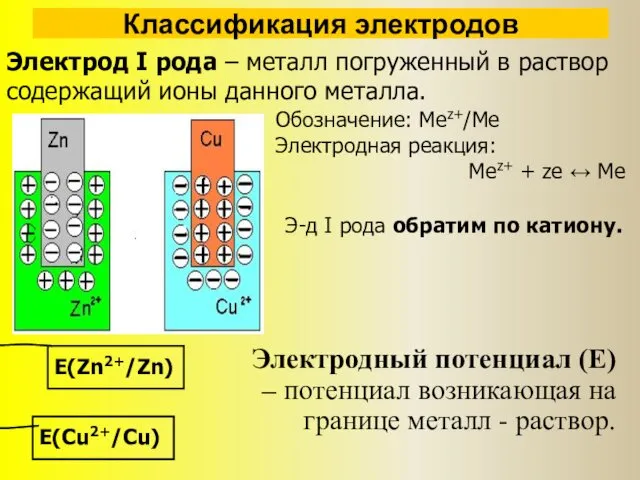
- 3. Классификация электродов Электрод I рода – металл погруженный в раствор содержащий ионы данного металла. Обозначение: Меz+/Ме
- 4. Рассчитывается по уравнению Нернста: Электродный потенциал (E) зависит от температуры, природы металла и концентрации его ионов
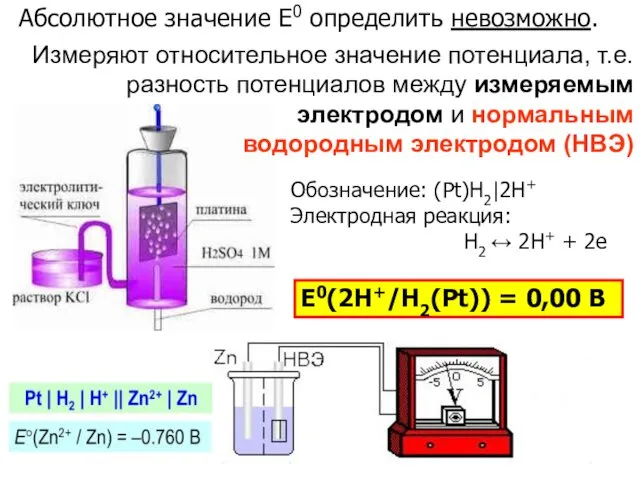
- 5. Е0(2Н+/Н2(Pt)) = 0,00 В Абсолютное значение E0 определить невозможно. Обозначение: (Pt)H2|2H+ Электродная реакция: H2 ↔ 2H+
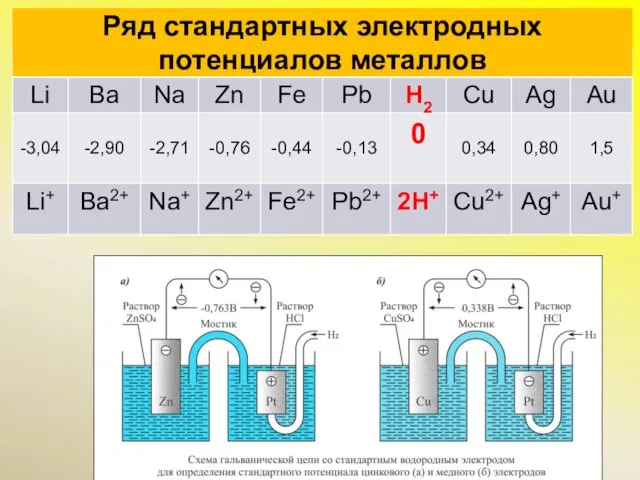
- 6. Ряд стандартных электродных потенциалов металлов
- 7. Электрод второго рода – металл покрытый труднорастворимой солью этого металла и погруженный в раствор содержащий анионы
- 8. Пример: Стеклянный электрод Ионоселективный (мембранный) электрод Обозначение: Н+ |стекло |HCl (0,1М)|AgCl,Ag или при 250С (298К)
- 9. Электрохимические цепи, способные вырабатывать электрическую энергию, называют гальваническими элементами.
- 11. Элемент Даниэля – Якоби схематически может быть изображен следующим образом: (Анод) Zn │ZnSO4 CuSO4│Cu (Катод). φ1
- 12. Электродвижущая сила (ЭДС) гальванического элемента равна алгебраической сумме скачков потенциала: ∆Е = φ1 + φ2 +
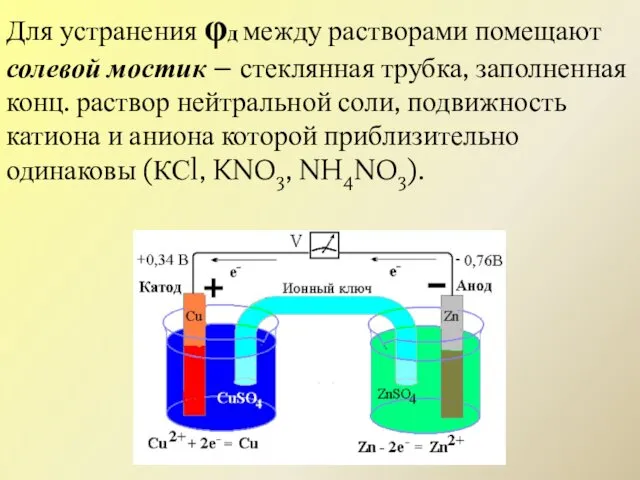
- 13. Для устранения φд между растворами помещают солевой мостик – стеклянная трубка, заполненная конц. раствор нейтральной соли,
- 14. Если диффузионный потенциал устранен, между растворами ставится двойная черта: (Анод) Zn│ZnSO4 ║ CuSO4│Cu (Катод) ЭДС этого
- 15. 1. Химические цепи Пример: Zn⎪ZnSO4 ⎪⎪ CuSO4⎪Cu 2. Концентрационные Пример: Ag⎪AgNO3 ⎪⎪ AgNO3⎪Ag а1 ЭДС такой
- 17. Скачать презентацию









 Окислительновосстановительные реакции ─ ОВР
Окислительновосстановительные реакции ─ ОВР Ионообменная хроматография
Ионообменная хроматография Получение и собирание газов
Получение и собирание газов Эколого-химическая характеристика качества почвы
Эколого-химическая характеристика качества почвы Аттестацианная работа. Основы исследовательской деятельности по химии
Аттестацианная работа. Основы исследовательской деятельности по химии Типы первичных химических источников тока
Типы первичных химических источников тока Свойства жидкостей
Свойства жидкостей Кислоты и основания
Кислоты и основания Epoxy-Based Fibre Reinforced Nanocomposites
Epoxy-Based Fibre Reinforced Nanocomposites Использование инновационных технологий в обучении химии как средство повышения качества подготовки специалистов. Методи
Использование инновационных технологий в обучении химии как средство повышения качества подготовки специалистов. Методи Растворы. Способы выражения концентраций. Сильные и слабые электролиты. Закон разведения Оствальда
Растворы. Способы выражения концентраций. Сильные и слабые электролиты. Закон разведения Оствальда Классификация химических элементов. Периодический закон Дмитрия Ивановича Менделеева
Классификация химических элементов. Периодический закон Дмитрия Ивановича Менделеева Природные смолы: мирра, ладан и шеллак
Природные смолы: мирра, ладан и шеллак Методы исследования химического состава нефти и продуктов ее переработки
Методы исследования химического состава нефти и продуктов ее переработки Внутренняя среда организма. Система крови. Физико-химические свойства крови
Внутренняя среда организма. Система крови. Физико-химические свойства крови Курсовая работа. Синтез адипиновой кислоты
Курсовая работа. Синтез адипиновой кислоты Универсальные пути катаболизма аминокислот. (Лекция 2)
Универсальные пути катаболизма аминокислот. (Лекция 2) Основные классы неорганических соединений
Основные классы неорганических соединений Решаем задачи «Домашняя аптечка» Карпухина Ирина Степановна Учитель химии МБОУ СОШ № 32 Город Новосибирск
Решаем задачи «Домашняя аптечка» Карпухина Ирина Степановна Учитель химии МБОУ СОШ № 32 Город Новосибирск Пластмассы (пластики)
Пластмассы (пластики) Типы химических реакций
Типы химических реакций Основные диагностические признаки рубина и его имитаций
Основные диагностические признаки рубина и его имитаций Мило. Мийні засоби
Мило. Мийні засоби  Презентация по Химии "Белки." - скачать смотреть бесплатно
Презентация по Химии "Белки." - скачать смотреть бесплатно Металлические элементы группы IA. ЛИТИЙ. Работу выполнила: Ученица 11 класса Иванова Ксения
Металлические элементы группы IA. ЛИТИЙ. Работу выполнила: Ученица 11 класса Иванова Ксения Гетероорганические углеводороды нефти и асфальто-смолистые вещества
Гетероорганические углеводороды нефти и асфальто-смолистые вещества Метаморфические горные породы
Метаморфические горные породы Polivinilpirrolidon-limon turşusunun Na duzu-su ikifazalı sisteminin fizikikimyəvi xassələri
Polivinilpirrolidon-limon turşusunun Na duzu-su ikifazalı sisteminin fizikikimyəvi xassələri