Содержание
- 2. 1. Адсорбция сильных электролитов из водных растворов твердым адсорбентом получила название ионной. Ионная адсорбция более сложное
- 3. Особенности ионной адсорбции: адсорбируются ионы, а не молекулы; адсорбция протекает только на полярных адсорбентах, поэтому ее
- 4. Избирательная адсорбция - это процесс фиксации на твердой поверхности ионов одного знака (потенциалообразующий слой ионов) при
- 5. Избирательный характер адсорбции описывается следующими правилами: I. Правилом Панета-Фаянса: на поверхности кристалла преимущественно адсорбируются те ионы,
- 6. II. Правило изоморфизма: На полярном адсорбенте из раствора электролита адсорбируются ионы, близкие по строению и размерам
- 7. III. Если ионы-адсорбаты имеют одинаковые по знаку и разные по величине степени окисления, то в первую
- 8. IV. Если ионы-адсорбаты имеют одинаковые по величине и знаку степени окисления, то в первую очередь адсорбируются
- 9. Закономерности избирательной адсорбции можно проиллюстрировать на примере образования трудно растворимых соединений. KI + AgN03 → AgI↓+
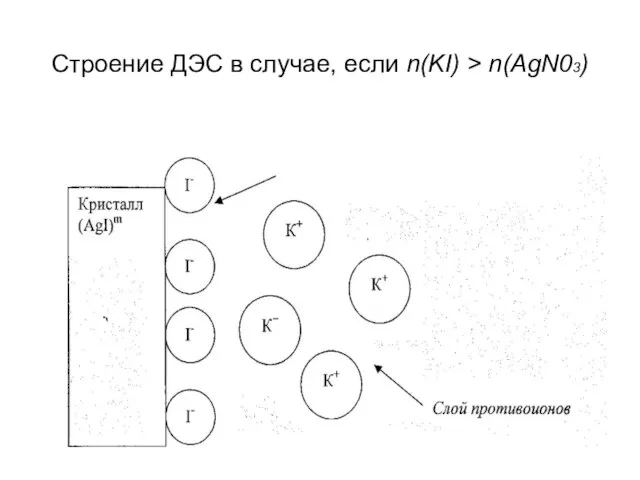
- 10. Строение ДЭС в случае, если n(KI) > n(AgN03)
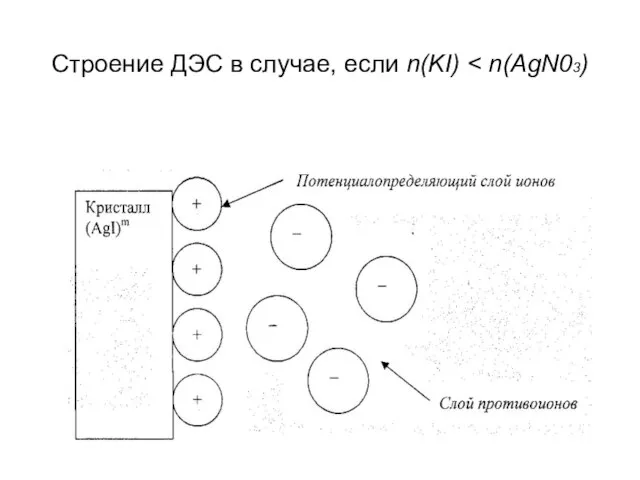
- 11. Строение ДЭС в случае, если n(KI)
- 12. Исключения из правила Панета-Фаянса: крупные ионы с жесткой электронной структурой: Сг042-, С2042- и др. Такие ионы
- 13. Факторы, влияющие на избирательную адсорбцию: Природа адсорбента. Чем более полярным является адсорбент, тем лучше адсорбируются ионы
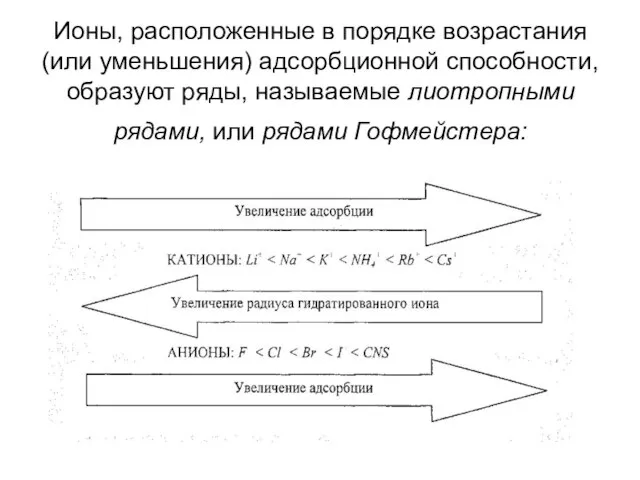
- 14. Ионы, расположенные в порядке возрастания (или уменьшения) адсорбционной способности, образуют ряды, называемые лиотропными рядами, или рядами
- 15. Различают необратимую и обратимую электролитную адсорбцию. При необратимой адсорбции адсорбат и адсорбент образуют нерастворимое химическое соединение.
- 16. 2. Ионообменная адсорбция - это процесс, при котором твердый адсорбент (ионит) обменивает эквивалентное количество своих ионов
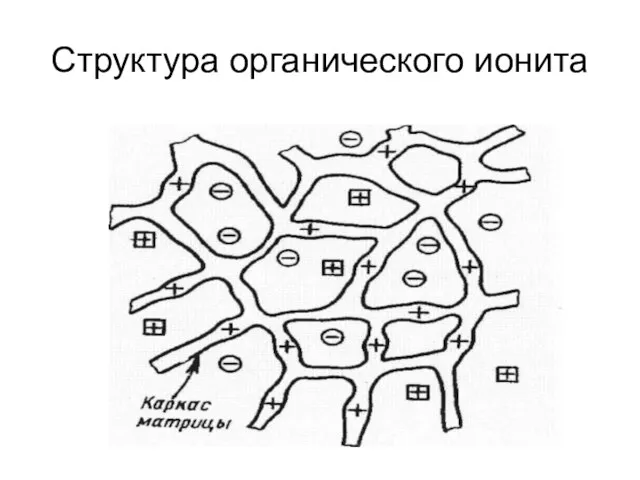
- 17. Адсорбенты, способные к обмену ионов, называют ионитами или ионообменниками. Иониты имеют структуру в виде каркаса, «сшитого»,
- 18. Структура органического ионита
- 19. Классификация ионитов: По происхождению: природные (кристаллические силикаты, апатиты, гуминовые кислоты) и синтетические (в качестве каркаса используют
- 20. Каркас любого ионита, называемый матрица (R), не участвует в ионообменной адсорбции. На нём закреплены либо ионы
- 21. Ионный обмен представляет собой обратимое стехиометрическое замещение подвижного иона, связанного с ионогенной группой ионита на другой
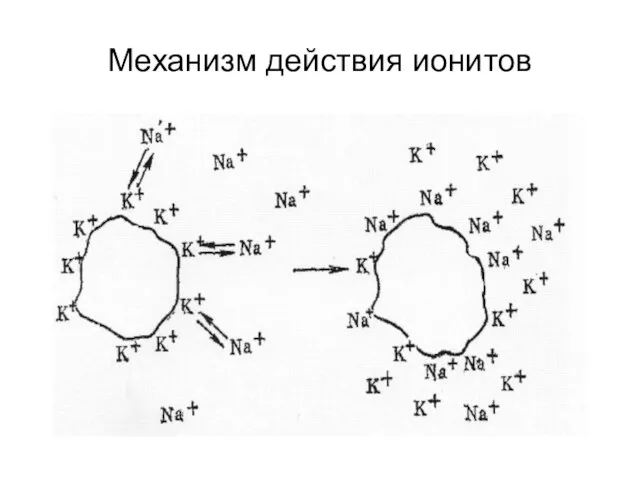
- 22. Механизм действия ионитов
- 23. Катиониты - представляют собой нерастворимые многоосновные кислоты; они высвобождают и обменивают катионы. Катиониты могут находиться либо
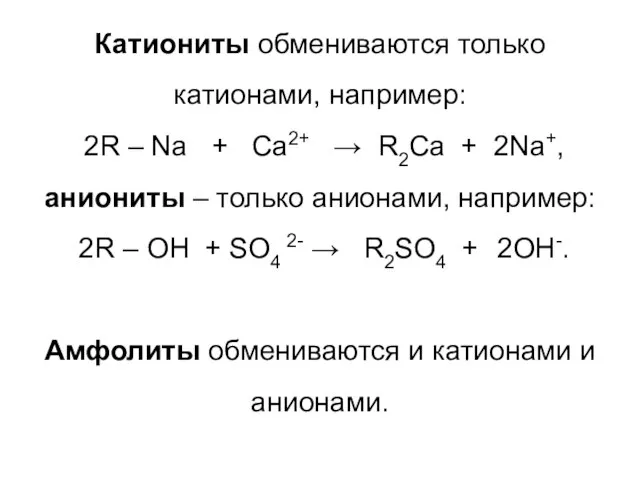
- 24. Катиониты обмениваются только катионами, например: 2R – Na + Ca2+ → R2Ca + 2Na+, аниониты –
- 25. Регенерация ионитов Поскольку ионообменная адсорбция обратима, катиониты и аниониты можно использовать неоднократно. Для этого использованные катиониты
- 26. Количественной характеристикой ионита является полная обменная емкость ПОЕ – количество вещества (в молях), способное связать 1
- 27. Определение ПОЕ осуществляется на основе двух методов: статического, в основе которого лежит титрование. Так, например катионит
- 28. Использование ионитов в фармации и медицине: для очистки, умягчения жесткой и опреснения засоленной воды; консервирования крови
- 30. Скачать презентацию





















 Алотропні модифікації карбону
Алотропні модифікації карбону  Термодинамика. Химическое равновесие. Кинетика
Термодинамика. Химическое равновесие. Кинетика ИЗВЕСТНЫЕ УЧЕНЫЕ – ХИМИКИ Немного из истории химии
ИЗВЕСТНЫЕ УЧЕНЫЕ – ХИМИКИ Немного из истории химии Харчові добавки. e-числа Підготувала учениця 7(11)-Б класу Луцької гімназії №4 Імені Модеста Левицького Цибульська Вікторія
Харчові добавки. e-числа Підготувала учениця 7(11)-Б класу Луцької гімназії №4 Імені Модеста Левицького Цибульська Вікторія  Теория растворов. Растворы электролитов
Теория растворов. Растворы электролитов Моделирование (7 класс)
Моделирование (7 класс) N-(2-амино-3,5-дибромбензил)-N-метилциклогексанамина гидрохлорид
N-(2-амино-3,5-дибромбензил)-N-метилциклогексанамина гидрохлорид Резины – эластомеры
Резины – эластомеры Презентация по Химии "Химические знаки и их история" - скачать смотреть
Презентация по Химии "Химические знаки и их история" - скачать смотреть  Применимость геохимических правил к распространенности лантанидов в земной коре
Применимость геохимических правил к распространенности лантанидов в земной коре Элементы главной подгруппы VII группы Периодической системы Д.И. Менделеева
Элементы главной подгруппы VII группы Периодической системы Д.И. Менделеева Табиғи үдерістерді физика, химия, механика, тағы басқа жаратылыстану ғылымдары зерттейді
Табиғи үдерістерді физика, химия, механика, тағы басқа жаратылыстану ғылымдары зерттейді “Необроблений” мас-спектр (йонізація електронним ударом)
“Необроблений” мас-спектр (йонізація електронним ударом) Ароматические углеводороды. Бензол
Ароматические углеводороды. Бензол Химия неметаллов
Химия неметаллов Группа веществ, изолируемых из биологического материала дистилляцией. (Лекция 11)
Группа веществ, изолируемых из биологического материала дистилляцией. (Лекция 11) Углеродистые конструкционные стали
Углеродистые конструкционные стали Экспериментальное исследование кипения сверхтекучего гелия на цилиндрическом нагревателе внутри пористой оболочки
Экспериментальное исследование кипения сверхтекучего гелия на цилиндрическом нагревателе внутри пористой оболочки Биологически значимые элементы
Биологически значимые элементы Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи
Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи Вклад М.В. Ломоносова в развитие науки химия
Вклад М.В. Ломоносова в развитие науки химия Основные характеристики различных сортов меда
Основные характеристики различных сортов меда The Krebs cycle
The Krebs cycle Метанол, етанол, гліцерин
Метанол, етанол, гліцерин Геохимия гранитоидов, зоны гипергенеза, осадочного процесса
Геохимия гранитоидов, зоны гипергенеза, осадочного процесса Виды химической связи
Виды химической связи Презентация по химии на тему: Бром
Презентация по химии на тему: Бром Периодический закон и периодическая система элементов Д.И. Менделеева
Периодический закон и периодическая система элементов Д.И. Менделеева