Содержание
- 2. Электролизная система состоит из: электролизер (электролитическая ванна), электроды (инертные или активные), электролит (раствор или расплав), источник
- 3. Катод – электрод, подключенный к «–» полюсу внешнего источника тока, на нем идут процессы восстановления. Анод
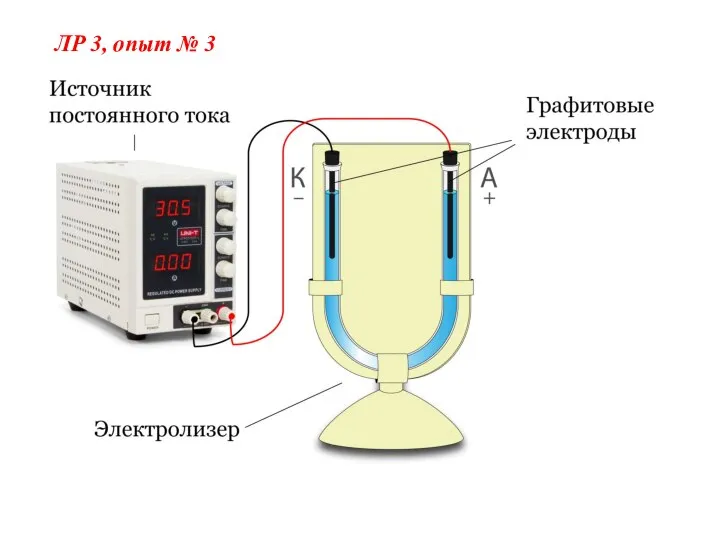
- 4. ЛР 3, опыт № 3
- 5. При отсутствии внешнего электрического поля ионы находятся в беспорядочном движении. При прохождении постоянного электрического тока через
- 6. Характер протекания электродных процессов при электролизе зависит от: состава электролита; pH среды; концентрации ионов электролита; материала
- 7. Количественные характерис-тики процессов электролиза устанавливаются законами Фарадея: I закон Фарадея; II закон Фарадея.
- 8. I закон Фарадея Масса или объём вещества, претерпевшего изменение на электродах, прямо пропорциональна количеству прошедшего через
- 9. II закон Фарадея При прохождении одинакового количества электричества через растворы (расплавы) электролитов массы (объемы) выделяющихся веществ
- 10. Следствия из II закона Фарадея: При прохождении через электролит количества электричества Q=F масса превращенного вещества m=Э
- 11. Количество вещества эквивалента nэ (или число эквивалентов в-ва) определяется: Из II закона Фарадея получаем: nэ1 =
- 12. Пример. При электролизе раствора AgNO3 на аноде выделилось 0,28 л O2. Сколько серебра выделилось на катоде
- 13. Массы выделившихся при электролизе веществ зависят от количества прошедшего электричества и эквивалентов этих веществ и не
- 14. Выход по току Вт Показателем эффективности электролиза является величина выхода по току: Qпракт > Qтеор из-за
- 15. Самостоятельно! В реальных электролизных системах накопление продуктов электролиза на электродах изменяет их природу и величину электродных
- 16. Самостоятельно! Для преодоления поляризации на электроды извне подается избыточное напряжение, называемое перенапряжением (η – «эта»): ηk
- 17. Самостоятельно! Минимальная разность потенциалов, при которой процесс электролиза становится возможным, называется ЭДС разложения электролита (Еразл):
- 18. Электролиз растворов электролитов В процессах на электродах могут участвовать частицы вещества, молекулы или ионы воды. ПРАВИЛА
- 19. 3. Катионы малоактивных Ме, расположенные в ряду напряжений после Н , восстанавливаются. Примечание: Если в р-ре
- 20. Анодные процессы: Характер анодных процессов определяется материалом анода. При использовании активного анода (любой Ме, кроме Au
- 21. При использовании инертного анода на нем идут процессы окисления. 1. Простые анионы (Сl–, I–, Br–, S2–)
- 22. !!! Катодный процесс: зависит только от активности катиона металла. Анодный процесс: зависит в первую очередь от
- 24. При записи схемы электролиза указывается материал электродов, заряды электродов. Отрицательный электрод (катод) принято изображать слева, положительный
- 25. Электролиз раствора СuSO4 на инертных (графитовых) электродах:
- 26. Электролиз раствора NaCl на инертных (графитовых) электродах: Что изменится: K(–) Zn│NaCl, H2O│C (+)А ?
- 27. В результате реакций, идущих у электродов, возможно изменение pH раствора у этих электродов: Этот факт используется
- 28. Электролиз NaCl На катоде выделяется газ Н2 и образуется щелочь NaОН. Увеличение СОН_ обусловило изменение окраски
- 29. Электролиз раствора Na2SO4 на инертных (платиновых) электродах:
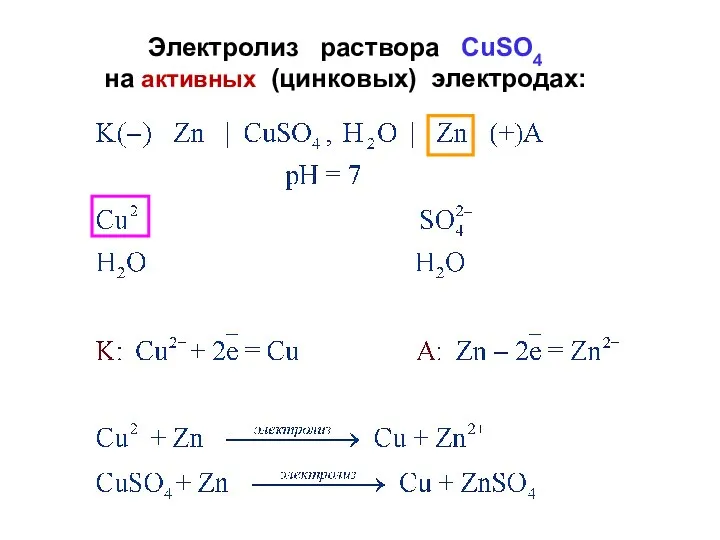
- 30. Электролиз раствора СuSO4 на активных (цинковых) электродах:
- 31. Электролиз раствора NaCl на активных (цинковых) электродах:
- 32. Электролиз раствора Na2SO4 на активных (цинковых) электродах:
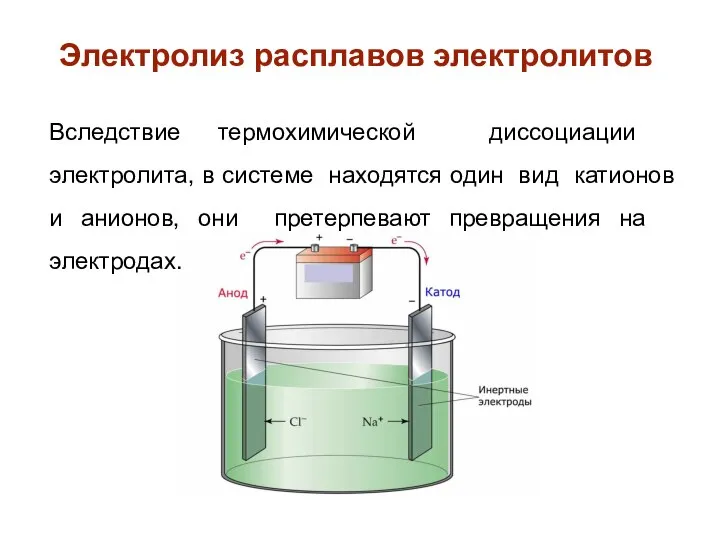
- 33. Электролиз расплавов электролитов Вследствие термохимической диссоциации электролита, в системе находятся один вид катионов и анионов, они
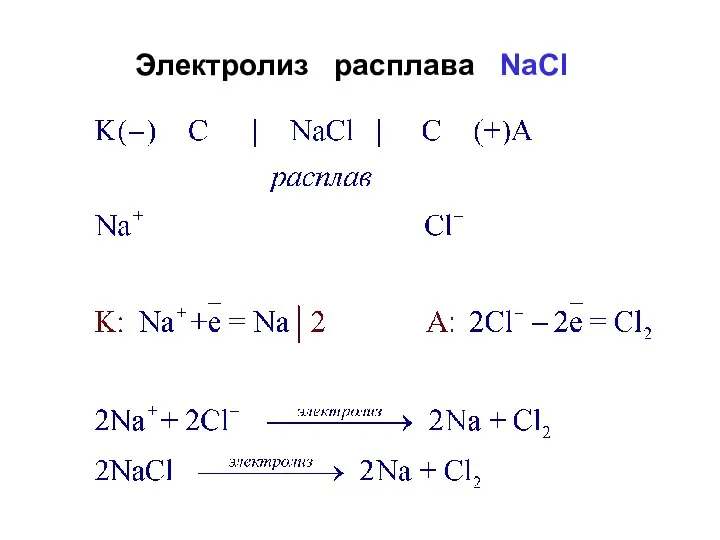
- 34. Электролиз расплава NaCl
- 35. ПРИМЕНЕНИЕ ЭЛЕКТРОЛИЗА 1. Электрохимическое производство химических продуктов: получение Сl2 и NaOH (электролиз водного р-ра NaCl); получение
- 36. 3. Гальванотехника: гальваностегия – нанесение Ме-х покрытий; гальванопластика – получение изделий путем электролиза. 4. Электрохимическая обработка
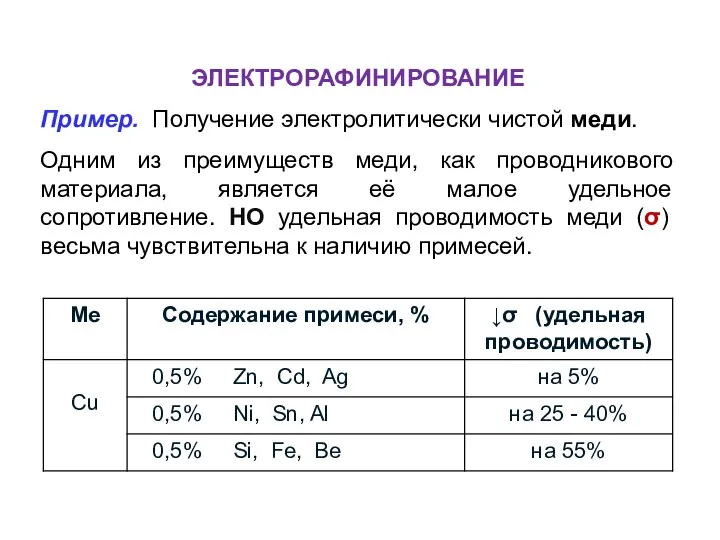
- 37. ЭЛЕКТРОРАФИНИРОВАНИЕ Пример. Получение электролитически чистой меди. Одним из преимуществ меди, как проводникового материала, является её малое
- 38. K(–) Cu ⎪ CuSO4, H2O ⎪ Cu ( Fe, Pb, Ag ) (+)А ↓ ↓ (чистая
- 40. Скачать презентацию
































 Смазочные материалы. Моторные масла
Смазочные материалы. Моторные масла Генетическая связь классов соединений
Генетическая связь классов соединений Презентация по Химии "Теория нормализации" - скачать смотреть бесплатно
Презентация по Химии "Теория нормализации" - скачать смотреть бесплатно Зміна складу і технологічних властивостей молока під впливом різних факторів
Зміна складу і технологічних властивостей молока під впливом різних факторів pH жидкостей, необходимых для человека
pH жидкостей, необходимых для человека  Материаловедение. Теория сплавов
Материаловедение. Теория сплавов Химия, как наука. Основные понятия и законы
Химия, как наука. Основные понятия и законы Силикатная промышленность
Силикатная промышленность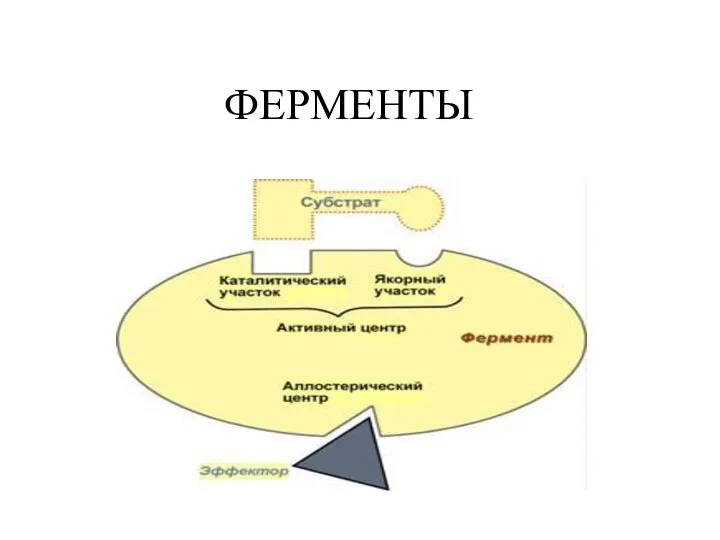 Ферменты. Значение ферментов
Ферменты. Значение ферментов Материаловедение. Влияние нагрева на структуру деформированного металла. (Тема 5)
Материаловедение. Влияние нагрева на структуру деформированного металла. (Тема 5) Предмет химии. Вещества. 8 клвсс
Предмет химии. Вещества. 8 клвсс Александр Михайлович БУТЛЕРОВ Презентация учителя химии школы №122 Центрального р-на Санкт-Петербурга Поспеловой Светланы Викто
Александр Михайлович БУТЛЕРОВ Презентация учителя химии школы №122 Центрального р-на Санкт-Петербурга Поспеловой Светланы Викто Introduction to effective permeability and relative permeability
Introduction to effective permeability and relative permeability Вода и растворы. Лекция 3
Вода и растворы. Лекция 3 Характеристика, состав и свойства нефти и нефтепродуктов
Характеристика, состав и свойства нефти и нефтепродуктов Теоретические основы применения органических реагентов в качественном анализе. (Лекция 8)
Теоретические основы применения органических реагентов в качественном анализе. (Лекция 8) Презентация по Химии "М.В. Ломоносов и химия" - скачать смотреть
Презентация по Химии "М.В. Ломоносов и химия" - скачать смотреть  Элементы V группы Периодической системы химических элементов Д.И.Менделеева Работу выполнила учитель химии МОУ Северн
Элементы V группы Периодической системы химических элементов Д.И.Менделеева Работу выполнила учитель химии МОУ Северн Добування кисню та вивчення його властивостей
Добування кисню та вивчення його властивостей Классификация химических реакций в неорганической химии
Классификация химических реакций в неорганической химии Строение газообразных, жидких и твердых тел
Строение газообразных, жидких и твердых тел Химическая взрывчатка
Химическая взрывчатка Органическая химия. Лекция 12
Органическая химия. Лекция 12 Презентация по химии Алканы, алкены, алкины.
Презентация по химии Алканы, алкены, алкины. Презентация по Химии "Степень окисления" - скачать смотреть бесплатно_
Презентация по Химии "Степень окисления" - скачать смотреть бесплатно_ Пестицидтердің қоршаған ортаға тигізетін әсері
Пестицидтердің қоршаған ортаға тигізетін әсері Презентация по Химии "Альдегиды, свойства, получение, применение" - скачать смотреть
Презентация по Химии "Альдегиды, свойства, получение, применение" - скачать смотреть  Соли. Названия и классификация солей
Соли. Названия и классификация солей