Содержание
- 2. Электролиз (электро... және грек. lysіs – еру, ыдырау) – еріген немесе балқыған электролитке батырылған электродтарда электр
- 3. Электролиз кезіндегі процестер Электрондар иондармен бірінші жақты өткізгіштер екінші жақты өткізгіштермен шектесетін электр тізбегі бар жерлерде
- 4. Сулы ерітінділердің оттексіз қышқылдары және олардың тұздарының анодтағы электролизі кезінде аниондар разрядталады. Көбінесе, HI, HBr, HCl
- 5. Егер MgCl2 балқымасы арқылы ток өткізетін болсақ, магний катиондары теріс ішкі тізбек арқылы келетін электрондармен өзара
- 6. KOH4H=2H22O=O2H2SO4 NiSO4 ерітіндісінің никельді анодпен электролизі. Никельдің стандартты потенциалы (-0,250B) -0,41Bден кішкене артық; сондықтан NiSO4 бейтарап
- 7. Ашылу тарихы Электрохимия ғылым ретінде ХVIII және XIX ғасырларда шет елдерде қалыптасты. Тек сол кезде шешімі
- 8. Электролиттік процестер металдардың балқымаларының алынуы. гальваникалық қабаттардың алынуы бейорганикалық заттардың алынуы (хлор, сутегі, оттегі, сілтілер және
- 9. Электролиздің мақсатты қолданылуы: оның көмегімен таза элементтің массалық үлесі жүз процентке ұмтылатын металдарды алуға болады. Ал
- 11. Скачать презентацию
Электролиз (электро... және грек. lysіs – еру, ыдырау) – еріген немесе
Электролиз (электро... және грек. lysіs – еру, ыдырау) – еріген немесе
Электролиз кезіндегі процестер
Электрондар иондармен бірінші жақты өткізгіштер екінші жақты өткізгіштермен шектесетін
Электролиз кезіндегі процестер
Электрондар иондармен бірінші жақты өткізгіштер екінші жақты өткізгіштермен шектесетін
Бұл жүйе энергияның химиялық көзі деп аталады, егер бұл процесстер өзімен жүреді .
Егер олардың жүруі электр энергиясының қосылуымен шартталатын болса, онда электролиз жүреді.
Электролиз кезінде электродтарда жүретін электрохимиялық процестер ең алдымен электрохимиялық жүйелерге сәйкес болатын электродтық потенциалдар қатынасына тәуелді болады.
Бірнеше мүмкін болатын процестерден минимальды энергия шығыны болатыны жүреді.
Бұл катодта ең көп электродты потенциалы болатын электрохимиялық жүйелердің тотықсызданған формаларының тотықтануы жүреді, ал анодта ең аз электродты потенциалы болатын жүйелердің тотықтанған формалары тотықсызданады.
Сулы ерітінділердің оттексіз қышқылдары және олардың тұздарының анодтағы электролизі кезінде аниондар
Сулы ерітінділердің оттексіз қышқылдары және олардың тұздарының анодтағы электролизі кезінде аниондар
Егер MgCl2 балқымасы арқылы ток өткізетін болсақ, магний катиондары теріс ішкі
Егер MgCl2 балқымасы арқылы ток өткізетін болсақ, магний катиондары теріс ішкі
KOH4H=2H22O=O2H2SO4 NiSO4 ерітіндісінің никельді анодпен электролизі. Никельдің стандартты потенциалы (-0,250B) -0,41Bден
KOH4H=2H22O=O2H2SO4 NiSO4 ерітіндісінің никельді анодпен электролизі. Никельдің стандартты потенциалы (-0,250B) -0,41Bден
Ашылу тарихы
Электрохимия ғылым ретінде ХVIII және XIX ғасырларда шет елдерде қалыптасты.
Ашылу тарихы
Электрохимия ғылым ретінде ХVIII және XIX ғасырларда шет елдерде қалыптасты.
Электролиттік процестер
металдардың балқымаларының алынуы.
гальваникалық қабаттардың алынуы
бейорганикалық заттардың алынуы (хлор, сутегі, оттегі,
Электролиттік процестер
металдардың балқымаларының алынуы.
гальваникалық қабаттардың алынуы
бейорганикалық заттардың алынуы (хлор, сутегі, оттегі,
органикалық заттардың алынуы
металдардың тазартылуы (қола, күміс)
металдардың алынуы (магнии, цинк, литий, натрий, калий, алюминий
металдар беттерінің өңделуі.
электорофорез көмегімен пленкалардың жабылуы.
электродиализ және судың тұзсыздандыруы.
Электролиздің мақсатты қолданылуы: оның көмегімен таза элементтің массалық үлесі жүз процентке
Электролиздің мақсатты қолданылуы: оның көмегімен таза элементтің массалық үлесі жүз процентке








 Уран. Получение урана
Уран. Получение урана Химическое оружие
Химическое оружие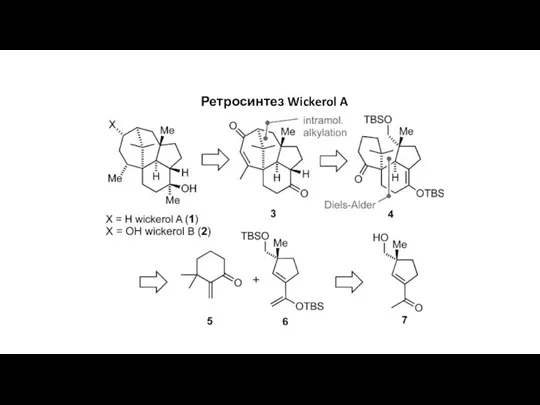 Ретросинтез Wickerol A
Ретросинтез Wickerol A Нефть. Общие сведения
Нефть. Общие сведения Процессы формирования водородной плазмы в зоне резания
Процессы формирования водородной плазмы в зоне резания Фенолы. Простые эфиры
Фенолы. Простые эфиры Органическая химия. Установочная лекция
Органическая химия. Установочная лекция Презентация по Химии "Взаимосвязь химии и русского языка" - скачать смотреть
Презентация по Химии "Взаимосвязь химии и русского языка" - скачать смотреть  Неорганическая химия Сероводород
Неорганическая химия Сероводород ИЗ ОПЫТА ИСПОЛЬЗОВАНИЯ ИНТЕРАКТИВНОЙ ДОСКИ НА УРОКАХ ХИМИИ.
ИЗ ОПЫТА ИСПОЛЬЗОВАНИЯ ИНТЕРАКТИВНОЙ ДОСКИ НА УРОКАХ ХИМИИ. 01. Характеристика ХЭ на основании его положения в ПС Д.И. Менделеева
01. Характеристика ХЭ на основании его положения в ПС Д.И. Менделеева Простой борный суперфосфат
Простой борный суперфосфат Мұнай. Мұнайдың шығу тарихы
Мұнай. Мұнайдың шығу тарихы I закон термодинамики, его применение для расчёта тепловых эффектов
I закон термодинамики, его применение для расчёта тепловых эффектов Колообіг Оксигену Підготувала: учениця 10-В
Колообіг Оксигену Підготувала: учениця 10-В  Общие вопросы аналитической химии. Химические методы обнаружения неорганических веществ
Общие вопросы аналитической химии. Химические методы обнаружения неорганических веществ Химическая связь
Химическая связь Темір туралы
Темір туралы Кислоты
Кислоты Алкіни
Алкіни  Органическая химия. Лекция 12
Органическая химия. Лекция 12 Высокомолекулярные соединения полимеры
Высокомолекулярные соединения полимеры Что у нас на столе? Сороколетова Ольга Аракчеева Елена
Что у нас на столе? Сороколетова Ольга Аракчеева Елена Масса и формулы (8 класс)
Масса и формулы (8 класс) Презентация по Химии "Алкины" - скачать смотреть бесплатно
Презентация по Химии "Алкины" - скачать смотреть бесплатно Нуклеиновые кислоты
Нуклеиновые кислоты Характеристика s,p,d,f - элементов
Характеристика s,p,d,f - элементов Витамины и коферменты
Витамины и коферменты