Содержание
- 2. Терминология Электролиз – совокупность ОВР, осуществляющихся на электродах при пропускании через раствор или расплав электролита постоянного
- 3. Электролиз расплавов NaCl, расплав NaCl → Na+ + Cl- (диссоциация на ионы) Катод(-): Na+ Na+ +
- 4. Электролиз расплавов NaCl, расплав NaCl → Na+ + Cl- (диссоциация на ионы) Катод(-): Na+ Na+ +
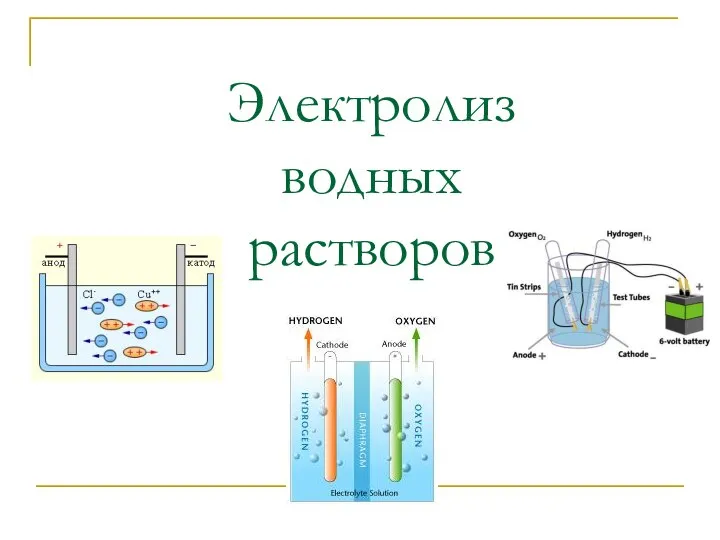
- 5. Электролиз водных растворов
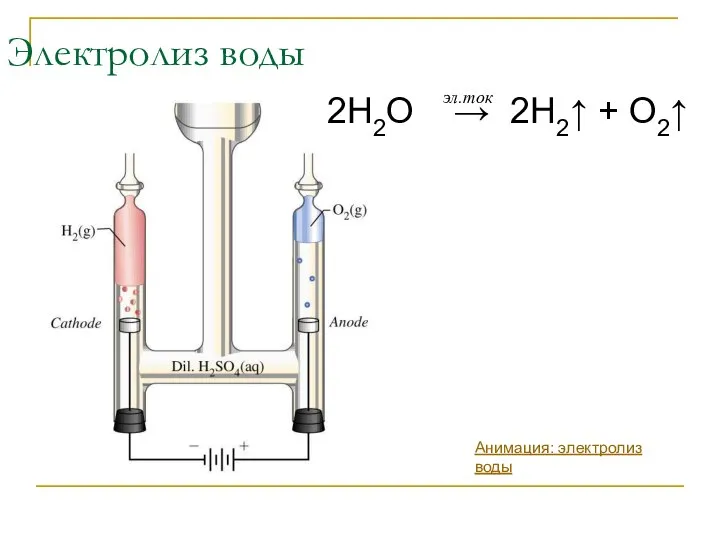
- 6. Электролиз воды 2H2O → 2H2↑ + O2↑ эл.ток Анимация: электролиз воды
- 7. Окисление и восстановление воды на электродах Катод H2O +1 -2 → H + OH- 0 2
- 8. Порядок восстановления на катоде Eº, В Процесс восстановления воды 2H2O + 2e- = H2 + 2OH-
- 9. Порядок окисления на аноде CO32-, SO42-, NO3- и т.д. 2H2O - 4e- → O20 + 4H+
- 10. Электролиз растворов солей (1). CuCl2, раствор CuCl2 → Cu2+ + 2Cl- (ЭД) Катод(-): Cu2+, H2O Cu2+
- 11. Электролиз CuCl2 Посмотрите схему
- 12. CuSO4, раствор CuSO4 → Cu2+ + SO42- (ЭД) Катод: Cu2+, H2O Cu2+ + 2e- → Cu0
- 13. NaCl, раствор NaCl → Na+ + Cl- (ЭД) Катод: Na+, H2O 2H2O + 2e- → H2↑
- 14. Электролиз растворов солей (4). Na2SO4, раствор Na2SO4 → 2Na+ + SO42- (ЭД) Катод: Na+, H2O 2H2O
- 15. Электролиз растворов солей (4). Na2SO4, раствор Na2SO4 → 2Na+ + SO42- (ЭД) Катод: Na+, H2O 2H2O
- 16. Электролиз растворов кислородсодержащих кислот H2SO4, раствор H2SO4 → 2H+ + SO42- (ЭД) Катод: H+, H2O 2H+
- 17. Электролиз растворов щелочей NaOH , раствор NaOH → Na+ + OH- (ЭД) Катод: Na+, H2O 2H2O
- 18. Электролиз по Кольбе CH3COONa , раствор CH3COONa → Na+ + CH3COO- (ЭД) Катод: Na+, H2O 2H2O
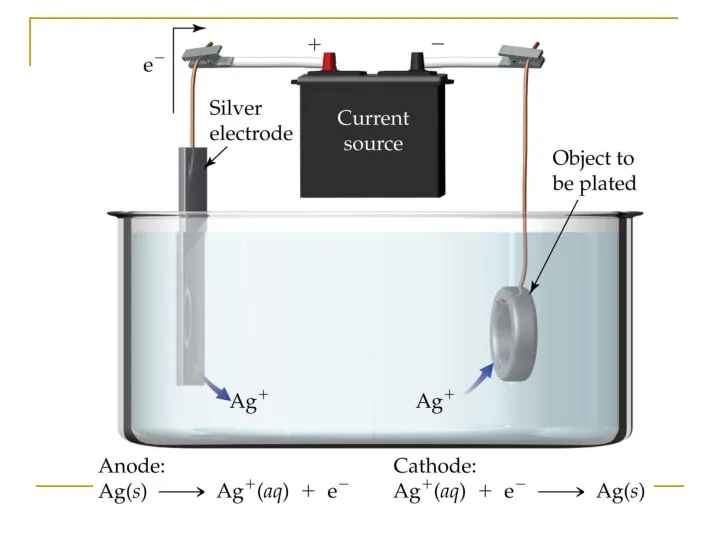
- 19. Электролиз с активным анодом NiSO4, раствор; анод - никель NiSO4 → Ni2+ + SO42- (ЭД) Катод:
- 21. Законы электролиза 1. Для любого данного электродного процесса количество вещества, испытывающее превращение в данном электродном процессе,
- 22. Законы электролиза 2. При прохождении одинакового количества электричества через растворы различных электролитов количества каждого из веществ,
- 23. Расчетные задачи по теме «Электролиз» Через 10%-ный раствор хлорида натрия массой 400 г пропустили постоянный электрический
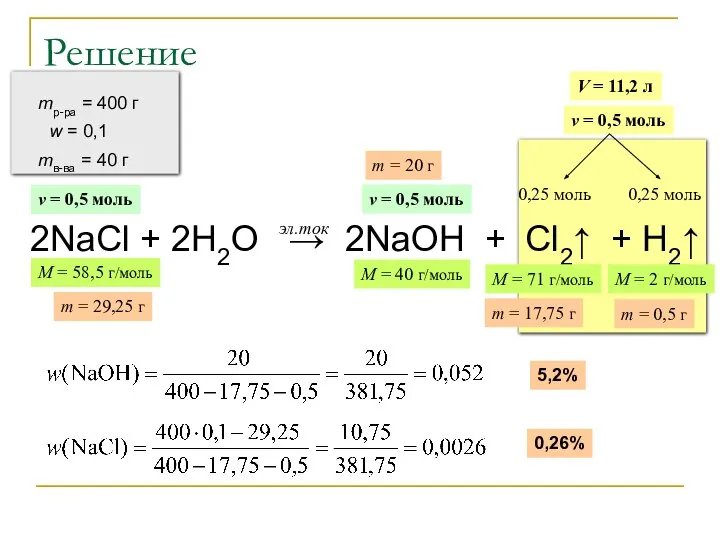
- 24. Решение 2NaCl + 2H2O → 2NaOH + Cl2↑ + H2↑ эл.ток mр-ра = 400 г w
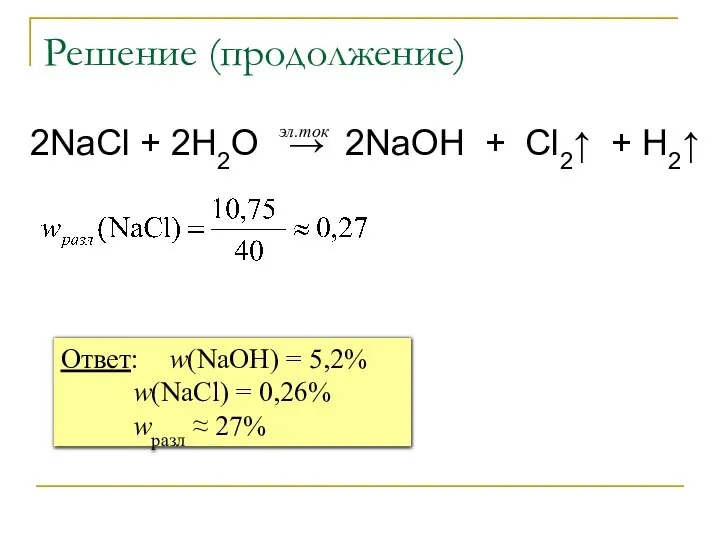
- 25. Решение (продолжение) 2NaCl + 2H2O → 2NaOH + Cl2↑ + H2↑ эл.ток Ответ: w(NaOH) = 5,2%
- 26. Майкл Фарадей (22.09.1791 – 25.08.1867) с 1813 г. работал в лаборатории Г.Дэви 1813 – 1815 сопровождает
- 27. Майкл Фарадей 1825 директор лаборатории Королевского общества, с 1827 г. – профессор. 1828 – получил этилсерную
- 29. Скачать презентацию





















 Методы трансформации карбоновых кислот и их производных
Методы трансформации карбоновых кислот и их производных Серная кислота
Серная кислота Галогены. История открытия галогенов
Галогены. История открытия галогенов Роль хімічних знань у пізнанні природи
Роль хімічних знань у пізнанні природи Классификация неорганических веществ
Классификация неорганических веществ Метаболизм липидов. Липолиз. Окисление жирных кислот и глицерола
Метаболизм липидов. Липолиз. Окисление жирных кислот и глицерола 8 класс. РЕШЕНИЕ ЗАДАЧ ПО УРАВНЕНИЯМ ХИМИЧЕСКИХ РЕАКЦИЙ
8 класс. РЕШЕНИЕ ЗАДАЧ ПО УРАВНЕНИЯМ ХИМИЧЕСКИХ РЕАКЦИЙ Водородная и донорно-акцепторная связи. (Лекция 15)
Водородная и донорно-акцепторная связи. (Лекция 15) «Гидролиз солей» Тема урока:
«Гидролиз солей» Тема урока: Титан. История открытия титана
Титан. История открытия титана Открытие водорода
Открытие водорода Хлор. Способы получения хлора
Хлор. Способы получения хлора Вязкость жидкости
Вязкость жидкости Объемная доля газа в смеси. (Урок 16. 7 класс)
Объемная доля газа в смеси. (Урок 16. 7 класс) Тосол. Гликолевые антифризы
Тосол. Гликолевые антифризы Нефть, как одна из основ жизни
Нефть, как одна из основ жизни Химия. Дисперсные системы. Растворы
Химия. Дисперсные системы. Растворы КОРОЗІЯ МЕТАЛІВ ЗАХИСТ ВІД КОРОЗІЇ Робота учениці 10-Б Єлісєєвої Марії
КОРОЗІЯ МЕТАЛІВ ЗАХИСТ ВІД КОРОЗІЇ Робота учениці 10-Б Єлісєєвої Марії  Щелочные металлы. Натрий. Выполнила: Ученица 9 Б класса МОУ СОШ №172 Мошкова Любовь. 2011 год.
Щелочные металлы. Натрий. Выполнила: Ученица 9 Б класса МОУ СОШ №172 Мошкова Любовь. 2011 год. Презентация по Химии "«Нитраты - минеральные удобрения»" - скачать смотреть
Презентация по Химии "«Нитраты - минеральные удобрения»" - скачать смотреть  Решение заданий ЕГЭ на составление окислительно-восстановительных реакций
Решение заданий ЕГЭ на составление окислительно-восстановительных реакций Азо-, диазосоединения
Азо-, диазосоединения Химическая кинетика
Химическая кинетика Нечаев 18
Нечаев 18 Графен. Силицен
Графен. Силицен Введение в химию органических соединений
Введение в химию органических соединений Автомобильные пластичные смазки
Автомобильные пластичные смазки Конструкционные материалы на основе легких металлов: сплавы алюминия
Конструкционные материалы на основе легких металлов: сплавы алюминия