Содержание
- 2. 1. История открытия галогенов 2. Положение в ПСХЭ 3. Химические свойства 4. Применение 5.Проверка знаний Главная
- 3. Фтор История открытия галогенов Хлор Бром Йод Астат
- 4. В 1886 году французский химик А. Муассан, используя электролиз жидкого фтороводорода, охлажденного до температуры –23°C, смог
- 5. В 1774 году шведский ученый К. Шееле открыл хлор, который принял за сложное вещество и назвал
- 6. В 1825 году французский химик А.Ж.Балар при изучении маточных рассолов выделил темно-бурую жидкость, который он назвал
- 7. В 1811 году французский химик Бернар Куртуа открыл иод путём перегонки маточных растворов от своего азотнокислого
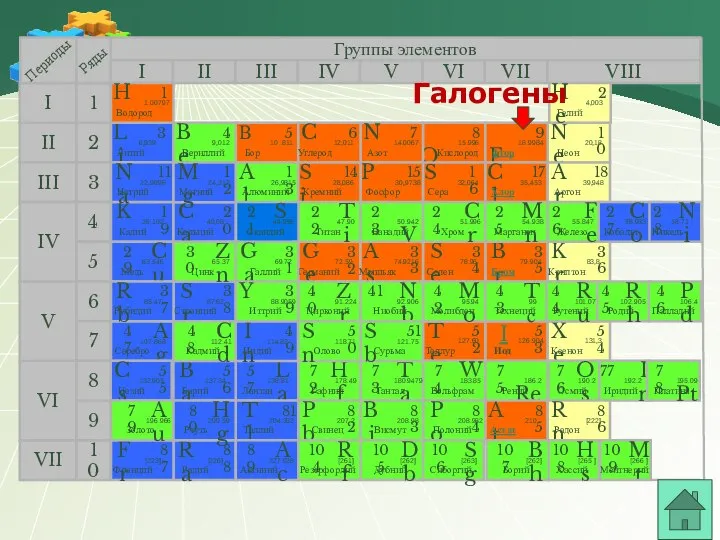
- 8. Группы элементов I III II VIII IV V VI VII II I III VII VI V
- 9. Группы элементов I III II VIII IV V VI VII II I III VII VI V
- 10. Группы элементов I III II VIII IV V VI VII II I III VII VI V
- 11. Группы элементов I III II VIII IV V VI VII II I III VII VI V
- 12. Группы элементов I III II VIII IV V VI VII II I III VII VI V
- 13. Группы элементов I III II VIII IV V VI VII II I III VII VI V
- 14. Химические свойства Взаимодействие с металлами: 2К + Cl2→ 2КCl 2Fe + 3Cl2 → 2FeCl3 Cu +
- 15. Химические свойства Взаимодействие с неметаллами: А) с водородом H2 + F2 → 2HF +Q Скорость H2
- 16. Химические свойства Взаимодействие со сложными веществами: А) с водой 2H2O + F2 → 4HF + O2
- 17. Химические свойства Взаимодействие со сложными веществами: Б) «ряд активности» галогенов F2 > Cl2 > Br2 >
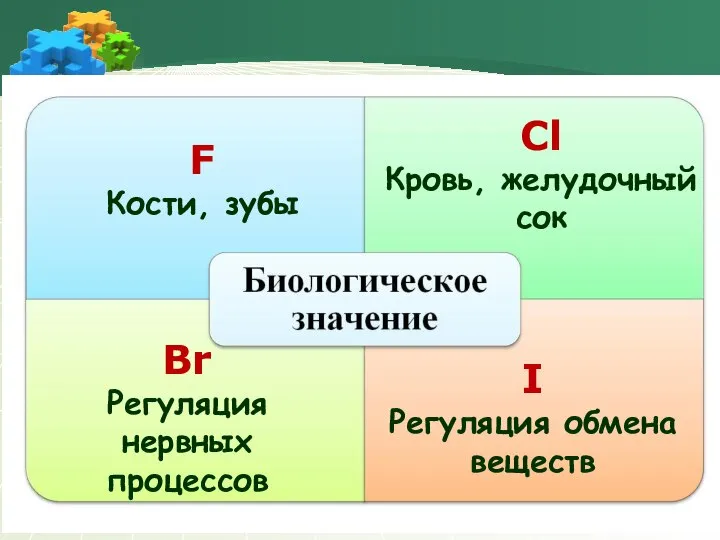
- 18. F Кости, зубы Сl Кровь, желудочный сок Br Регуляция нервных процессов I Регуляция обмена веществ
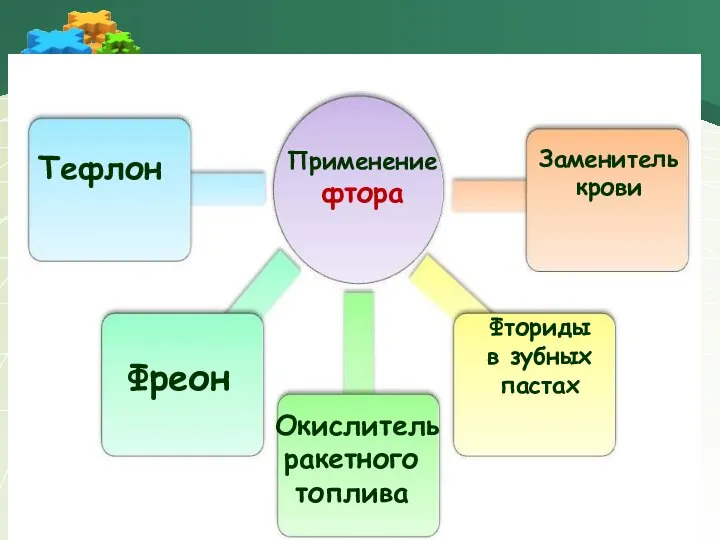
- 19. Применение фтора Тефлон Фреон Окислитель ракетного топлива Заменитель крови Фториды в зубных пастах
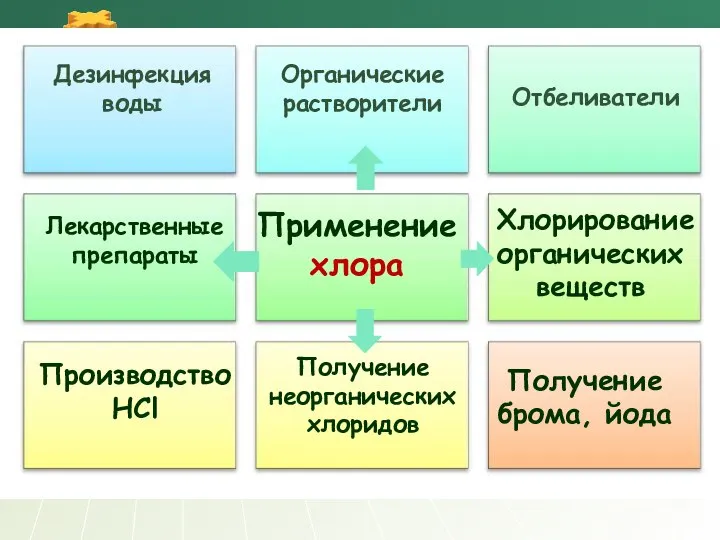
- 20. Применение хлора Отбеливатели Производство HCl Получение брома, йода Дезинфекция воды Органические растворители Лекарственные препараты Хлорирование органических
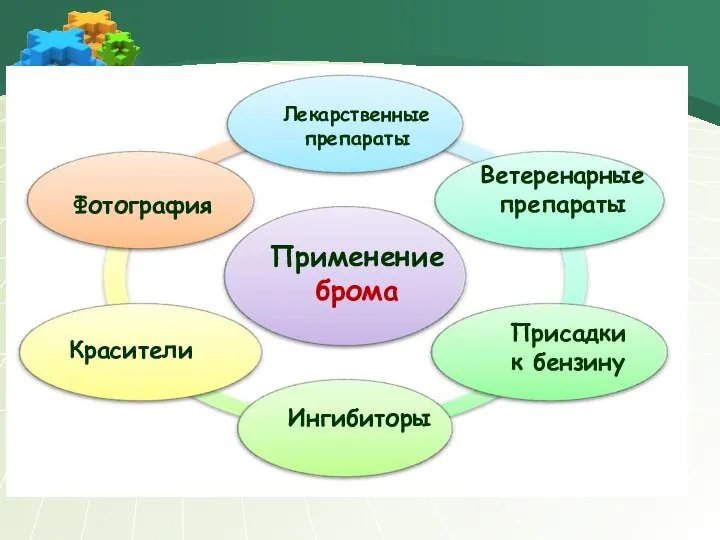
- 21. Применение брома Лекарственные препараты Красители Фотография Ветеренарные препараты Ингибиторы Присадки к бензину
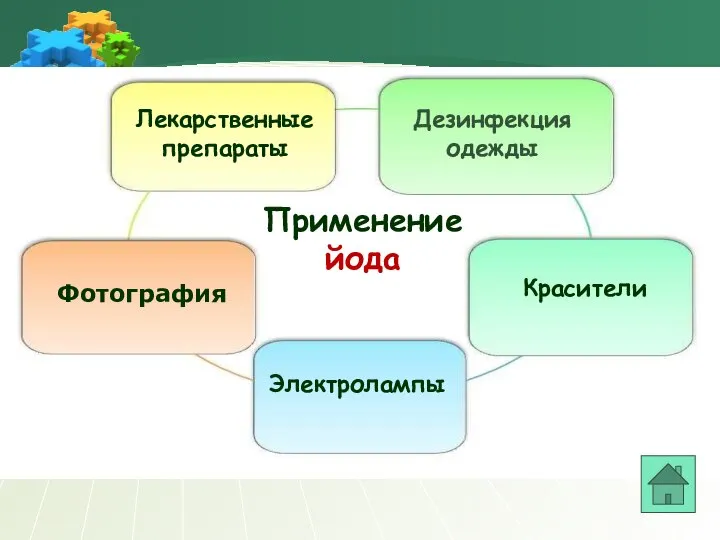
- 22. Применение йода Лекарственные препараты Фотография Красители Дезинфекция одежды Электролампы
- 23. Химические свойства галогенов Вставьте коэффициенты: Na + Cl2 = NaCl S + F2 = SF6 Fe
- 24. Подумайте… Что образуется в данной реакции, оксид фтора или фторид кислорода? F2 + O2 →
- 26. Скачать презентацию
















 Фенолы. Физические свойства. Получение
Фенолы. Физические свойства. Получение Объемная доля газа в смеси. (Урок 16. 7 класс)
Объемная доля газа в смеси. (Урок 16. 7 класс) Мұнай, құрамыөңдеу әдістері
Мұнай, құрамыөңдеу әдістері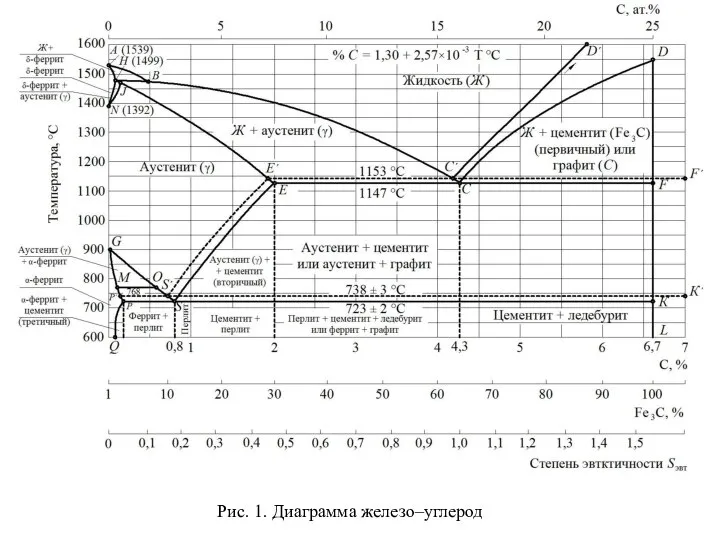 Чугуны и стали
Чугуны и стали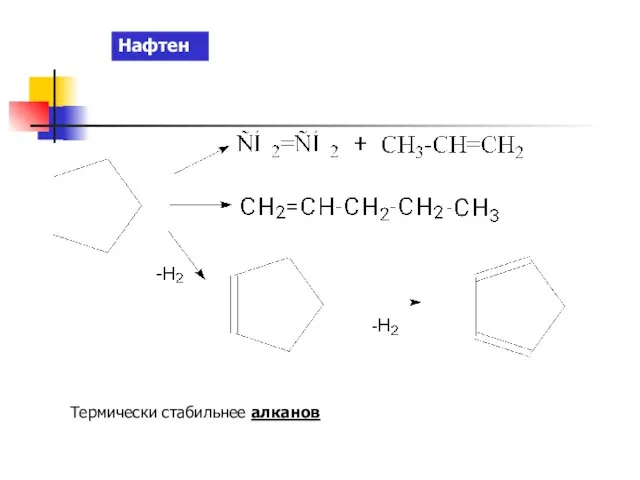 Нафтены
Нафтены «ХИМИКИ НА ЗАЩИТЕ РОДИНЫ»
«ХИМИКИ НА ЗАЩИТЕ РОДИНЫ» Некоторые примеры использования Ферментов в промышленности
Некоторые примеры использования Ферментов в промышленности Синтез нанопроволок, наностержней и нанотрубок неорганических соединений. (Лекция 8)
Синтез нанопроволок, наностержней и нанотрубок неорганических соединений. (Лекция 8) Слайд-шоу
Слайд-шоу Пролекарственные стратегии в создании клинически используемых лекарственных средств
Пролекарственные стратегии в создании клинически используемых лекарственных средств Презентация по Химии "Строение атома" - скачать смотреть бесплатно_
Презентация по Химии "Строение атома" - скачать смотреть бесплатно_ Месторождения железистых кварцитов
Месторождения железистых кварцитов Гомология и изомерия алканов. 10 класс
Гомология и изомерия алканов. 10 класс Комплексные соединения
Комплексные соединения Гормоны. Регуляция метаболизма
Гормоны. Регуляция метаболизма Натуральний каучук Підготувала учениця 11-Б класу ЗОШ І-ІІІст. №11 Відняк Людмила
Натуральний каучук Підготувала учениця 11-Б класу ЗОШ І-ІІІст. №11 Відняк Людмила  Кислотно-основні рівноваги в біологічних системах. (Лекція 2)
Кислотно-основні рівноваги в біологічних системах. (Лекція 2) Исследование фруктовых и овощных соков на наличие в них синтетических красителей и кислотность среды
Исследование фруктовых и овощных соков на наличие в них синтетических красителей и кислотность среды Азот и его соединения
Азот и его соединения Базовое нефтехимическое сырье
Базовое нефтехимическое сырье Алканы. Физические свойства
Алканы. Физические свойства Пластмаси, синтетичні каучуки Підготували учениці 11-б класу Оренбургська Марина та Козаренко Таїсія
Пластмаси, синтетичні каучуки Підготували учениці 11-б класу Оренбургська Марина та Козаренко Таїсія  Карбонат калия K2CO3
Карбонат калия K2CO3 Оксиды, свойства и способы получения
Оксиды, свойства и способы получения Химический эквивалент. Формульные единицы
Химический эквивалент. Формульные единицы ЛРС и производящие растения, содержащие полисахариды
ЛРС и производящие растения, содержащие полисахариды Алканы
Алканы Явище ізомерії. Структурна ізомерія Близнюки органічного світу
Явище ізомерії. Структурна ізомерія Близнюки органічного світу