Электронное и пространственное строение молекул органических соединений – основа биологической активности
Содержание
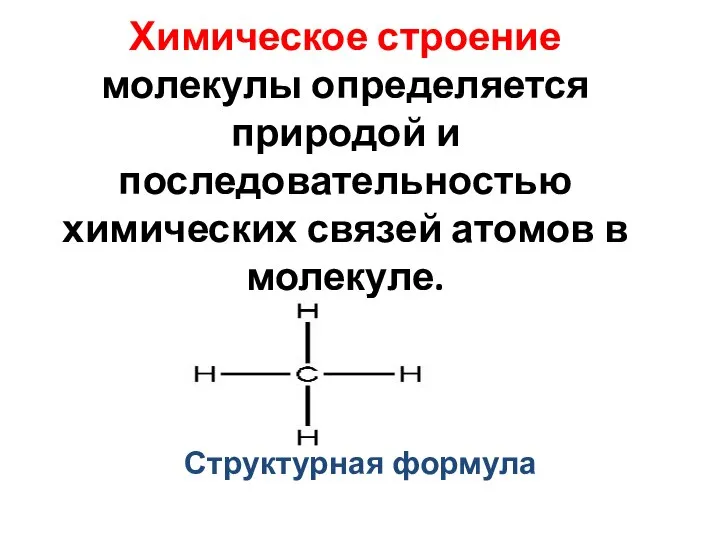
- 2. Химическое строение молекулы определяется природой и последовательностью химических связей атомов в молекуле. Н Н - С
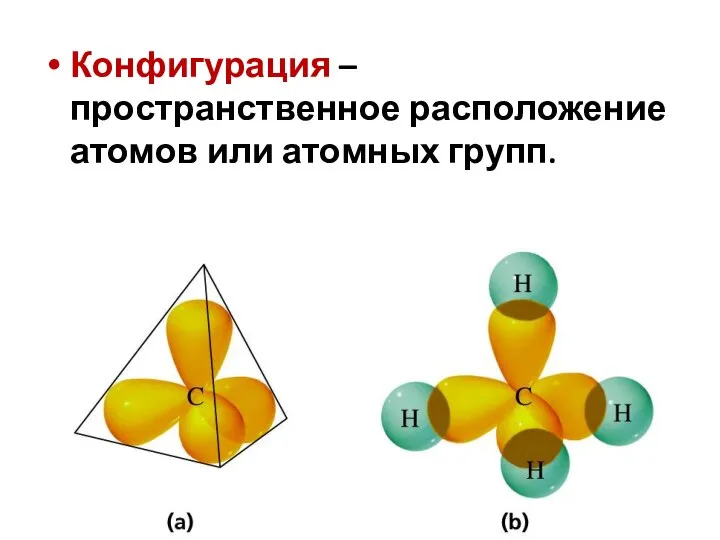
- 3. Конфигурация – пространственное расположение атомов или атомных групп.
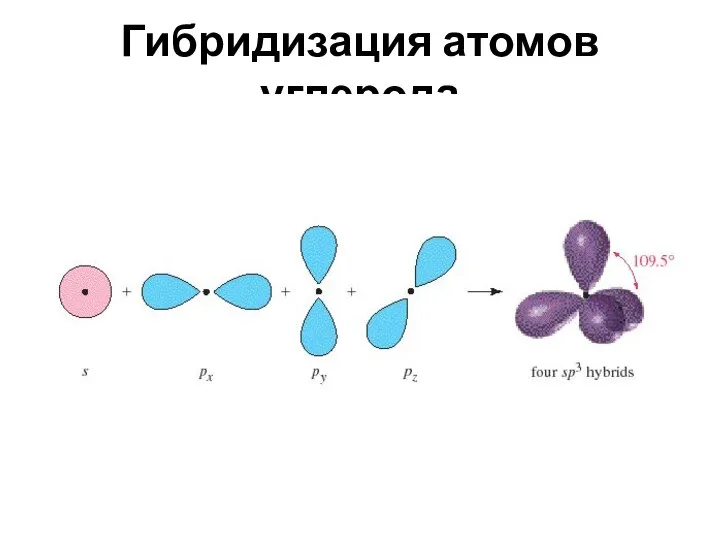
- 4. Гибридизация атомов углерода
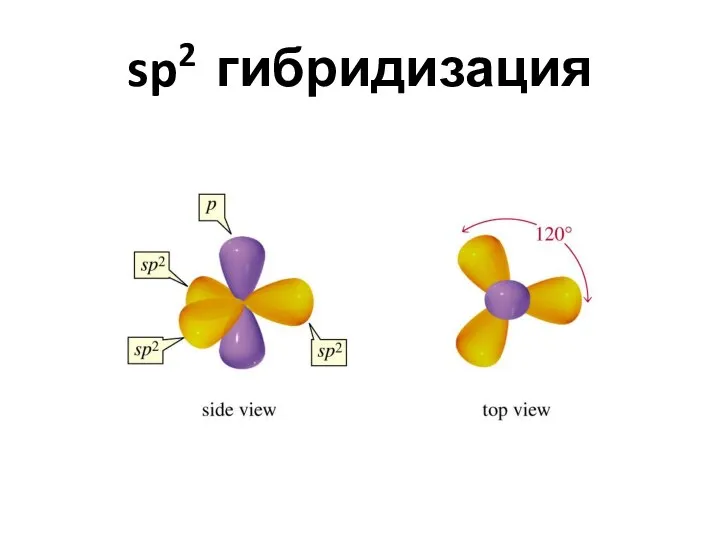
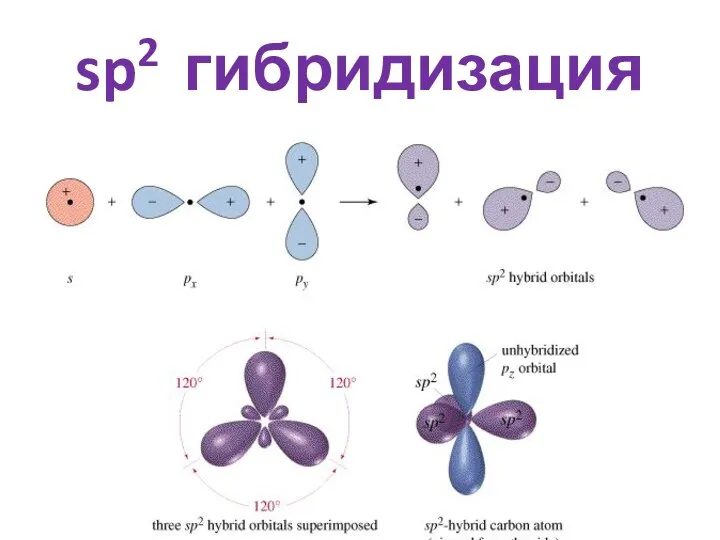
- 5. sp2 гибридизация
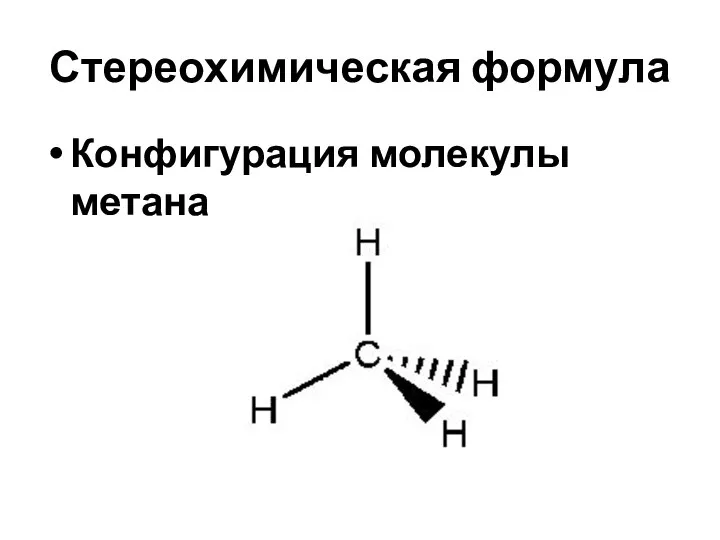
- 6. Стереохимическая формула Конфигурация молекулы метана
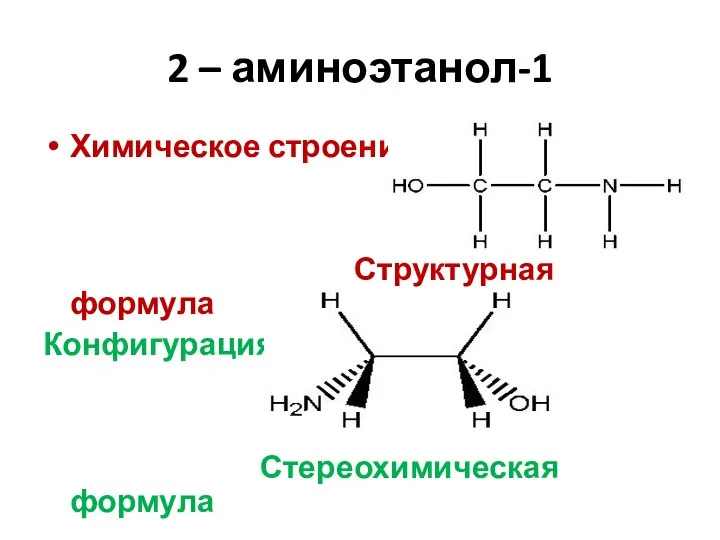
- 7. 2 – аминоэтанол-1 Химическое строение Структурная формула Конфигурация Стереохимическая формула
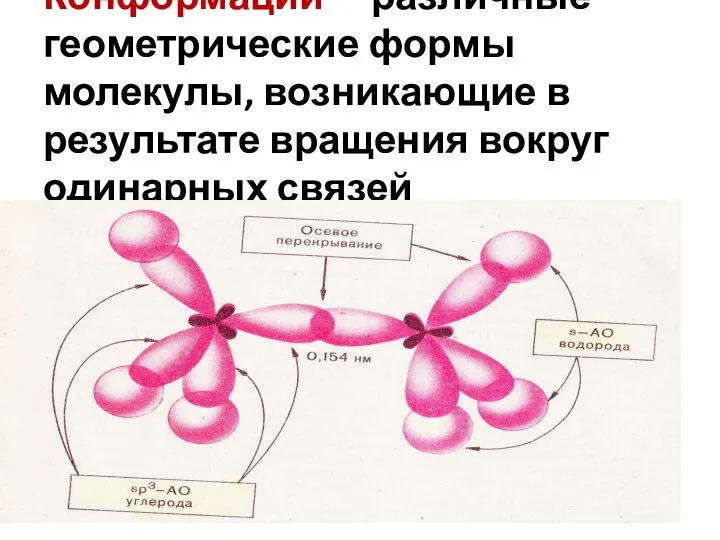
- 8. Конформации – различные геометрические формы молекулы, возникающие в результате вращения вокруг одинарных связей
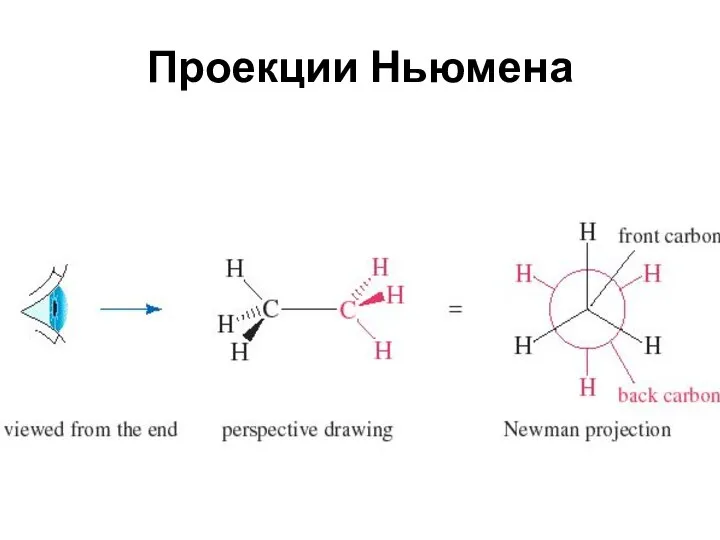
- 10. Проекции Ньюмена
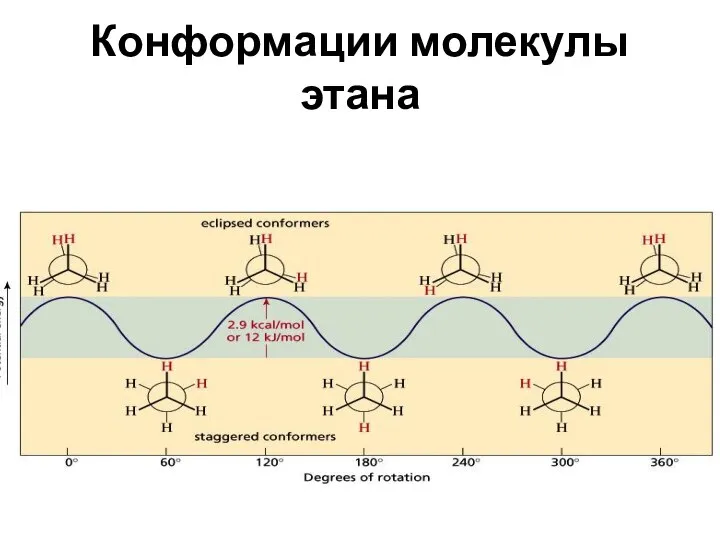
- 11. Конформации молекулы этана
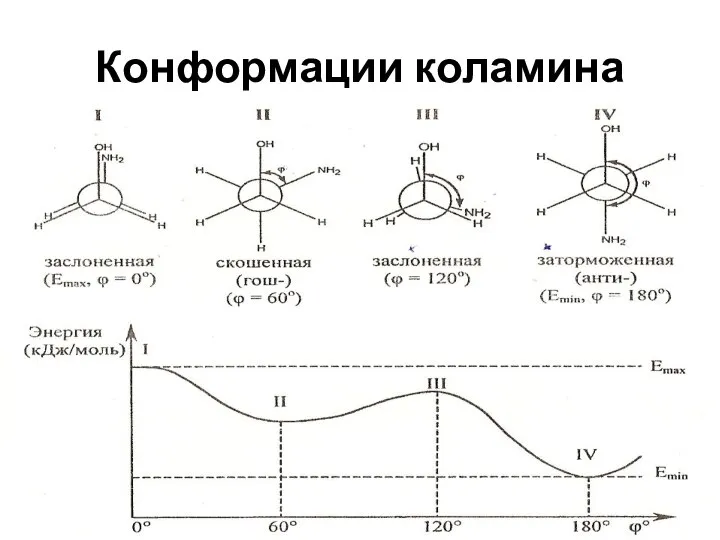
- 12. Конформации коламина
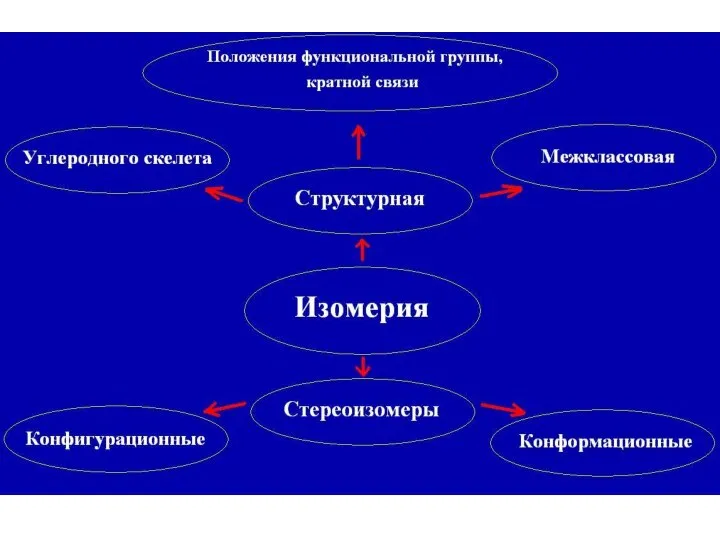
- 14. Структурная изомерия - углеродной цепи ( бутан , изобутан) положения кратных связей (бутен-1,бутен- 2) - положения
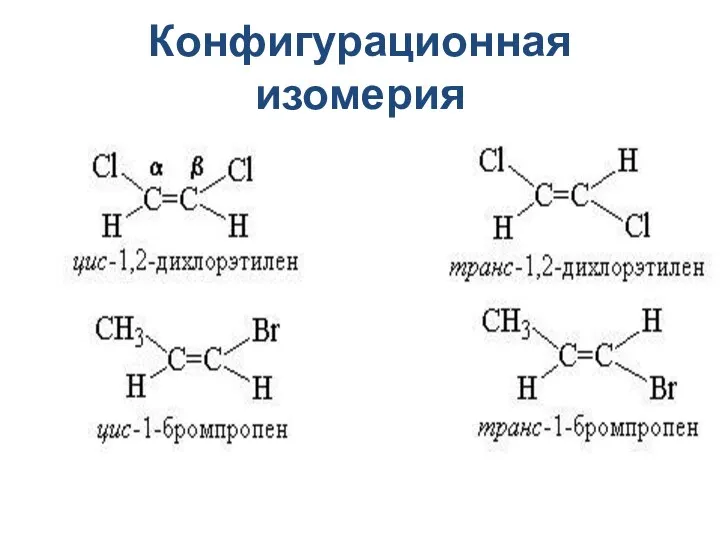
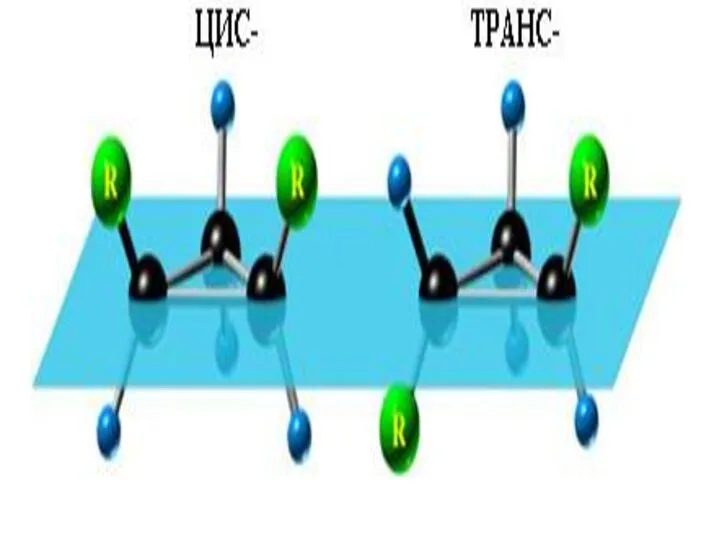
- 15. Конфигурационная изомерия
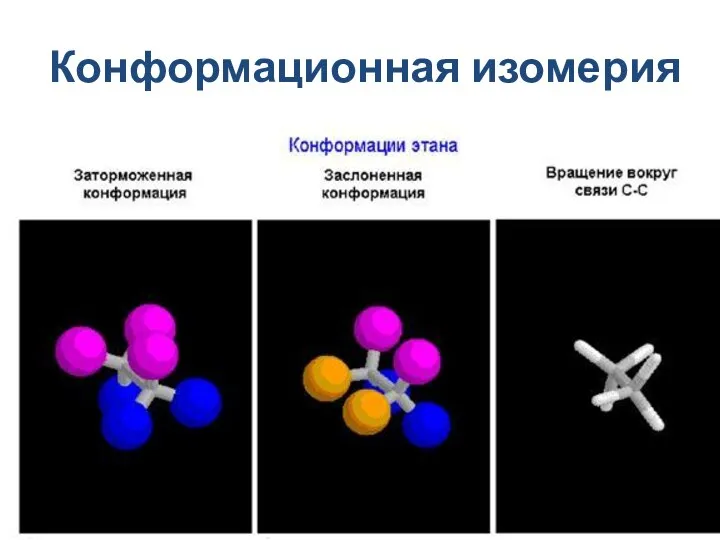
- 17. Конформационная изомерия
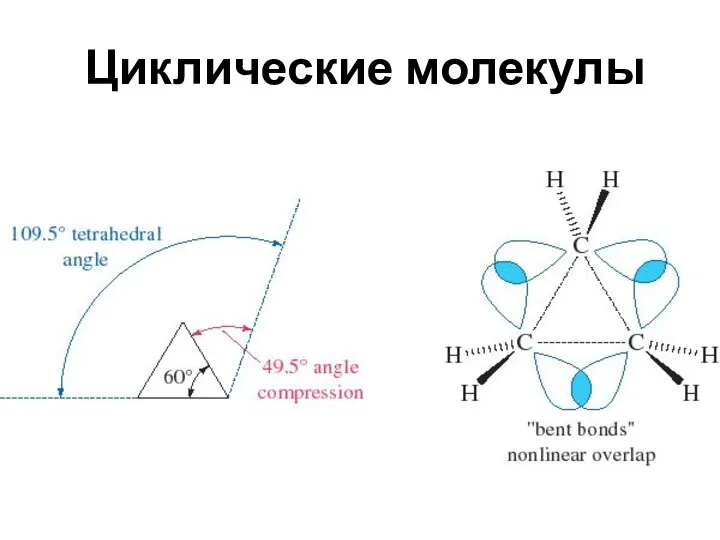
- 18. Циклические молекулы
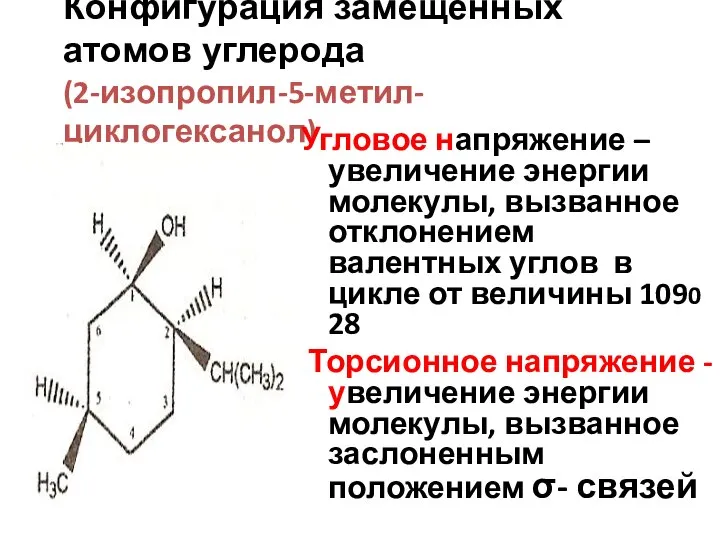
- 19. Конфигурация замещенных атомов углерода (2-изопропил-5-метил-циклогексанол) Угловое напряжение – увеличение энергии молекулы, вызванное отклонением валентных углов в
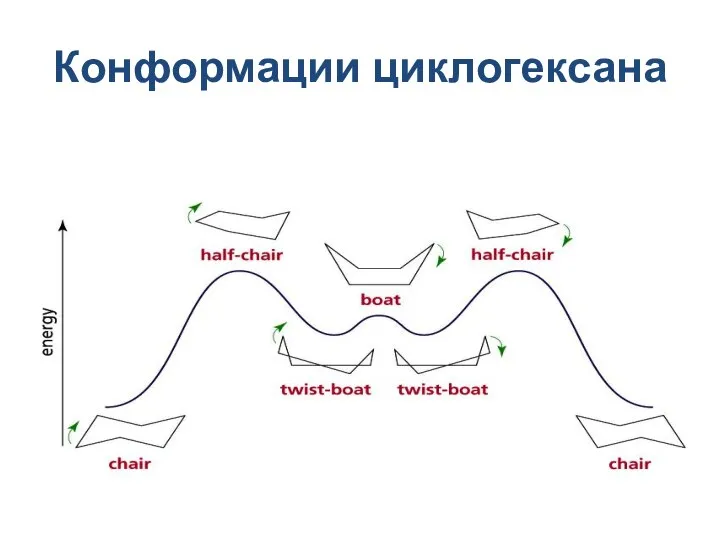
- 20. Конформации циклогексана
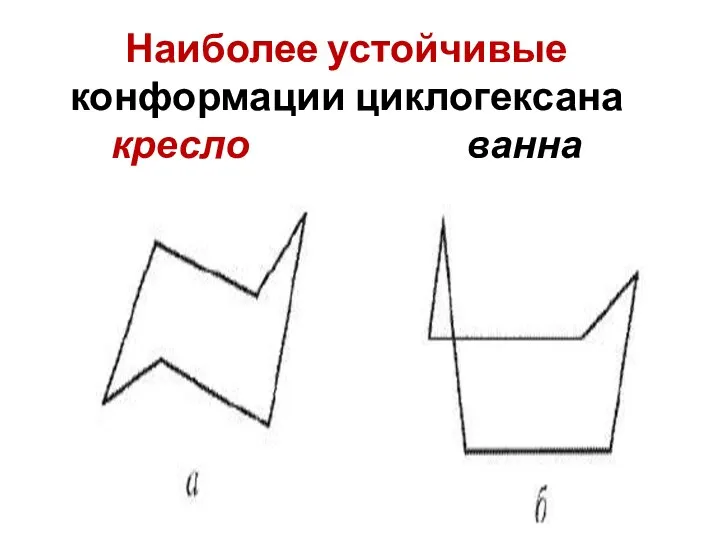
- 21. Наиболее устойчивые конформации циклогексана кресло ванна
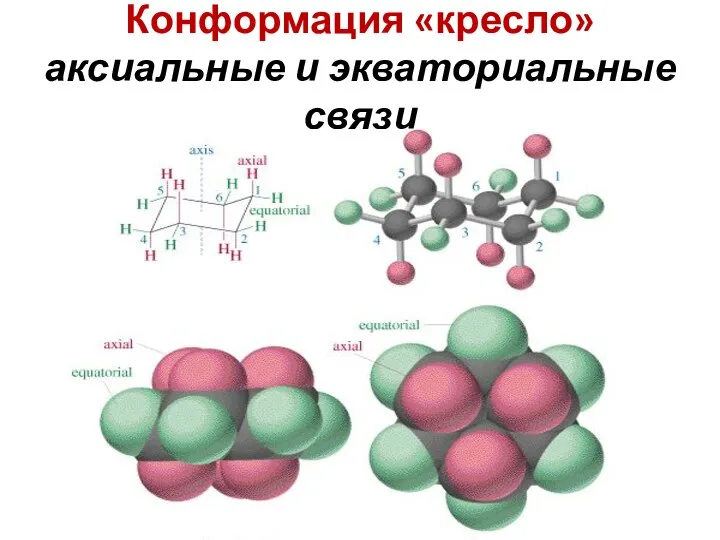
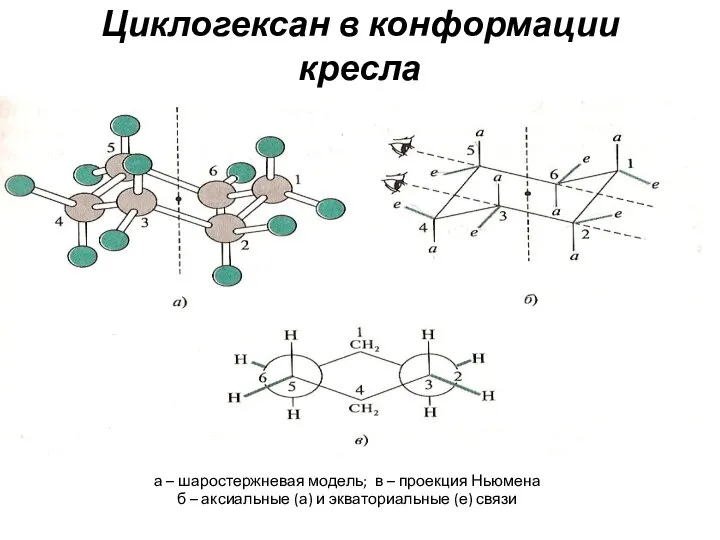
- 22. Конформация «кресло» аксиальные и экваториальные связи
- 23. Циклогексан в конформации кресла а – шаростержневая модель; в – проекция Ньюмена б – аксиальные (а)
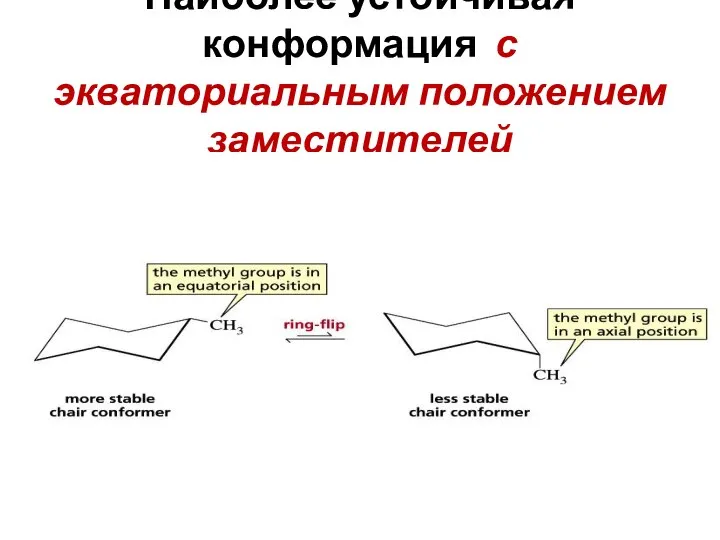
- 24. Наиболее устойчивая конформация с экваториальным положением заместителей
- 25. Сопряжение и ароматичность – энергетический фактор стабилизации молекул биологически активных соединений
- 26. Классификация двойных связей по расположению в молекуле СН2=СН-(СН2)-СН=СН2 Изолированные двойные связи СН2=С=СН2 Кумулированные двойные связи СН2=СН-СН=СН2
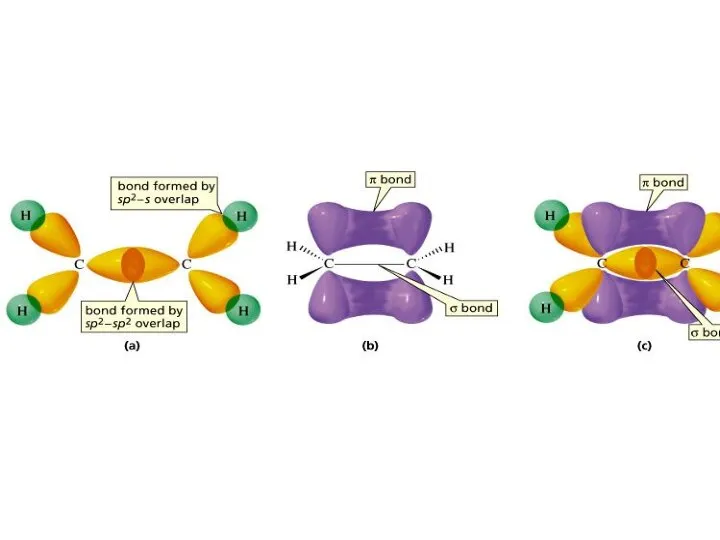
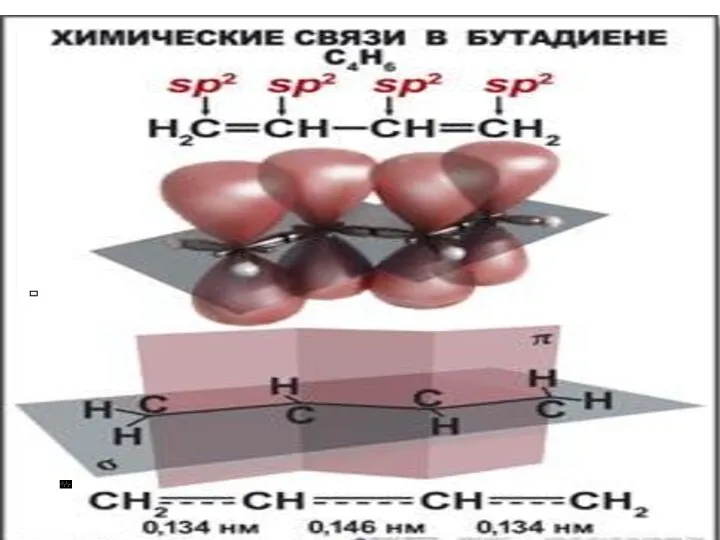
- 27. sp2 гибридизация
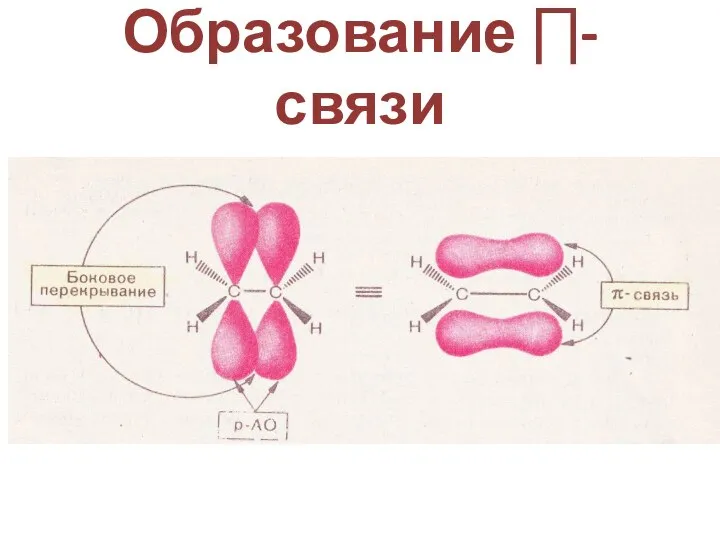
- 28. Образование ∏-связи
- 29. Сопряжение – перераспределение электронной плотности в молекуле, приводящее к выравниванию связей по длине и энергии Энергия
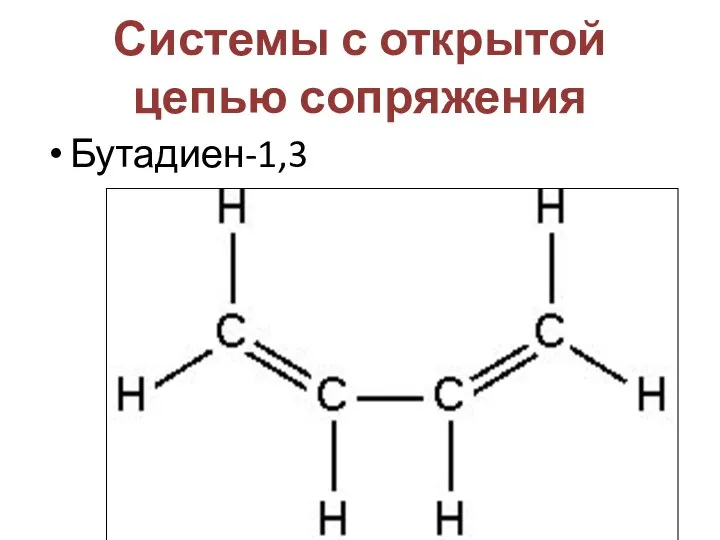
- 30. Системы с открытой цепью сопряжения Бутадиен-1,3
- 31. Алифатические системы
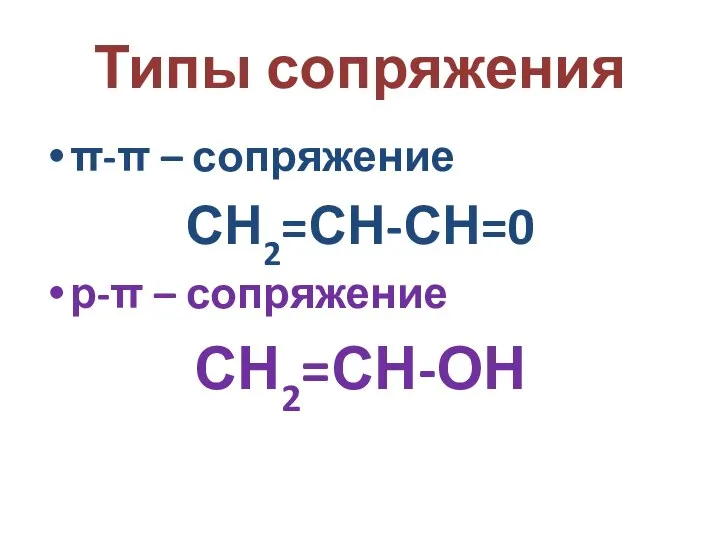
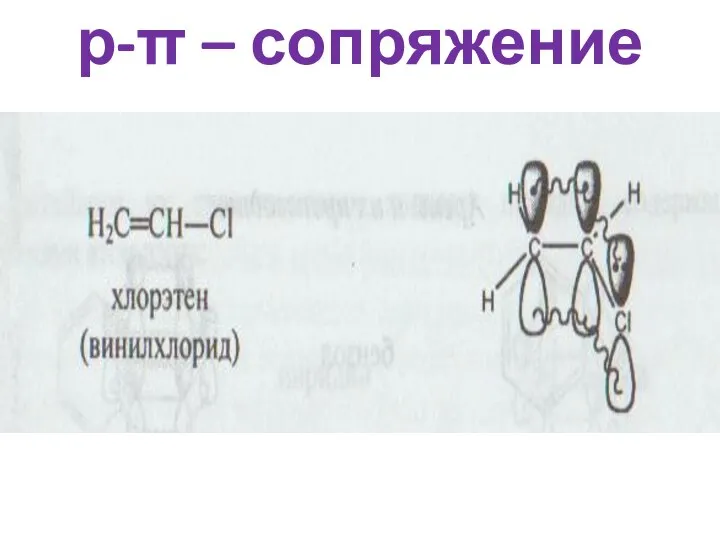
- 32. Типы сопряжения π-π – сопряжение СН2=СН-СН=0 р-π – сопряжение СН2=СН-ОН
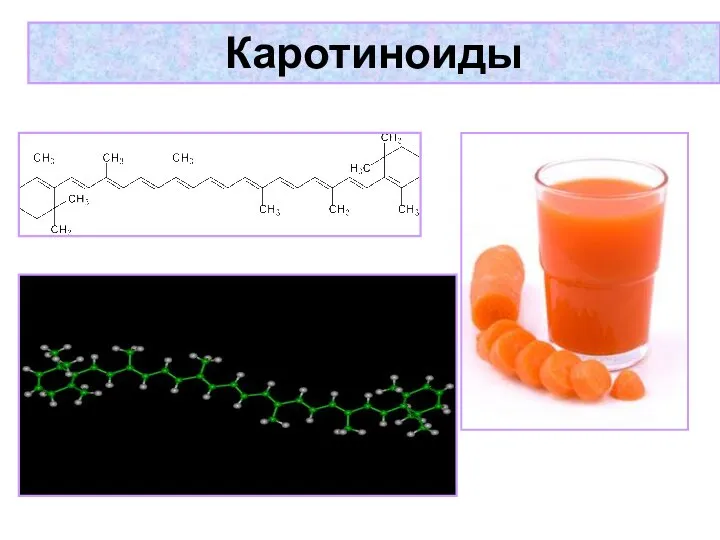
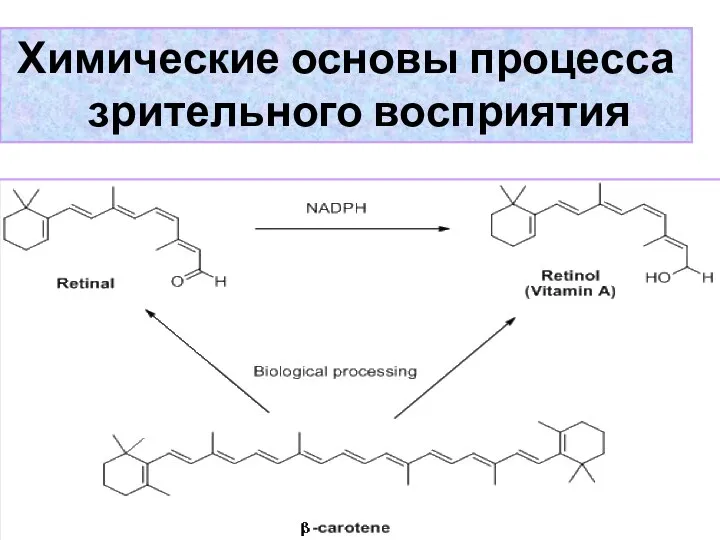
- 33. Каротиноиды
- 34. Химические основы процесса зрительного восприятия
- 35. р-π – сопряжение
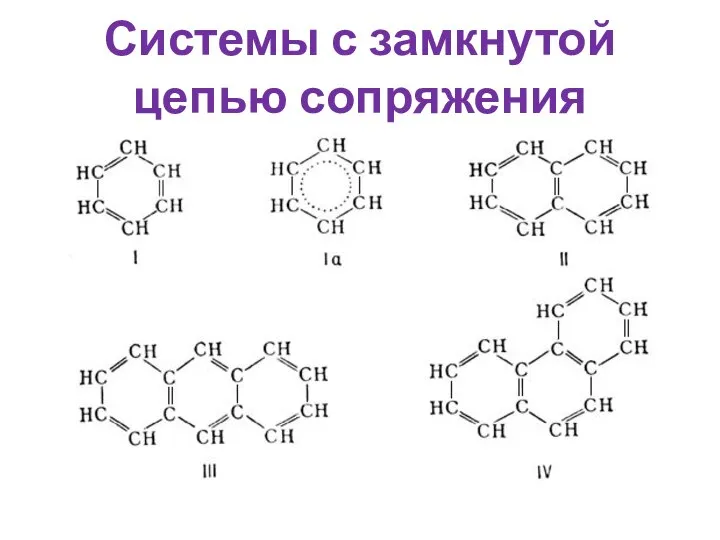
- 36. Системы с замкнутой цепью сопряжения
- 37. Есопр. Замкнутых ˃ Есопр.открытых Критерии ароматичности Плоский замкнутый цикл Замкнутая сопряженная система Число электронов в сопряженной
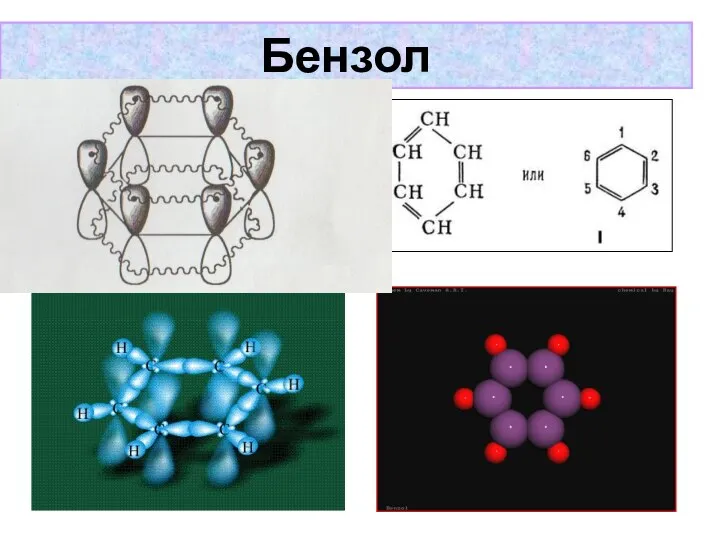
- 38. Бензол
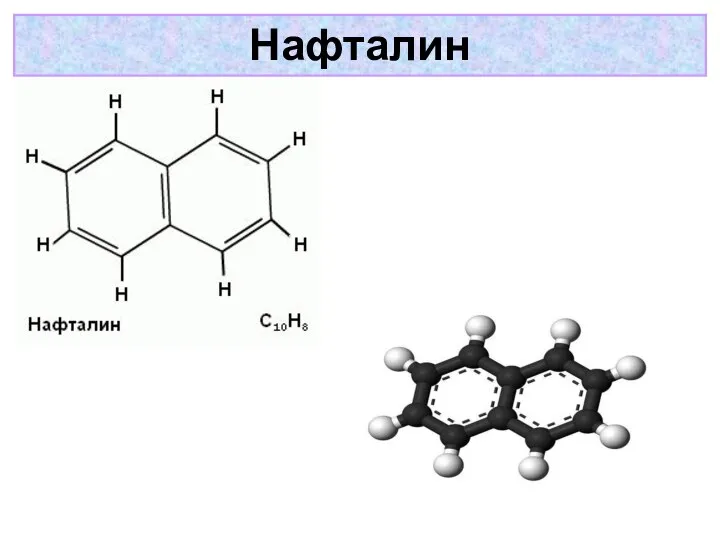
- 39. Нафталин
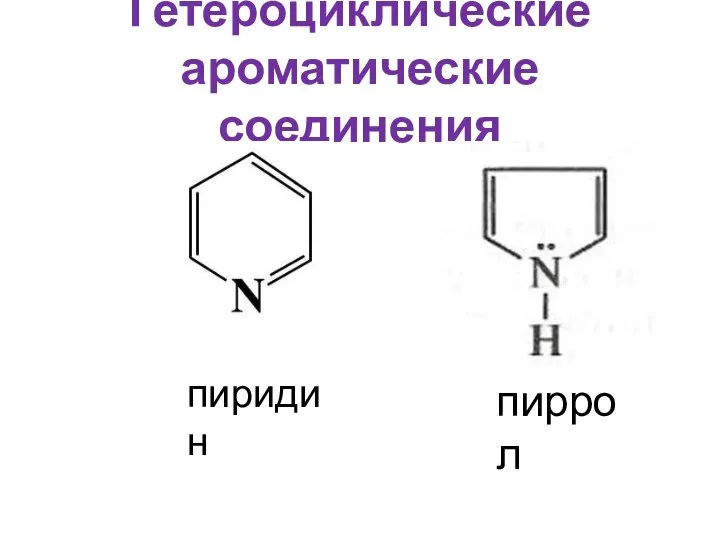
- 40. Гетероциклические ароматические соединения пиридин пиррол
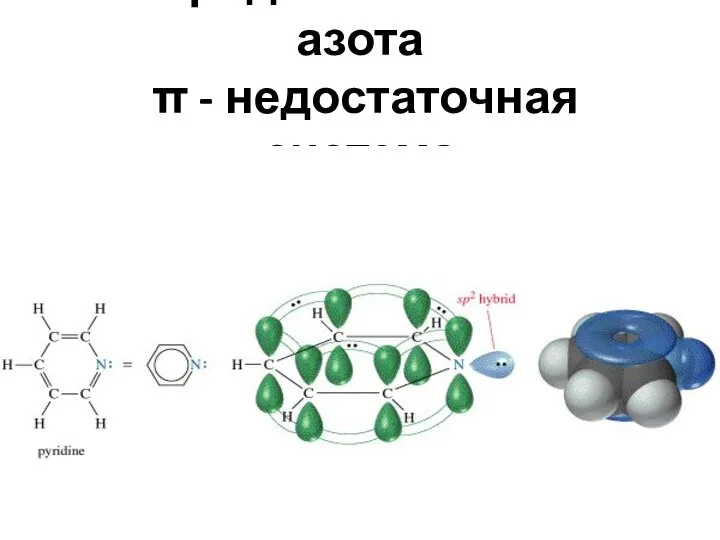
- 41. «пиридиновый» атом азота π - недостаточная система
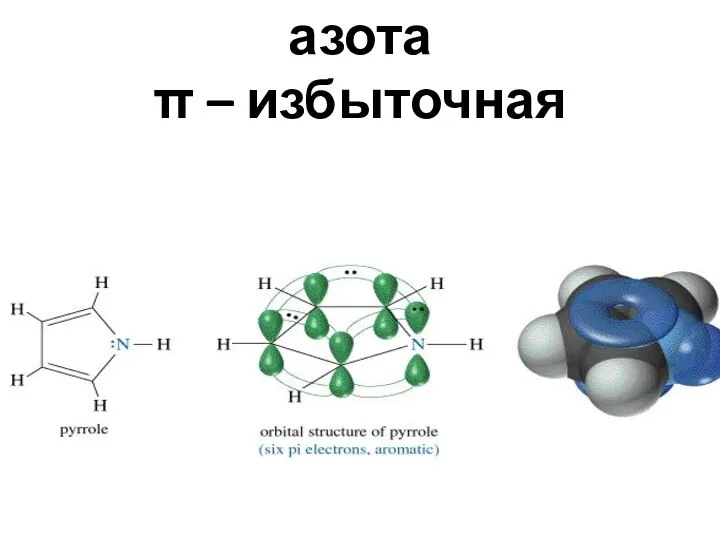
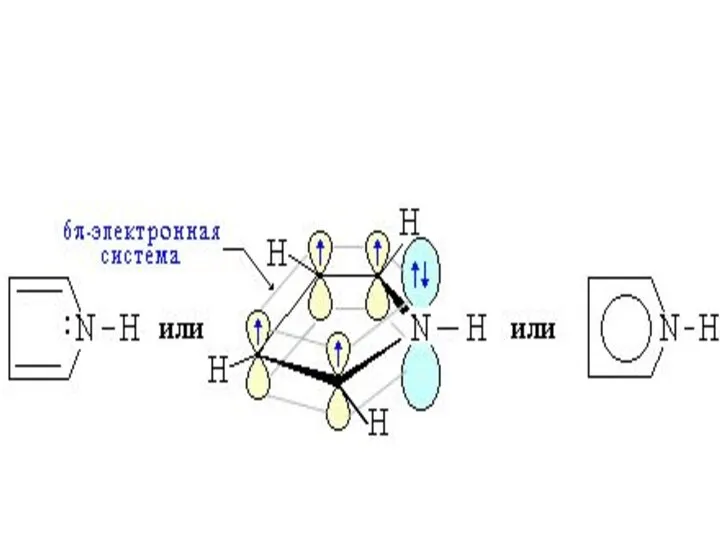
- 42. «пиррольный» атом азота π – избыточная система
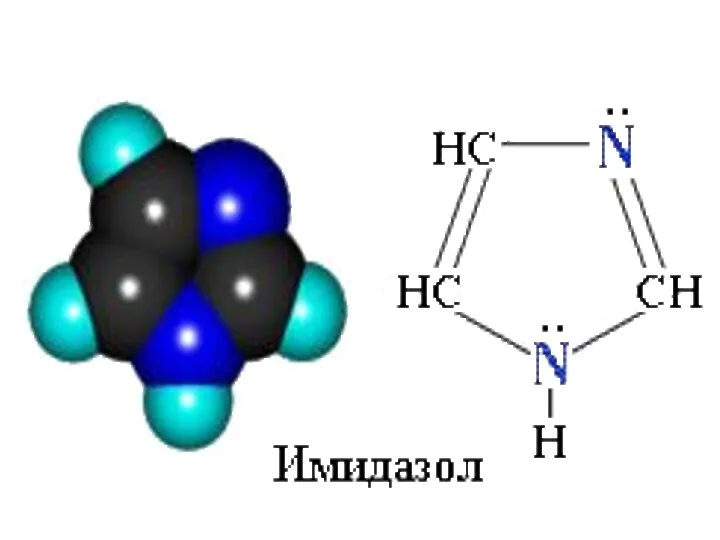
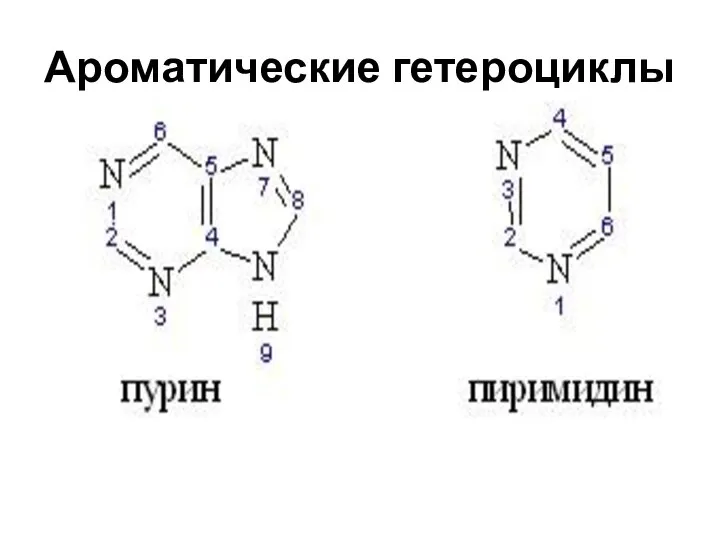
- 45. Ароматические гетероциклы
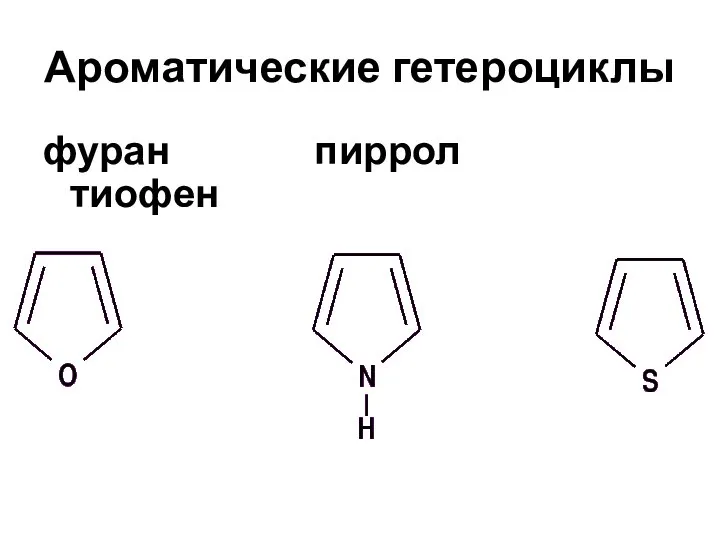
- 46. Ароматические гетероциклы фуран пиррол тиофен
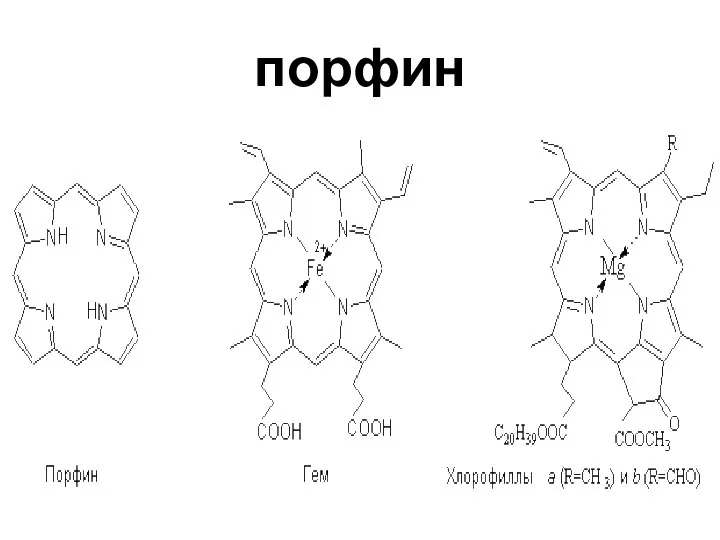
- 47. порфин
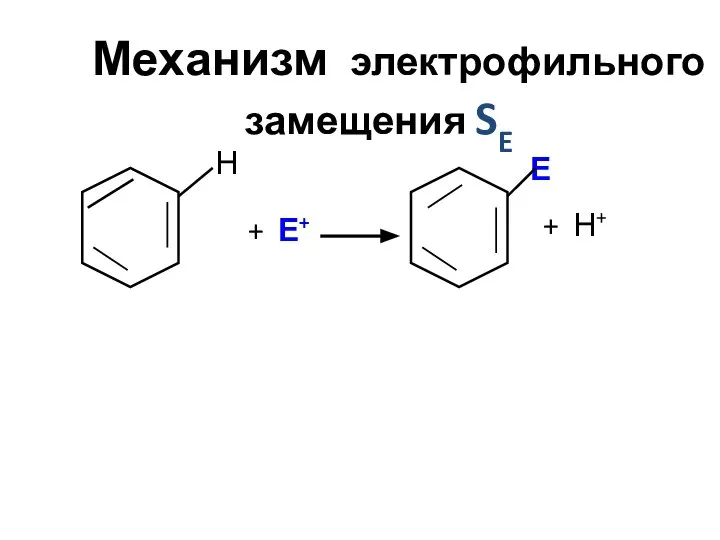
- 48. Механизм электрофильного замещения SE Н + Е+ + Н+ Е
- 49. Реакции электрофильного замещения
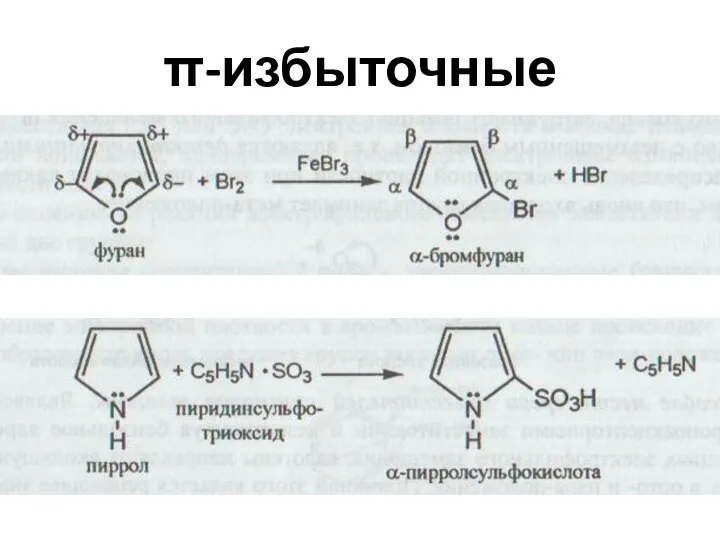
- 50. Реакционная способность ароматических гетероциклических соединений π-избыточные π-недостаточные (пиррол) (пиридин) Реакции SЕ легче Реакции SЕ труднее Е+
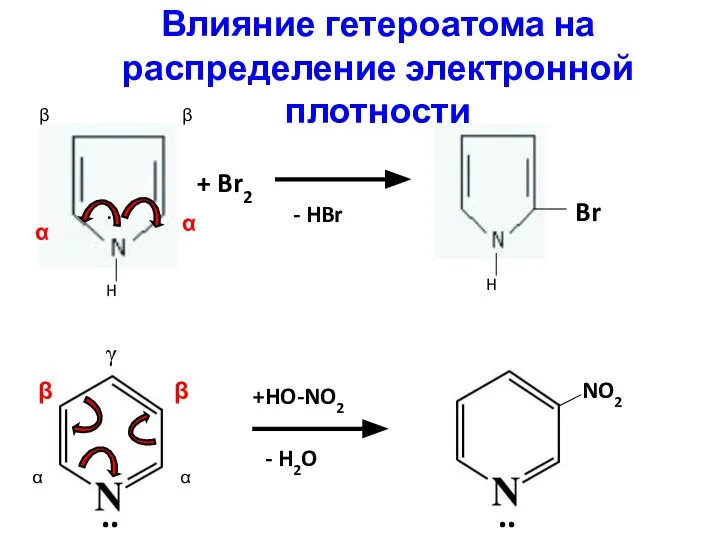
- 51. Влияние гетероатома на распределение электронной плотности + Br2 - HBr β α α β .. H
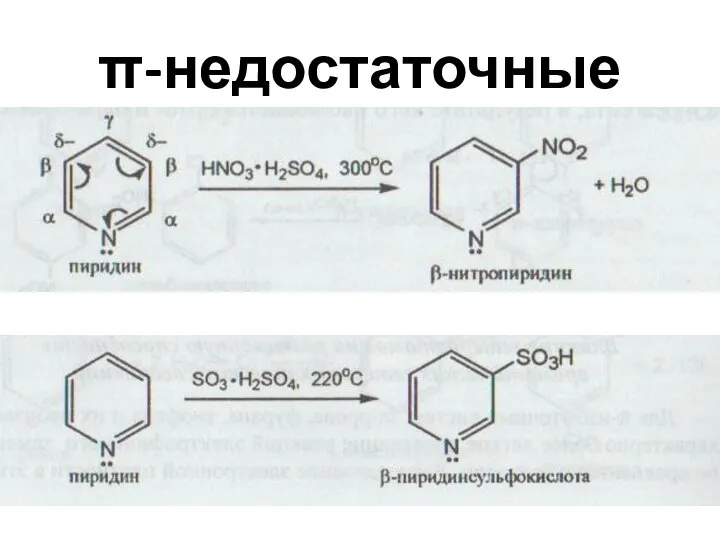
- 52. π-недостаточные
- 53. π-избыточные
- 55. Скачать презентацию







 Строение атома Подготовка к ЕГЭ
Строение атома Подготовка к ЕГЭ Презентация по Химии "Презентация Щелочные металлы" - скачать смотреть
Презентация по Химии "Презентация Щелочные металлы" - скачать смотреть  Фосфор – тіршілік пен ақыл – ой элементі
Фосфор – тіршілік пен ақыл – ой элементі Тема урока:„Строение атома” Учитель химии МБОУ СОШ №20 г.Королева Московской области Баранова Ирина Александровна
Тема урока:„Строение атома” Учитель химии МБОУ СОШ №20 г.Королева Московской области Баранова Ирина Александровна  Изготовление индикаторной бумаги
Изготовление индикаторной бумаги Тепло- и массообменные процессы при синтезе Фишера-Тропша
Тепло- и массообменные процессы при синтезе Фишера-Тропша Домашняя аптечка исследовательская работа Авторы: Полынникова Анастасия, Савина Мария учащиеся 9 «Б» класса Руководитель: Ма
Домашняя аптечка исследовательская работа Авторы: Полынникова Анастасия, Савина Мария учащиеся 9 «Б» класса Руководитель: Ма Атыраудағы химиялық өндіріс кәсіп орындары
Атыраудағы химиялық өндіріс кәсіп орындары Лужні метали Властивості, будова, застосування.
Лужні метали Властивості, будова, застосування.  Научные основы управления свойствами композиционных пленок для электролюминесцентных устройств
Научные основы управления свойствами композиционных пленок для электролюминесцентных устройств Карбоновые кислоты. Модели молекул
Карбоновые кислоты. Модели молекул Развитие учебной мотивации на уроках химии через систему урочной и внеурочной деятельности
Развитие учебной мотивации на уроках химии через систему урочной и внеурочной деятельности Фосге́н (дихлорангидрид угольной кислоты)
Фосге́н (дихлорангидрид угольной кислоты) Розв’язування розрахункових хімічних задач. Методичні рекомендації для вчителів хімії та школярів
Розв’язування розрахункових хімічних задач. Методичні рекомендації для вчителів хімії та школярів Аммиак. Образование молекулы аммиака
Аммиак. Образование молекулы аммиака Алканы
Алканы Урок-упражнение по веществам
Урок-упражнение по веществам Фенол 10 класс - Презентация по Химии
Фенол 10 класс - Презентация по Химии Все технико-экономические показатели производства определяются на основе материального баланса.
Все технико-экономические показатели производства определяются на основе материального баланса. Кристаллдық және аморфтық күй
Кристаллдық және аморфтық күй Резеңке. Каучук
Резеңке. Каучук Презентация по химии выполнили ученицы 8а класса Соболева Екатерина Кудаева Кристина Учитель Полянская И.В.
Презентация по химии выполнили ученицы 8а класса Соболева Екатерина Кудаева Кристина Учитель Полянская И.В.  Графен. Классические и квантовые низкоразмерные системы. Ковалентная химическая связь: σ- и π-электроны
Графен. Классические и квантовые низкоразмерные системы. Ковалентная химическая связь: σ- и π-электроны Приборы для измерения температуры
Приборы для измерения температуры Нуклеопротеиды. Структура и функция нуклеиновых кислот. (Лекция 4)
Нуклеопротеиды. Структура и функция нуклеиновых кислот. (Лекция 4) Электрохимические анализаторы медицинского назначения
Электрохимические анализаторы медицинского назначения Фосфорное сырье. Применение и обогащение фосфорного сырья
Фосфорное сырье. Применение и обогащение фосфорного сырья Особенности строения, реакционной способности и методы синтеза гидроксилсодержащих соединений
Особенности строения, реакционной способности и методы синтеза гидроксилсодержащих соединений