Содержание
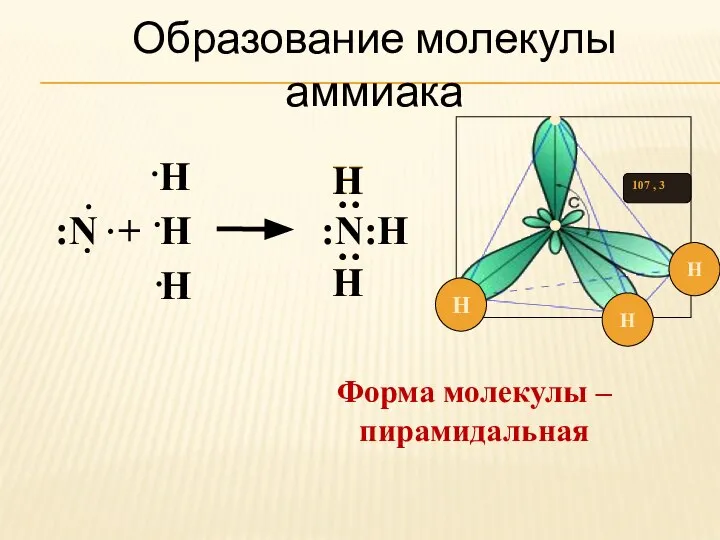
- 2. Образование молекулы аммиака :N + H :N:Н Н Н Н : : Н ⋅ ⋅ ⋅
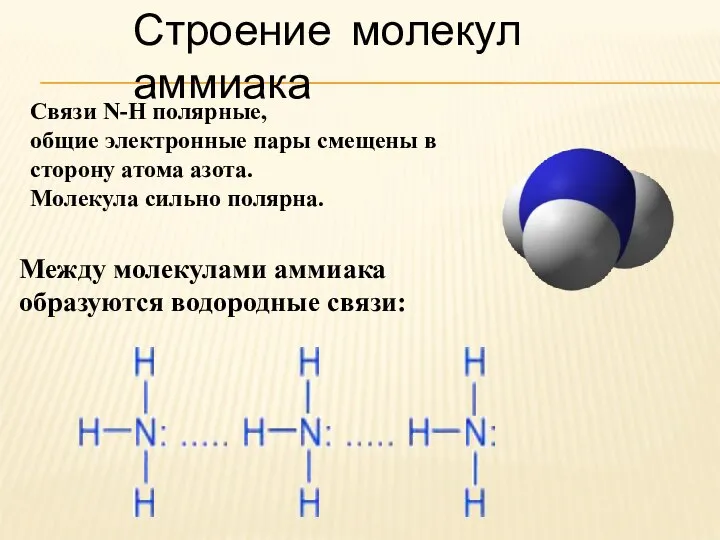
- 3. Строение молекул аммиака Между молекулами аммиака образуются водородные связи: Связи N-H полярные, общие электронные пары смещены
- 4. Физические свойства аммиака Бесцветный газ с резким запахом. Почти в два раза легче воздуха: При охлаждении
- 5. Способы получения аммиака В промышленности: N2 + 3H2 2NH3 Усл: Кат., Р, t В лаборатории: Действием
- 6. Химические свойства аммиака NH3 – низшая степень окисления азота. -3 I. Аммиак - восстановитель Реакция горения
- 7. II. Основные свойства аммиака: При растворении аммиака в воде образуется гидрат аммиака, который диссоциирует: NH3 +
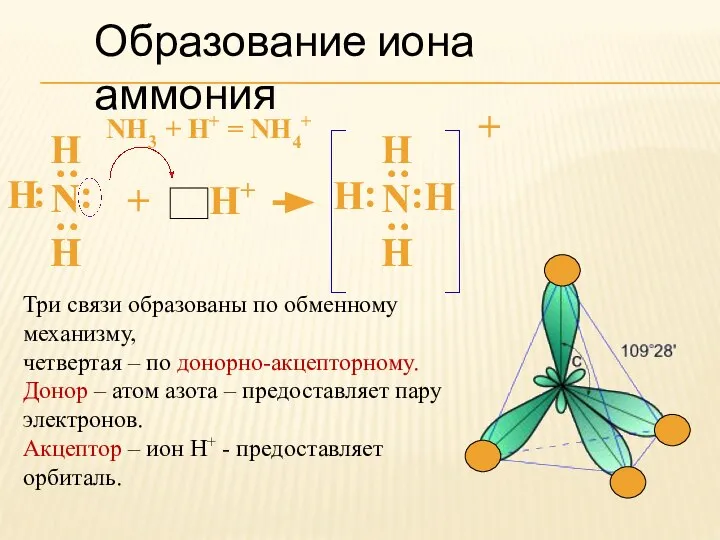
- 8. Образование иона аммония NH3 + H+ = NH4+ Н : : Н Н : : Н
- 9. Соли аммония Ион аммония по размерам и заряду близок к ионам щелочных металлов, поэтому соли аммония
- 10. Разложение солей аммония при нагревании 1. Соли летучих кислот: NH4Cl = NH3 + HCl (NH4)2CO3 =
- 11. Азотная кислота Аммиачная селитра Ca(NO3)2 Сульфат аммония (NH4)2SO4 Хлорид аммония NH4Cl Карбамид (мочевина) CO(NH2)2 Аммиачная вода
- 13. Скачать презентацию







 Анализ красителей и консервантов, входящих в состав безалкогольных газированных и негазированных напитков
Анализ красителей и консервантов, входящих в состав безалкогольных газированных и негазированных напитков Презентация по Химии "Предмет химии" - скачать смотреть
Презентация по Химии "Предмет химии" - скачать смотреть  Степень окисления. Составление формул бинарных соединений
Степень окисления. Составление формул бинарных соединений Циклічна обернено-похідна хронопотенціометрія пірокатехіну та його похідних
Циклічна обернено-похідна хронопотенціометрія пірокатехіну та його похідних Галогенидные и полигалогенидные комплексы постпереходных элементов
Галогенидные и полигалогенидные комплексы постпереходных элементов Электродные процессы, их биологическая роль и применение в медицине
Электродные процессы, их биологическая роль и применение в медицине Взаимодействие солей аммония со щелочами
Взаимодействие солей аммония со щелочами Алканы. Получение и применение алканов
Алканы. Получение и применение алканов Алкины
Алкины Химическая связь
Химическая связь Презентация по Химии "Штучні волокна" - скачать смотреть бесплатно
Презентация по Химии "Штучні волокна" - скачать смотреть бесплатно Пептиды. Белки
Пептиды. Белки Эмульсии и эмульгаторы
Эмульсии и эмульгаторы Сполуки фосфору
Сполуки фосфору Навчальний проект «Дослідження зміни концентрації CO2 у класній кімнаті під час занять»
Навчальний проект «Дослідження зміни концентрації CO2 у класній кімнаті під час занять» Производные пирролидина, пиразолона и пиразолидиндиона: их свойства, анализ, хранение, применение
Производные пирролидина, пиразолона и пиразолидиндиона: их свойства, анализ, хранение, применение Витамины и авитаминоз - презентация_
Витамины и авитаминоз - презентация_ Железо. Строение атома, физические и химические свойства простого вещества
Железо. Строение атома, физические и химические свойства простого вещества Электродные материалы для электрохимических систем
Электродные материалы для электрохимических систем Комплексті қосылыстар
Комплексті қосылыстар Абсолютное первенство по химии
Абсолютное первенство по химии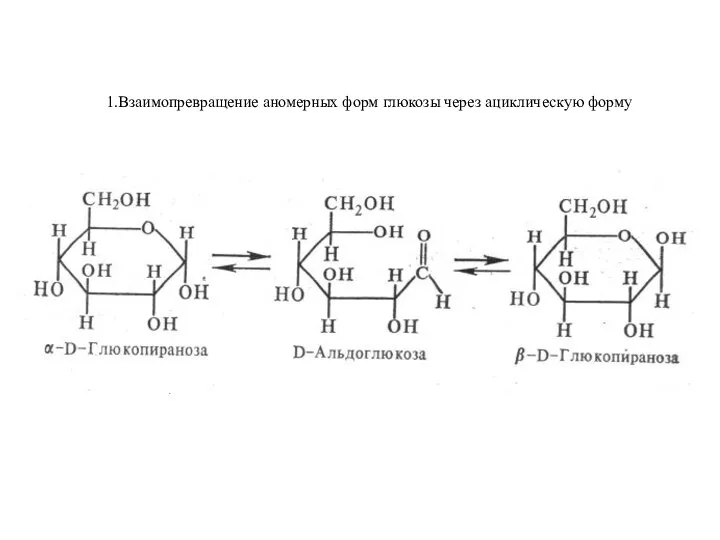 Взаимопревращение аномерных форм глюкозы через ациклическую форму
Взаимопревращение аномерных форм глюкозы через ациклическую форму Биологически важные ароматические и гетероциклические соединения
Биологически важные ароматические и гетероциклические соединения Химическая связь
Химическая связь Полимерные материалы и изделия
Полимерные материалы и изделия Классификация дисперсных систем. Электрокинетические свойства и устойчивость коллоидных растворов. (Лекция 8)
Классификация дисперсных систем. Электрокинетические свойства и устойчивость коллоидных растворов. (Лекция 8) Хром и его соединения
Хром и его соединения Липиды. Классификация
Липиды. Классификация