Основные правила заполнения электронами электронных уровней
На одной орбитали не может находится
одновременно больше двух электронов (Правило Паули)
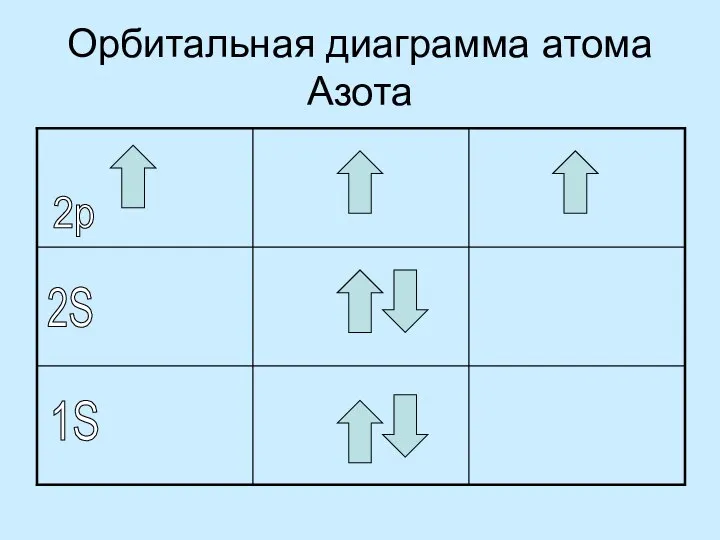
Электроны заполняют свои орбитали вначале по одиночке, а только потом образуют пары (Правило Гунда)
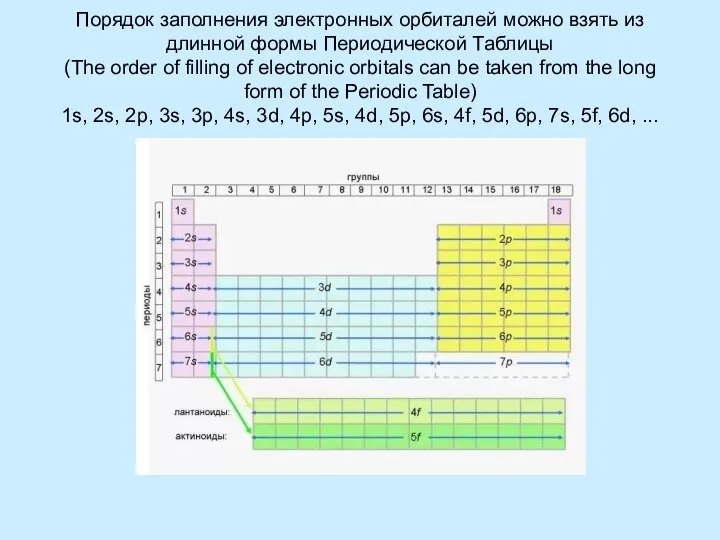
Принцип минимума энергии: при заполнении электронных оболочек в первую очередь заполняются оболочки с минимальной энергией (ближайшие к ядру уровни и подуровни)
Правило «октета - дублета»Все атомы стремятся к завершению своего внешнего уровня до двух или восьми электронов.
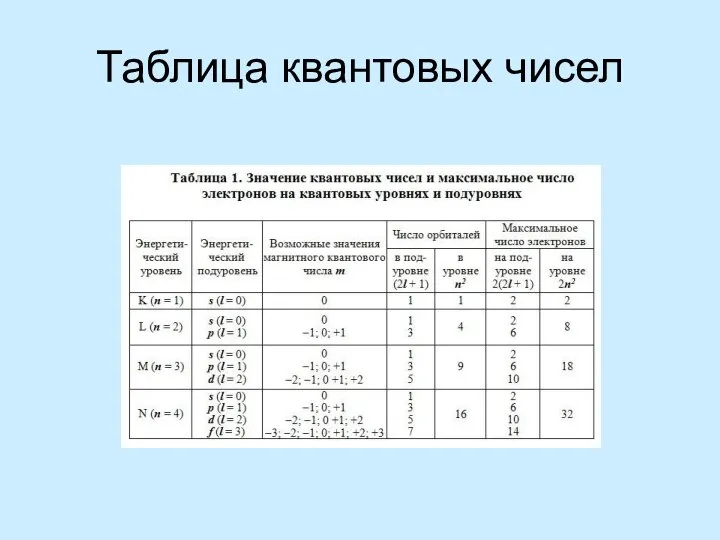
Правило Клечковского – Меделунга. Заполнение электронами орбиталей в атоме происходит в порядке возрастания суммы главногоПравило Клечковского – Меделунга. Заполнение электронами орбиталей в атоме происходит в порядке возрастания суммы главного и орбитальногоПравило Клечковского – Меделунга. Заполнение электронами орбиталей в атоме происходит в порядке возрастания суммы главного и орбитального квантовых чисел . При одинаковой сумме раньше заполняется орбиталь с меньшим значением .
On one orbital is not at the same time more than two electrons (Pauli Rule)
Electrons fill their orbitals in the beginning alone and then form pairs (Rule Gund)
The principle of minimum energy: when filling the electron shells first shell filled with a minimum of energy (closest to nucleus levels and sub-levels)
The rule of "octet - doublet"All the atoms tend to complete their outer level to two or eight electrons.
The Rule Kleczkowska – Madelung. The filling of the electron orbitals in the atom occurs in ascending order of the sum of the main and orbital quantum numbers . For the same amount ahead is filled orbital with a lower value .












 Полиметилметакрилат
Полиметилметакрилат Алканы «Гексан»
Алканы «Гексан» Кислородсодержащие классы органических соединений. Гидроксисоединения. Карбонильные соединения. (Лекция 3)
Кислородсодержащие классы органических соединений. Гидроксисоединения. Карбонильные соединения. (Лекция 3) Презентация по Химии "Теория Витализма" - скачать смотреть бесплатно
Презентация по Химии "Теория Витализма" - скачать смотреть бесплатно Каталитический риформинг
Каталитический риформинг Кислоты в природе: состав, классификация, значение
Кислоты в природе: состав, классификация, значение Основные понятия и законы химии
Основные понятия и законы химии Применение спиртов
Применение спиртов Решение заданий С1 вариантов ЕГЭ учитель химии – Новикова Е.В. Окислительно-восстановительные реакции
Решение заданий С1 вариантов ЕГЭ учитель химии – Новикова Е.В. Окислительно-восстановительные реакции Полимеры. Классификация, применение
Полимеры. Классификация, применение Стекло — твердое неорганическое вещество
Стекло — твердое неорганическое вещество Строение атома. Опыты Резерфорда
Строение атома. Опыты Резерфорда Массовая доля элемента в веществе Задачи урока: 1. Познакомиться с понятием «массовая доля элемента в веществе» 2. Научиться рассч
Массовая доля элемента в веществе Задачи урока: 1. Познакомиться с понятием «массовая доля элемента в веществе» 2. Научиться рассч Полімери. Їх властивості та застосування
Полімери. Їх властивості та застосування Биоэнергетика. Современное представление о биологическом окислении
Биоэнергетика. Современное представление о биологическом окислении Выделение урана из растворов (пульп)
Выделение урана из растворов (пульп) Классификация полимеров по способу получения
Классификация полимеров по способу получения Нарушения окисления жирных кислот
Нарушения окисления жирных кислот Хімія запаху і смаку
Хімія запаху і смаку Свойства идеального газа на примере воздуха
Свойства идеального газа на примере воздуха Пантотен қышқылы (В3 дәрумені)
Пантотен қышқылы (В3 дәрумені) Геология и геохимия нефти и газа
Геология и геохимия нефти и газа Етери. Ізомерія та номенклатура
Етери. Ізомерія та номенклатура Особенности строения, реакционной способности и методы синтеза гидроксилсодержащих соединений
Особенности строения, реакционной способности и методы синтеза гидроксилсодержащих соединений Оксид кальция (СаО)
Оксид кальция (СаО) Radioimmunoassay& enzyme linked immunosorbent
Radioimmunoassay& enzyme linked immunosorbent Технология кварцевого стекла
Технология кварцевого стекла Чистые вещества и смеси
Чистые вещества и смеси