Содержание
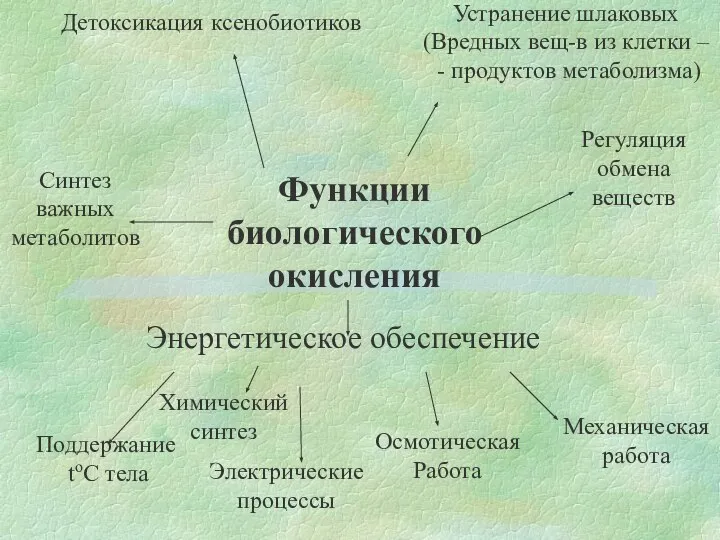
- 2. Детоксикация ксенобиотиков Регуляция обмена веществ Устранение шлаковых (Вредных вещ-в из клетки – - продуктов метаболизма) Синтез
- 3. Способы передачи электронов 1. Прямой перенос электронов Fe2+ + Cu2+ ----- Fe 3+ + Cu+ 2.
- 4. I. Оксидазный: в митохондриях II. Пероксидазный : в макрофагах, фагоцитах, лейкоцитах, гистиоцитах - флавопротеиды (ФМН, ФАД)
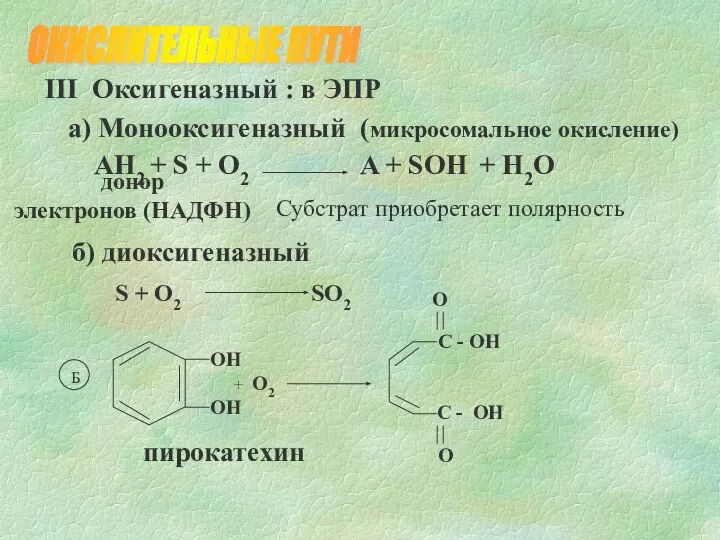
- 5. III Оксигеназный : в ЭПР а) Монооксигеназный (микросомальное окисление) б) диоксигеназный S + O2 SO2 Субстрат
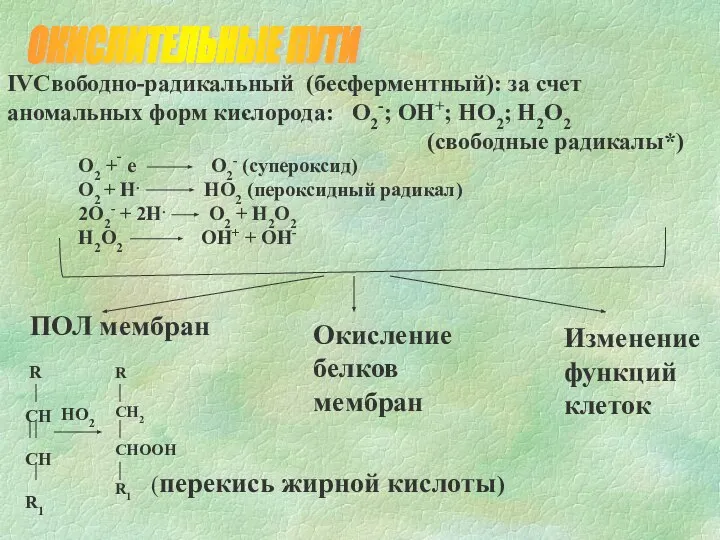
- 6. ПОЛ мембран Окисление белков мембран Изменение функций клеток ОКИСЛИТЕЛЬНЫЕ ПУТИ
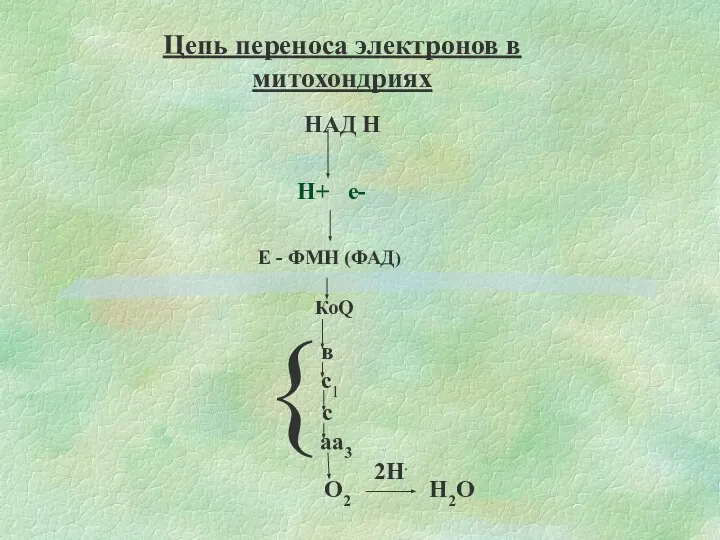
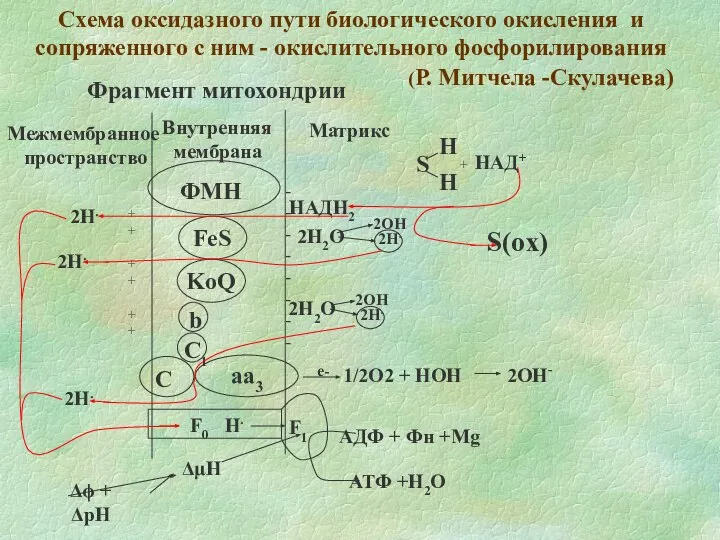
- 7. НАД Н Н+ е- Е - ФМН (ФАД) О2 2Н. Н2О Цепь переноса электронов в митохондриях
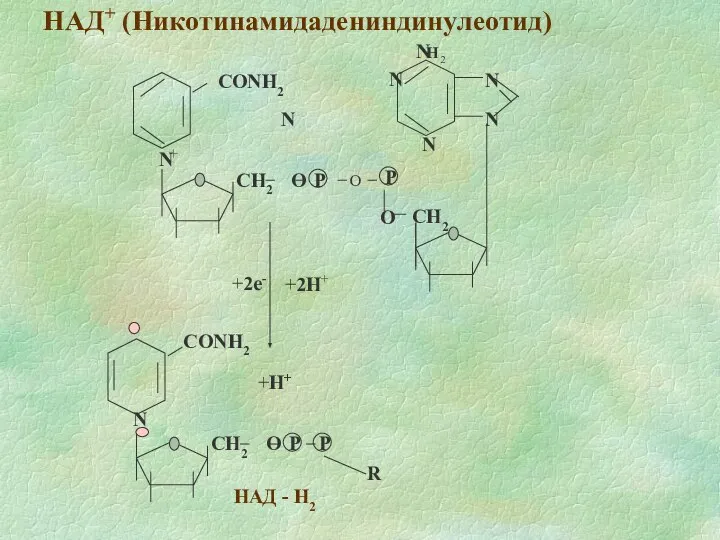
- 8. НАД+ (Никотинамидадениндинулеотид) +2e- +2H+
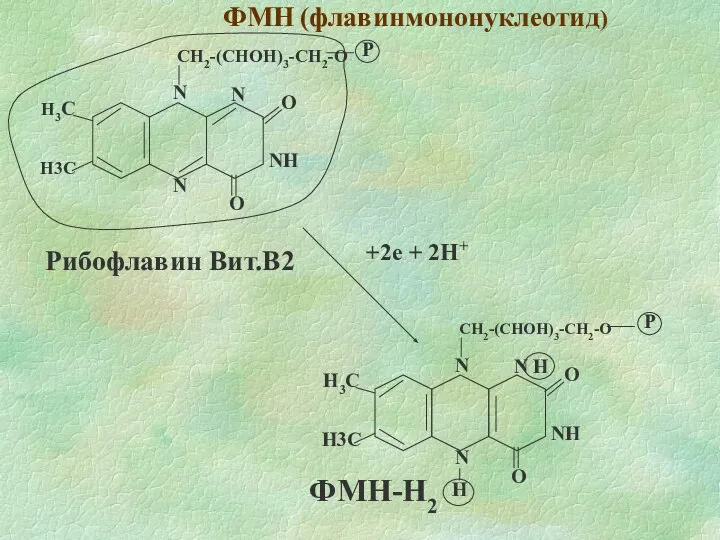
- 9. ФМН (флавинмононуклеотид) Рибофлавин Вит.B2 +2e + 2H+
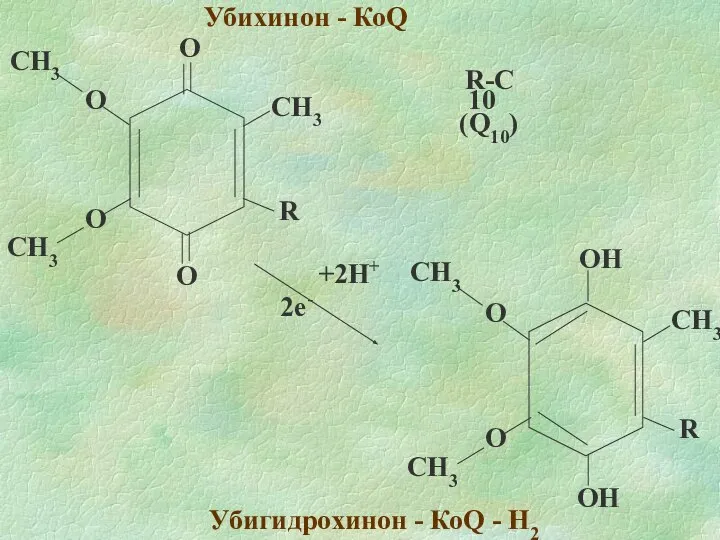
- 10. Убихинон - КоQ Убигидрохинон - КоQ - H2 2e- +2H+
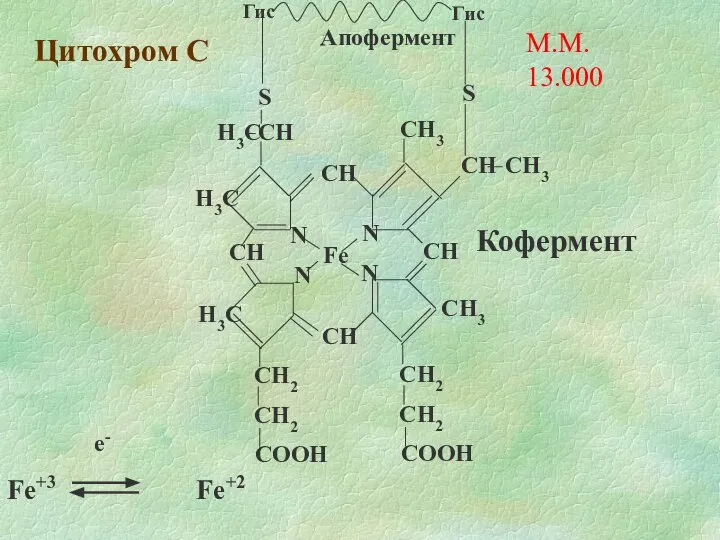
- 11. Цитохром С М.М. 13.000 е-
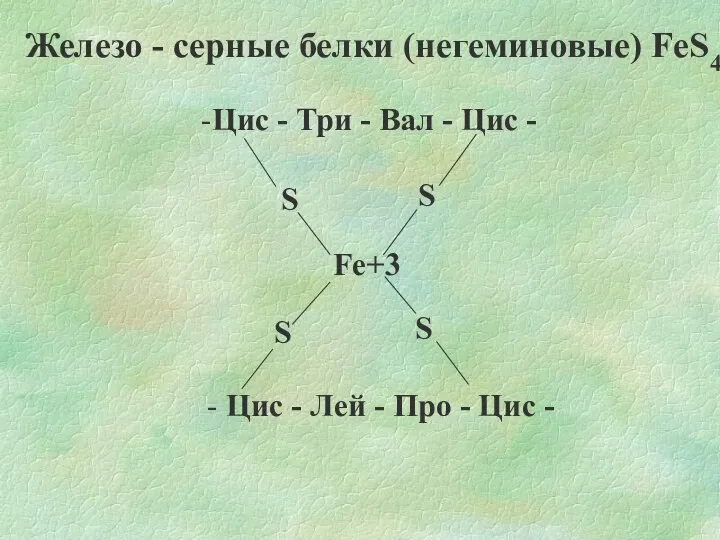
- 12. Железо - серные белки (негеминовые) FeS4
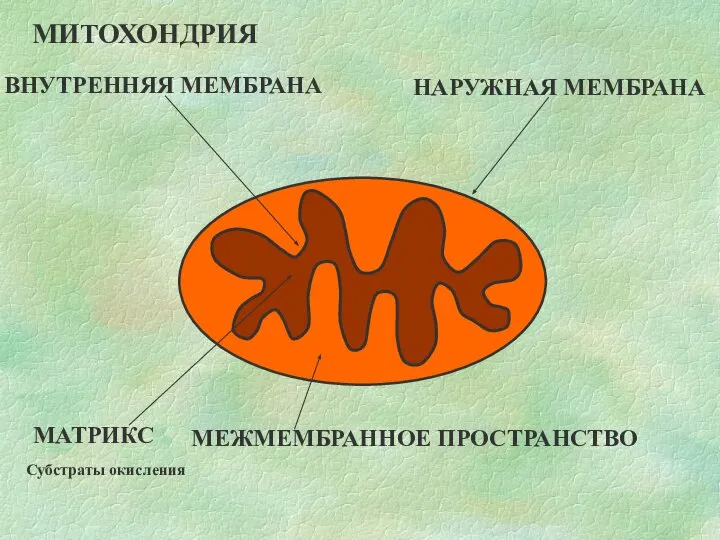
- 13. МАТРИКС МЕЖМЕМБРАННОЕ ПРОСТРАНСТВО ВНУТРЕННЯЯ МЕМБРАНА НАРУЖНАЯ МЕМБРАНА МИТОХОНДРИЯ Субстраты окисления
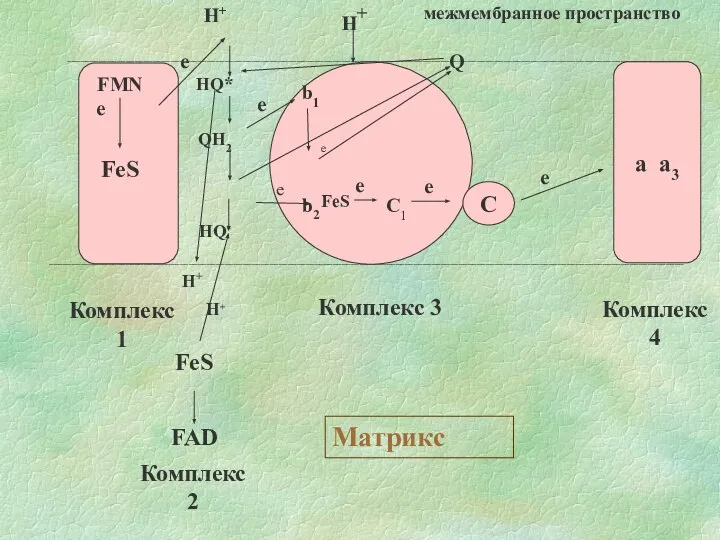
- 14. FMN е FeS H+ HQ* QH2 HQ* H+ b1 e b2 FeS C1 Q C a
- 15. Разность Е0 стандартных потенциалов от НАДН2/НАД к паре Н2О/1/2О2 равна [0,82 V - ( - 0,32V)]
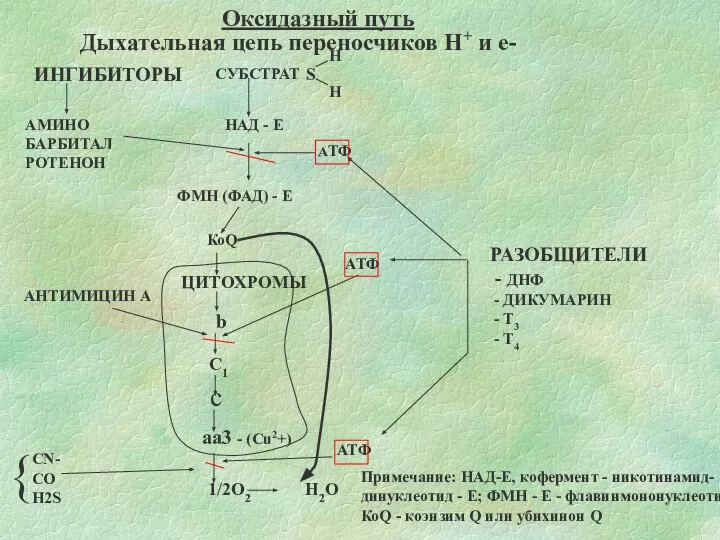
- 16. Оксидазный путь Дыхательная цепь переносчиков Н+ и е- ИНГИБИТОРЫ АМИНО БАРБИТАЛ РОТЕНОН НАД - Е АТФ
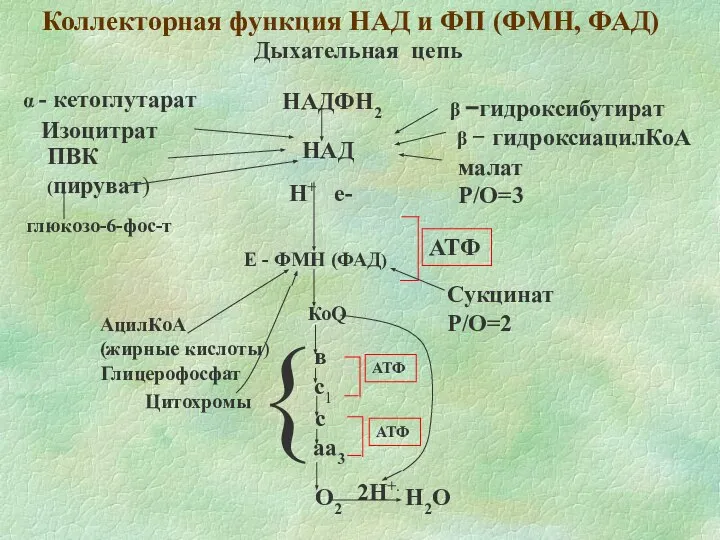
- 17. Коллекторная функция НАД и ФП (ФМН, ФАД) О2 Н2О Дыхательная цепь НАДФН2 НАД Н+ е- Е
- 18. СУБСТРАТНОЕ ФОСФОРИЛИРОВАНИЕ (образование АТФ из высокоэнергетических соединений) СН2 С O ~ Р СООН ФЕП (ФОСФОЕНОЛ- ПИРУВАТ)
- 19. W + АДФ + Фнеорг АТФ + Н2О 1936 г. проф. Энгельгардт В.Н. ФОСФОРИЛИРОВАНИЕ АДФ СОПРЯЖЕНО
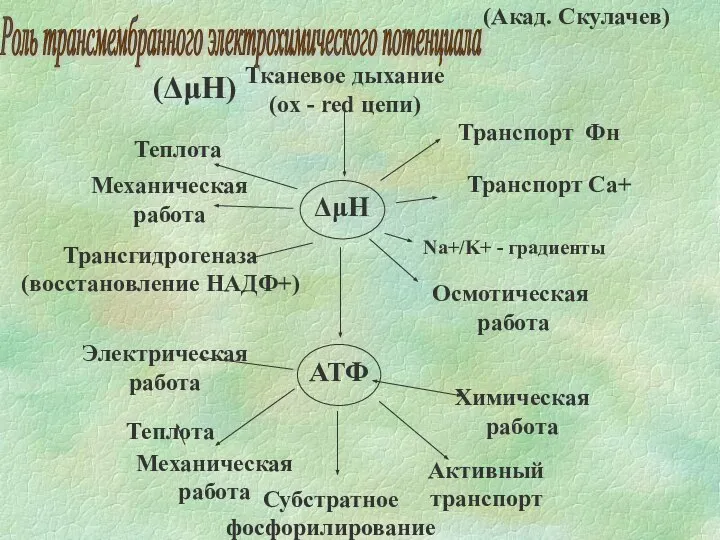
- 20. Тканевое дыхание (ox - red цепи) Роль трансмембранного электрохимического потенциала (ΔμH) (Акад. Скулачев)
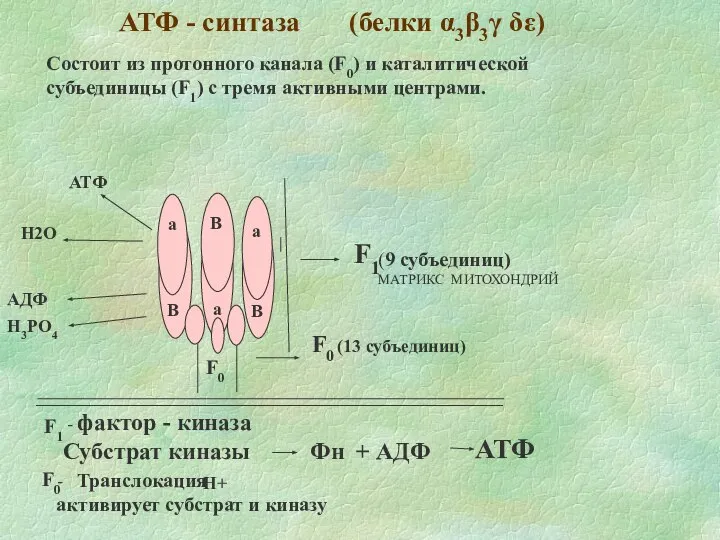
- 22. АТФ - синтаза (белки α3β3γ δε) а B B B a a АТФ H2O АДФ H3PO4
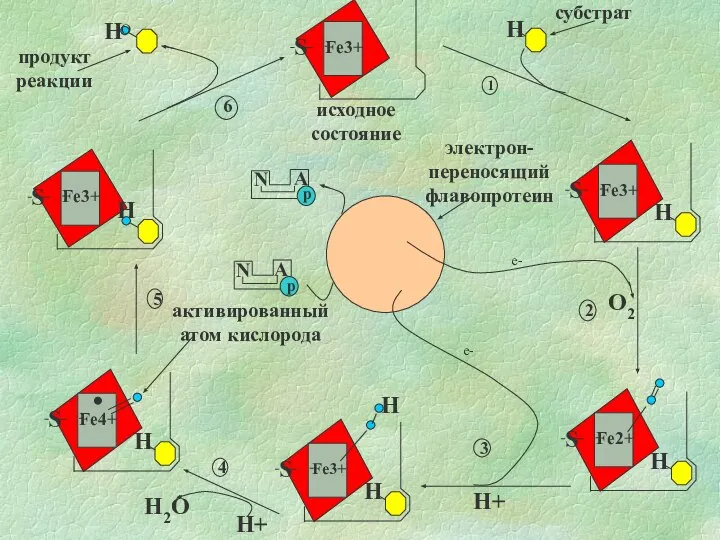
- 23. Микросомальное окисление SН+НАДФH2 + O2 SOH + H2O + НАДФ 1. НАДФH2 ФАД ФМН Fe3+ (P450)
- 24. O2 H H+ H Fe3+ S Fe3+ S H O e- e- H+ H2O H 1
- 26. Скачать презентацию






 СОЕДИНЕНИЯ ЩЕЛОЧНОЗЕМЕЛЬНЫХ МЕТАЛЛОВ
СОЕДИНЕНИЯ ЩЕЛОЧНОЗЕМЕЛЬНЫХ МЕТАЛЛОВ Аттестационная работа. Программа кружка по химии «Юный химик»
Аттестационная работа. Программа кружка по химии «Юный химик» Электронное строение атома. Периодический закон
Электронное строение атома. Периодический закон Кетоны
Кетоны Point defects and diffusion
Point defects and diffusion Презентация по Химии "Презентация Химический состав растений" - скачать смотреть
Презентация по Химии "Презентация Химический состав растений" - скачать смотреть  Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Продолжение лекции «Химическая связь»
Продолжение лекции «Химическая связь» Коллоидно-химические свойства и методы определения дисперсности НДС. Лекция 3
Коллоидно-химические свойства и методы определения дисперсности НДС. Лекция 3 Обмен липидов
Обмен липидов Неорганические вещества, входящие в состав клетки
Неорганические вещества, входящие в состав клетки Биогенные элементы периодической системы
Биогенные элементы периодической системы Опыты в домашних условиях
Опыты в домашних условиях Элементы подгруппы углерода
Элементы подгруппы углерода Химические реакции. Изменение степеней окисления
Химические реакции. Изменение степеней окисления Виды химической связи
Виды химической связи Характеристика азота и фосфора. Свойства азота
Характеристика азота и фосфора. Свойства азота Температурная зависимость скорости химической реакции
Температурная зависимость скорости химической реакции Решение задач на избыток и недостаток
Решение задач на избыток и недостаток Углерод. 9 класс
Углерод. 9 класс Применение газовых разрядов в быту Подготовила: ученица 9-А класса СООШ №18 Кальченко Елена
Применение газовых разрядов в быту Подготовила: ученица 9-А класса СООШ №18 Кальченко Елена  Одноатомные спирты
Одноатомные спирты Количество вещества
Количество вещества Классификация органических реакций в органической химии
Классификация органических реакций в органической химии Игра по химии Разработала учитель химии МОУ «Яльчикская СОШ» Левая В.Н.
Игра по химии Разработала учитель химии МОУ «Яльчикская СОШ» Левая В.Н. Пигменті в реставрации декоративно-прикладного искусства
Пигменті в реставрации декоративно-прикладного искусства БЫТОВАЯ ХИМИЯ. МОЮЩИЕ СРЕДСТВА МОУ СОШ № 95 Советского района городского округа г.Уфа
БЫТОВАЯ ХИМИЯ. МОЮЩИЕ СРЕДСТВА МОУ СОШ № 95 Советского района городского округа г.Уфа Сапропель және бактериалды тыңайтқыштар және қордалар
Сапропель және бактериалды тыңайтқыштар және қордалар