Содержание
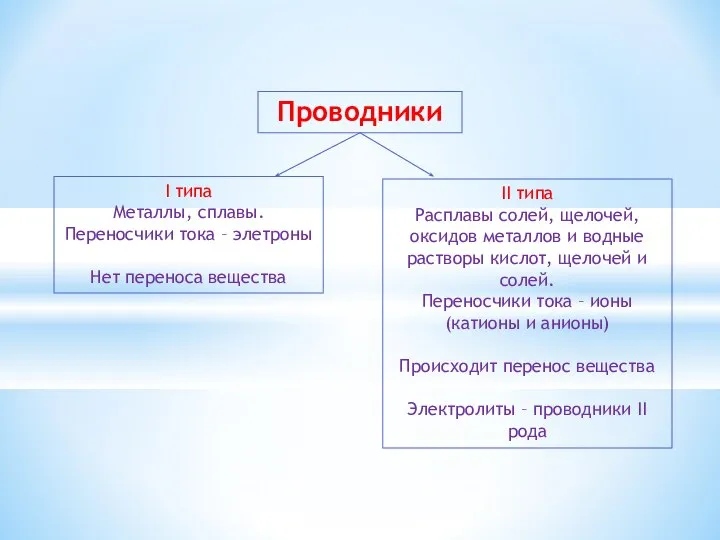
- 2. Проводники I типа Металлы, сплавы. Переносчики тока – элетроны Нет переноса вещества II типа Расплавы солей,
- 3. Сила тока, напряжение и сопротивление проводников связано уравнением: I = U/R
- 4. Электропроводность – способность вещества проводить электрический ток L = 1/R [ом-1] Зависит от: 1) природы электролита
- 5. Электропроводность Удельная χ = 1/ρ [ом-1⋅м-1] χ-каппа Молярная λ = 1000 χ /C [ом-1⋅м2⋅моль-1] λ -
- 6. Известно, что: R = ρ ⋅ l/S, или ρ = R⋅S / l, иначе L =
- 7. Удельная электропроводность – электропроводность раствора, заключенного между 2-мя параллельными электродами площадью 1м2 и расположенными на расстоянии
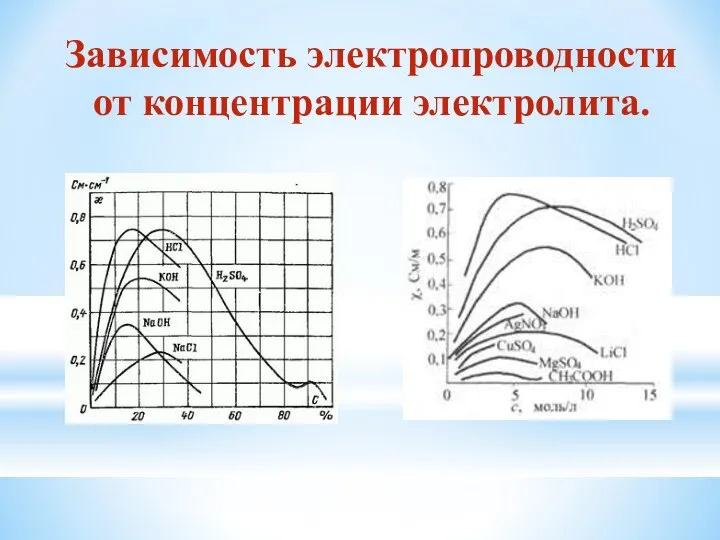
- 8. Зависимость электропроводности от концентрации электролита.
- 9. Молярная электропроводность – электропроводность объема раствора, содержащего 1 моль/л электролита, находящегося между 2-мя параллельными электродами на
- 10. Молярная (эквивалентная) электропроводность возрастает с разбавлением. При С → 0 λ → max Причины: 1) исчезает
- 11. Молярная (эквивалентная) электропроводность при бесконечном разведении (λ∞) зависит только от скорости движения ионов. Кольрауш (1875 г)
- 12. Из всех катионов – катионы Н+ и анионов – гидроксид-ионы ОН- обладают аномально большой подвижностью. Имеет
- 13. При полной диссоциации электролита α=1, а λ=λ∞, отсюда α = λ / λ∞ Оствальд установил, что:
- 14. Организм человека можно отнести к группе своеобразных полимеров – биополимеров, это химические соединения, состоящие из большого
- 15. Живая ткань, особенно ткань нервной системы, обладает сложнейшей комплексной электропроводностью. На практике в качестве диагностического признака
- 16. Электропунктурная диагностика (ЭПД) – метод диагностики заболеваний, основанный на измерении электропроводности биологически активных точек (БАТ). Реография
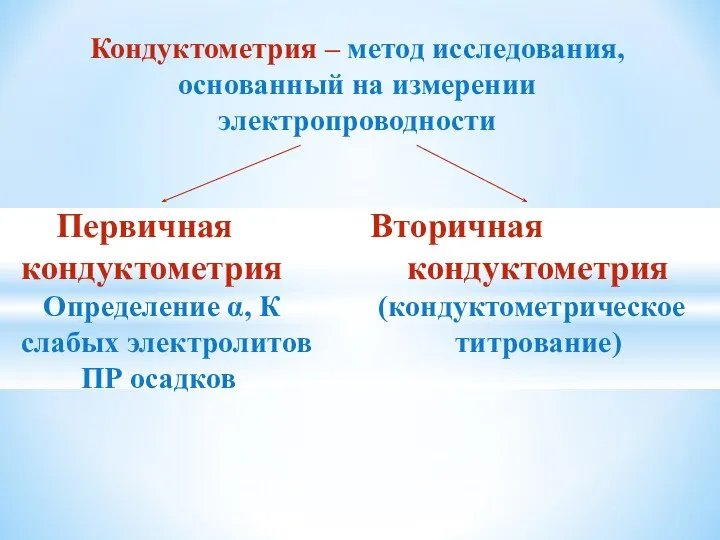
- 17. Кондуктометрия – метод исследования, основанный на измерении электропроводности Первичная Вторичная кондуктометрия кондуктометрия Определение α, К (кондуктометрическое
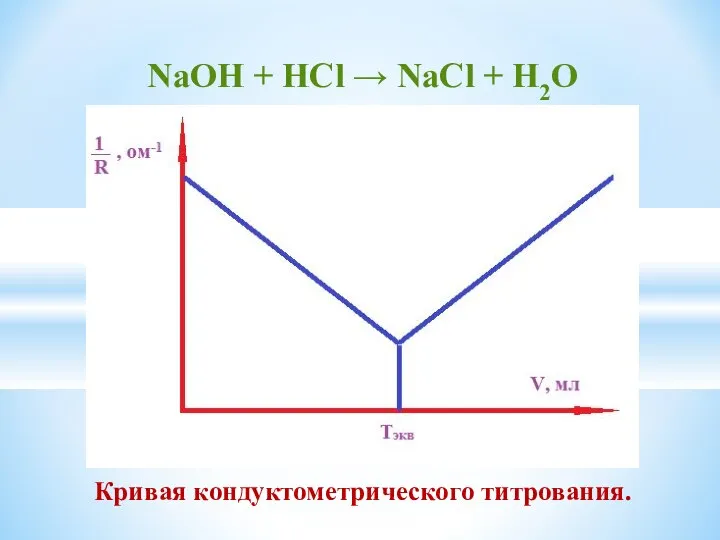
- 18. NaОН + HСl → NaCl + H2O Кривая кондуктометрического титрования.
- 19. Электрохимия изучает взаимное превращение химической энергии в электрическую и наоборот. 2 типа электрохимии Химическая Химическая энергия
- 20. В электрическую энергию можно превратить энергию только окислительно-восстановительного процесса. Гальванический элемент – это устройство, в котором
- 21. Электрохимические цепи – системы, состоящие из двух электродов, помещенных в раствор электролита или в два разных
- 22. Гальванические элементы Химические Концентрационные В химических цепях источником электрической энергии является энергия Гиббса, протекающей в системе
- 23. В гальваническом элементе есть: - металл (электрод) – проводник I рода - раствор электролита – проводник
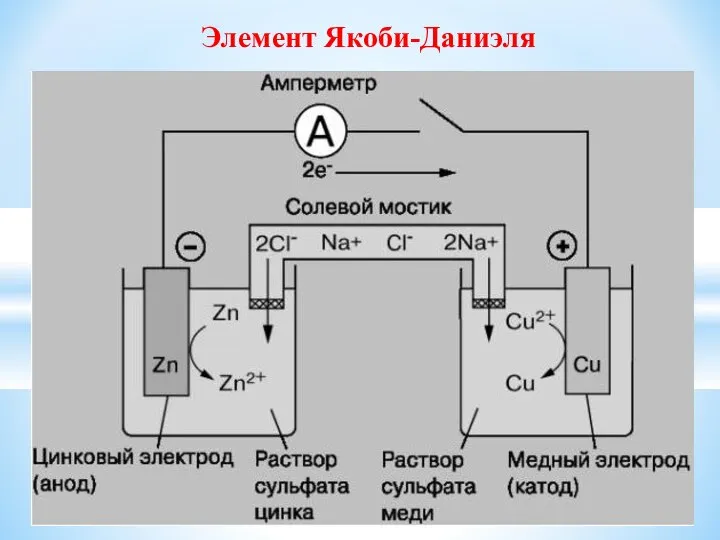
- 24. Элемент Якоби-Даниэля
- 25. Работа гальванического элемента можно рассматривать как результат окислительно- восстановительной реакции Zn – 2e → Zn2+ ΔGo
- 26. Электродвижущая сила (Е) гальванического элемента равна разности потенциалов правого и левого электродов Е = ϕправ -
- 27. Если ЭДС элемента положительна, то реакция протекает самопроизвольно, т.е. Е > 0 и ΔG где z
- 28. При погружении металла в воду или раствор его соли часть ионов металла Мz+ переходит в раствор.
- 29. Абсолютное значение электродного потенциала определить невозможно. На практике измеряют разность потенциалов исследуемого электрода и некоторого стандартного
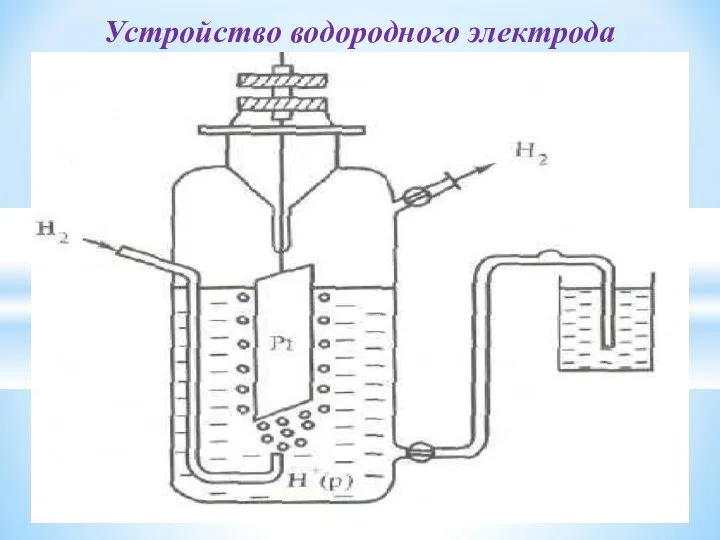
- 30. Устройство водородного электрода
- 31. Концентрационные элементы состоят из двух одинаковых электродов, помещенных в растворы с разной концентрацией соли С1 и
- 32. Все используемые электроды делят: 1) Электроды I рода, они обратимы относительно катионов. Это металлические электроды, опущенные
- 33. К электродам сравнения относят: 1) водородный электрод. 2) хлорсеребряный электрод. 3) каломельный электрод. Хлорсеребряный электрод состоит
- 34. Окислительно-восстановительные (редокс) электроды – такие полуэлементы, в которых материал электрода (Pt, Pd) в реакции не участвует,
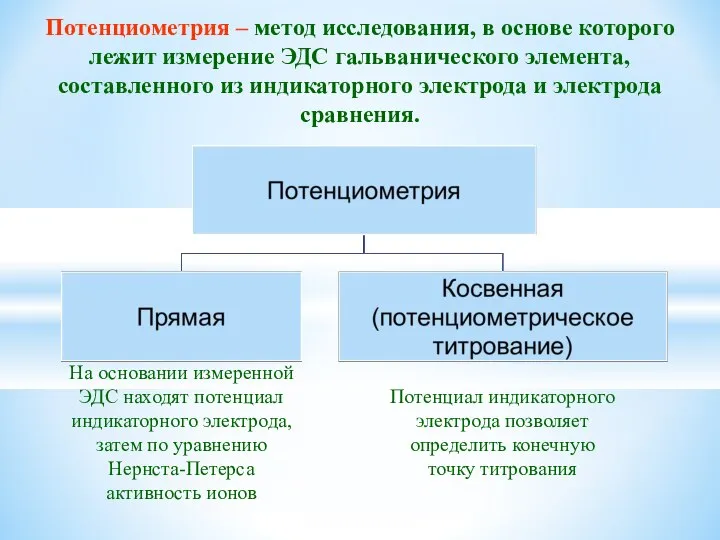
- 35. Потенциометрия – метод исследования, в основе которого лежит измерение ЭДС гальванического элемента, составленного из индикаторного электрода
- 36. Для определения рН раствора составляется гальванический элемент. Для 2Н+ + 2е ↔ Н2
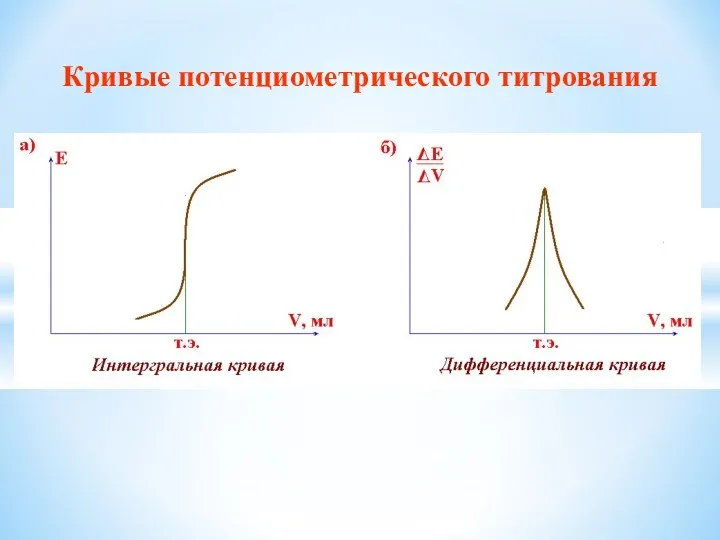
- 37. Кривые потенциометрического титрования
- 39. Скачать презентацию

![Электропроводность – способность вещества проводить электрический ток L = 1/R [ом-1]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394736/slide-3.jpg)
![Электропроводность Удельная χ = 1/ρ [ом-1⋅м-1] χ-каппа Молярная λ = 1000](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394736/slide-4.jpg)

























 Натрій. Знаходження в періодичній системі і основні характеристики
Натрій. Знаходження в періодичній системі і основні характеристики Степень окисления. Бинарные соединения металлов и не металлов: оксиды, хлориды, сульфиды и др.
Степень окисления. Бинарные соединения металлов и не металлов: оксиды, хлориды, сульфиды и др.  Кальций
Кальций Вода - Н2О
Вода - Н2О ZnS и ZnSe как оптические материалы,люминофоры, лазерные матрицы
ZnS и ZnSe как оптические материалы,люминофоры, лазерные матрицы Многообразие органических веществ
Многообразие органических веществ Личностно-ориентированный подход в обучении химии
Личностно-ориентированный подход в обучении химии Первые шаги в минералогию: от новичка до знатока
Первые шаги в минералогию: от новичка до знатока Иерархия классов методов моделирования. Атомистические и микроскопические методы
Иерархия классов методов моделирования. Атомистические и микроскопические методы Задачи на смеси (задание № 33)
Задачи на смеси (задание № 33) Характеристика галогенів. Їх біологічне значення Виконали учениці 10-Б класу Халімон Заріна Петрова Оксана Борисенко Юлія Ми
Характеристика галогенів. Їх біологічне значення Виконали учениці 10-Б класу Халімон Заріна Петрова Оксана Борисенко Юлія Ми Температура точки росы газа
Температура точки росы газа ОГЭ химия 2021 задание 13
ОГЭ химия 2021 задание 13 Химическая природа и состав нефти и газа. Физико-химические свойства нефтей и нефтепродуктов
Химическая природа и состав нефти и газа. Физико-химические свойства нефтей и нефтепродуктов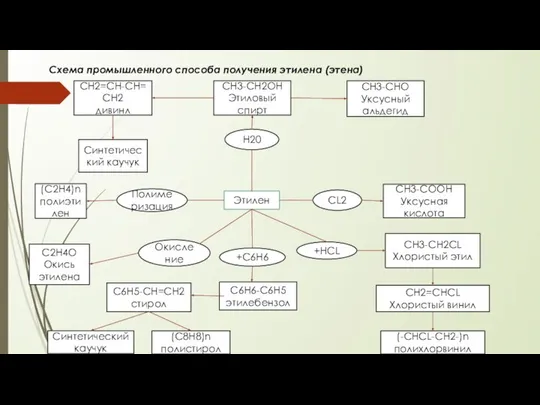 Промышленній способ получения этилена (этена)
Промышленній способ получения этилена (этена)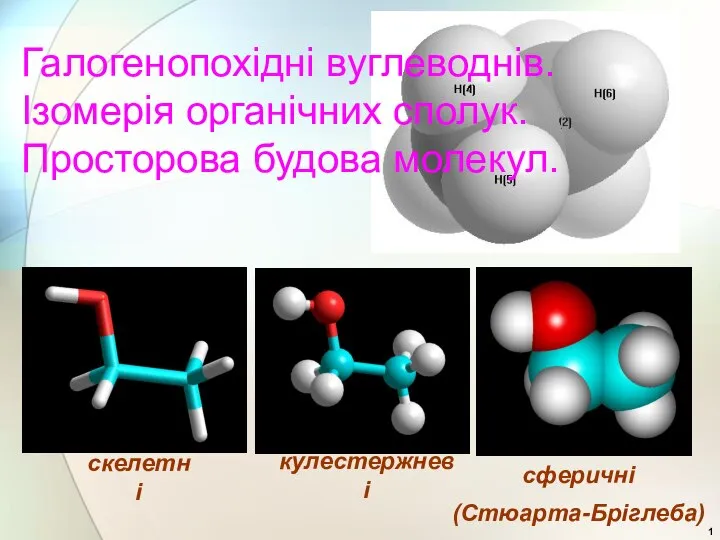 Галогенопохідні вуглеводнів. Ізомерія органічних сполук. Просторова будова молекул
Галогенопохідні вуглеводнів. Ізомерія органічних сполук. Просторова будова молекул Производные пиррозилидина. (Лекция 6)
Производные пиррозилидина. (Лекция 6) Диагностика магматических горных пород
Диагностика магматических горных пород Хлороводород и соляная кислота
Хлороводород и соляная кислота Презентация по Химии "Техника безопасности на уроках химии" - скачать смотреть
Презентация по Химии "Техника безопасности на уроках химии" - скачать смотреть  Циклоалканы и их применение
Циклоалканы и их применение Хімічні явища в побуті
Хімічні явища в побуті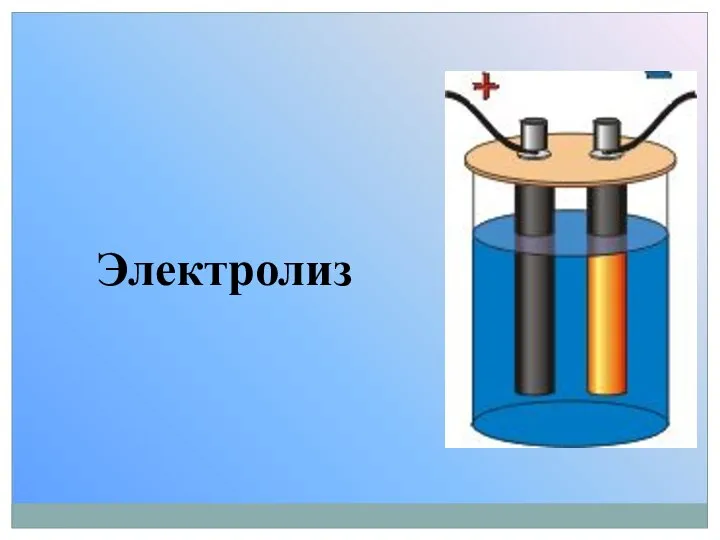 Электролиз
Электролиз Химиялық тепе-теңдік және оның ығысуына әсер етуші жағдайлар. Ле Шателье-Браун принциптері
Химиялық тепе-теңдік және оның ығысуына әсер етуші жағдайлар. Ле Шателье-Браун принциптері Вода. Состав и строение молекулы
Вода. Состав и строение молекулы Кислород
Кислород Геохимия природных процессов. Редкие элементы, как индикаторы геодинамических обстановок формирования комплексов. (Лекция 5)
Геохимия природных процессов. Редкие элементы, как индикаторы геодинамических обстановок формирования комплексов. (Лекция 5) Закономерности управления каталитическими процессами. Упрощенный вариант
Закономерности управления каталитическими процессами. Упрощенный вариант