Содержание
- 2. Основные тенденции в 7 группе 1. Свойства Mn отличаются от свойств Tc и Re, которые похожи
- 3. Сравнение свойств в периоде MnO4– TcO4– ReO4– Увеличивается радиус металла Уменьшается сила кислот Уменьшается окислительная способность
- 4. Сравнение свойств в периоде VO43– CrO42– MnO4– Возрастает число связей М=О Увеличивается сила кислот Уменьшается радиус
- 5. Свойства марганца Марганец - серебристо-белый металл. На воздухе металл покрывается пестрыми пятнами оксидной пленки, которая предохраняет
- 6. Свойства марганца Mn
- 7. Свойства марганца
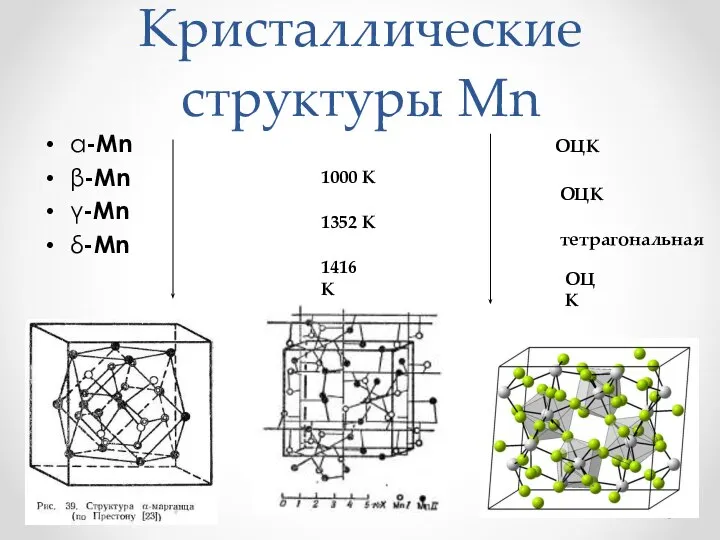
- 8. Кристаллические структуры Mn α-Mn ОЦК β-Mn γ-Mn δ-Mn 1000 К 1352 К 1416 К ОЦК тетрагональная
- 9. Химические свойства Mn 1.Высокая реакционная способность 2Mn + 2NH4Cl + 2H2O = 2MnCl2+ 2NH3·H2O + H2
- 10. Химические свойства Mn 5.Реагирует с F2, O2 с образованием Mn3+ 2Mn + 3F2 = 2MnF3(200 oC)
- 11. Химические свойства Mn 7.Реагирует с углеродом, образуя карбиды Mn7C3, Mn3C, Mn5C2
- 12. Нахождение в природе Марганец–распространенный элемент (0.028 ат.%) Основные минералы: Пиролюзит β-MnO2·nH2O Родохрозит MnCO3 Браунит Mn2O3 Манганит
- 13. Получение Mn Основные процессы получения Mn: MnO2 + Fe2O3 + 5C = Mn + 2Fe +
- 14. Применение Mn Mn-для инструментальных и конструкционных сталей высокой ударной стойкости Mn-бронзы Mn-электротехнические сплавы Mn2+–микродобавки к удобрениям
- 15. Окислительно-восстановительные свойства Mn 1. В кислой среде самая устойчивая с.о. +2 2. В щелочной среде устойчивы
- 16. Высшие степени окисления Mn 1. Получение: MnO2+ 2KOH + KNO3= K2MnO4+ KNO2+ H2O Mn+4→Mn+6 2K2MnO4+ Cl2=
- 17. 2. Марганцевая кислота: Получение: 2Mn(NO3)2+ 5PbO2+ 6HNO3= 2HMnO4+ 5Pb(NO3)2+ 2H2O Х.С. 2KMnO4+ H2SiF6= K2SiF6 ↓+ 2HMnO4
- 18. 3. Окислитель(+7): 8KMnO4+ 5K2S + 12H2SO4= 8MnSO4+ 9K2SO4+ 12H2O 2KMnO4+ 3H2SO3= 2MnO2↓+ K2SO4+ 2H2SO4+ H2O 4KMnO4+
- 19. 4. Диспропорционирование манганата(VI): 3K2MnO4+ 2H2O = 2KMnO4+ MnO2+ 4KOH 3K2MnO4+ 2CO2= 2KMnO4+ MnO2+ 2K2CO3 Кислота H2MnO4
- 20. Соединения Mn(V,IV) Соединения Mn(V) неустойчивы, сильные окислители 2KMnO4+ 2Na2SO3+ 4NaOH = 2Na3MnO4+ Na2SO4+ K2SO4+2H2O 2. Соединения
- 21. Соединения Mn(V,IV) 4. Соли Mn(IV) легко гидролизуются: Mn(SO4)2+ 2H2O = MnO2+ 2H2SO4 5. Известен фторид Mn(IV)
- 22. Соединения Mn(III) Бинарные соединения: 2Mn + 3F2= 2MnF3 (200 оС) 4MnO2= 2Mn2O3+ O2 (500 oC) 2.
- 23. Комплексы Mn(III) Образование комплексов KMnO4+ 6KF + 8HCl = K3[MnF6]+ 4H2O + 4KCl KMnO4+ 2H2SO4+ 2H2O2=
- 24. Соединения Mn(II) Получение: 2MnO2+ 2H2SO4(70%) = 2MnSO4+ O2+ 2H2O Mn+ 2HCl = MnCl2+ H2 2. Гидроксид
- 25. Соединения Mn(II) 3. Mn(II) окисляется в щелочной среде или при нагревании: 3MnSO4= Mn3O4+ 3SO2+ O2 Mn(NO3)2=
- 26. Комплексы Mn(II) Наиболее устойчивы оксо- и фторо-комплексы: MnSO4+ 6H2O = [Mn(H2O)6]SO4 4KF + MnF2= K4[MnF6] 2.
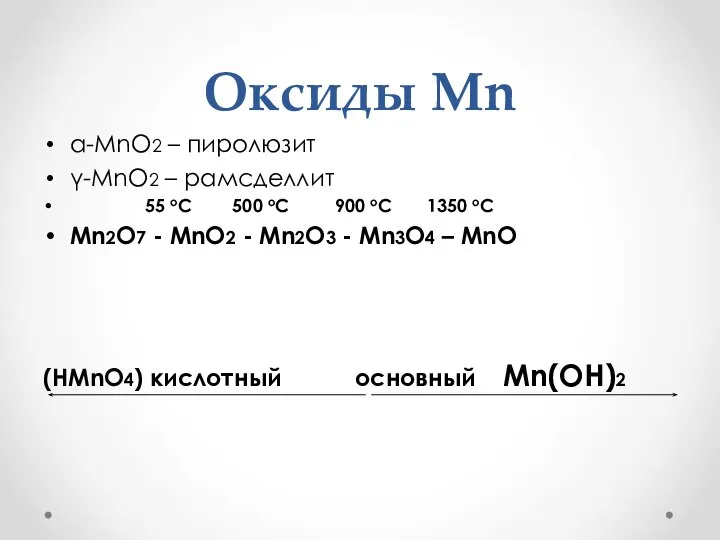
- 27. Оксиды Mn α-MnO2 – пиролюзит γ-MnO2 – рамсделлит 55 oC 500 oC 900 oC 1350 oC
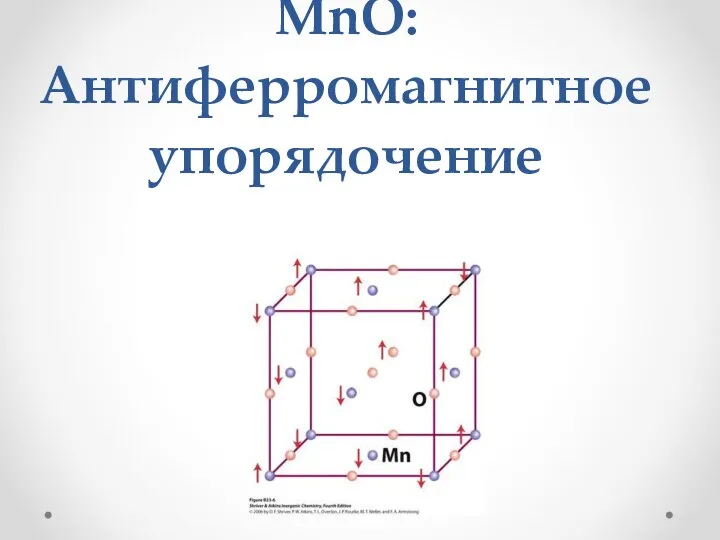
- 28. MnO: Антиферромагнитное упорядочение
- 30. Скачать презентацию




















![Комплексы Mn(III) Образование комплексов KMnO4+ 6KF + 8HCl = K3[MnF6]+ 4H2O](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1407027/slide-22.jpg)


![Комплексы Mn(II) Наиболее устойчивы оксо- и фторо-комплексы: MnSO4+ 6H2O = [Mn(H2O)6]SO4](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1407027/slide-25.jpg)
 ПРЕЗЕНТАЦИЯ «Химия и повседневная жизнь человека»
ПРЕЗЕНТАЦИЯ «Химия и повседневная жизнь человека»  Видатні вітчизняні хіміки
Видатні вітчизняні хіміки Альдегиды и кетоны
Альдегиды и кетоны Дизельное топливо
Дизельное топливо Презентация по Химии "Применение алюминия и его сплава" - скачать смотреть
Презентация по Химии "Применение алюминия и его сплава" - скачать смотреть  Химический аквариум или живое из неживого
Химический аквариум или живое из неживого Общая характеристика металлов
Общая характеристика металлов Кобальт. Химический элемент
Кобальт. Химический элемент Презентация на тему «Металлы и сплавы в моей профессии. Антикоррозийные покрытия»
Презентация на тему «Металлы и сплавы в моей профессии. Антикоррозийные покрытия»  Углерод
Углерод Колебания кристаллической решетки и ее тепловые свойства. Динамика решетки
Колебания кристаллической решетки и ее тепловые свойства. Динамика решетки Традиции и обычаи Узбекистана Национальные обряды, игры, праздники
Традиции и обычаи Узбекистана Национальные обряды, игры, праздники Презентация по Химии "Химия неметаллов. Общая характеристика" - скачать смотреть
Презентация по Химии "Химия неметаллов. Общая характеристика" - скачать смотреть  Простой борный суперфосфат
Простой борный суперфосфат Нафта: склад,властивості, основні процеси переробки,застосування
Нафта: склад,властивості, основні процеси переробки,застосування  Массовая доля растворённого вещества
Массовая доля растворённого вещества Получение армированных фотополимерных композиций
Получение армированных фотополимерных композиций Презентация по Химии "Синтетичні мийні засоби" - скачать смотреть бесплатно
Презентация по Химии "Синтетичні мийні засоби" - скачать смотреть бесплатно Посвящение в химики. Игра-викторина. Внеклассное мероприятие по химии для учащихся 8 классов.
Посвящение в химики. Игра-викторина. Внеклассное мероприятие по химии для учащихся 8 классов.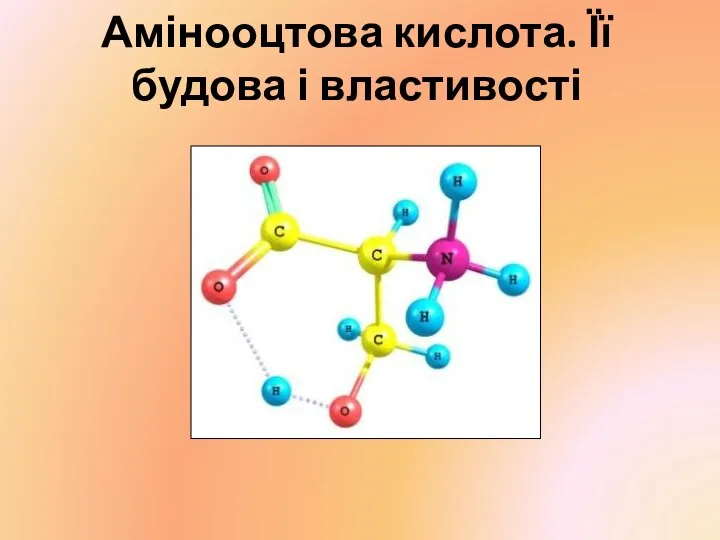 Амінооцтова кислота. Її будова і властивості
Амінооцтова кислота. Її будова і властивості Методы исследования белковых молекул
Методы исследования белковых молекул Именные реакции в органической химии. Органический синтез. Механизмы химических процессов
Именные реакции в органической химии. Органический синтез. Механизмы химических процессов Ph воды
Ph воды Нуклеопротеины
Нуклеопротеины Углеводы. Структура
Углеводы. Структура Спирты: свойства, получение, применение
Спирты: свойства, получение, применение Колоїдна хімія
Колоїдна хімія Химические свойства хрома
Химические свойства хрома