Содержание
Химические свойства хрома:
Cr2O72- + 2OH- ↔ 2CrO42- + H2O
В щелочной среде
Химические свойства хрома:
Cr2O72- + 2OH- ↔ 2CrO42- + H2O
В щелочной среде
CrO42- + 3ē + 4H2O = Cr(OH)3 + 5OH-
(Eo=-0.13 B)
Ион Cr6+ в щелочной среде – очень слабый окислитель:
CrO42- + K2SO3 + OH- → нет взаимодействия
(изменение цвета раствора)
Свойства марганца
MnCl2 + 2KOH
Mn2+ при взаимодействии с OH- выпадает в осадок
Свойства марганца
MnCl2 + 2KOH
Mn2+ при взаимодействии с OH- выпадает в осадок
Mn(OH)2 + 2KCl
Хранение на воздухе Mn(OH)2 приводит к медленному окислению до MnO2. Для ускорения процесса используем Br2 (бромная вода) – более cильный окислитель:
2Mn(OH)2 + O2
2MnO2 + 2H2O
Mn(OH)2 + Br2
MnO2 + 2HBr
K2MnO4 – манганат калия в кислой среде диспропорционирует:
Mn2+
Mn6+
2K2MnO4 + 4CH3COOH = MnO2 + KMnO4 + 4CH3COOK + 2H2O
Восстановительные свойства K2MnO4:
K2MnO4 + 4FeSO4 +4H2SO4 = MnSO4 + K2SO4 + Fe2(SO4)3 + 4H2O
K2MnO4 + HNO3(конц.) = Mn(NO3)2 + KMnO4 + 2KNO3 + 4H2O
(ПР~10-13)
MnCl2 + Na2S
MnS + 2NaCl
(ПР~10-17)


 синтетичні мийні засоби
синтетичні мийні засоби  Көмірсу. Көмірсулардың қасиеттері. Көмірсудың метаболизмі
Көмірсу. Көмірсулардың қасиеттері. Көмірсудың метаболизмі Лужні метали Підготувала: Анна Сідорова
Лужні метали Підготувала: Анна Сідорова 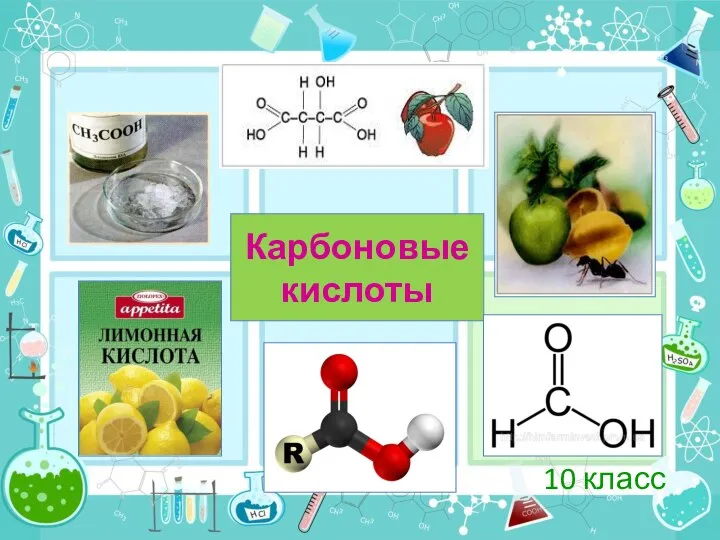 Карбоновые кислоты. (10 класс)
Карбоновые кислоты. (10 класс) Адсорбция
Адсорбция Массовая доля вещества в растворе
Массовая доля вещества в растворе Виды парфюмерно-косметической косметики
Виды парфюмерно-косметической косметики Классификация органических соединений
Классификация органических соединений Эксперимент. Выращивание солевых кристаллов
Эксперимент. Выращивание солевых кристаллов Атомы и молекулы
Атомы и молекулы Рибонуклеиновая кислота
Рибонуклеиновая кислота Распределение электронов в атомах. Энергетические уровни
Распределение электронов в атомах. Энергетические уровни Химия в пищевой промышленности
Химия в пищевой промышленности Коррозия металлов в контакте
Коррозия металлов в контакте Оружие массового поражения. Биологическое оружие
Оружие массового поражения. Биологическое оружие  Абразивные материалы
Абразивные материалы Условия проведения реакции дегидратации
Условия проведения реакции дегидратации Интоксикации сельскохозяйственными ядохимикатами (пестицидами)
Интоксикации сельскохозяйственными ядохимикатами (пестицидами) Неорганическая химия Сероводород
Неорганическая химия Сероводород  Практична робота з хімії “Металічні елементи та їхні сполуки” Виконала учениця 10-А класу Ковальова Анастасія
Практична робота з хімії “Металічні елементи та їхні сполуки” Виконала учениця 10-А класу Ковальова Анастасія  Корень как часть слова
Корень как часть слова  Синтез наночастиц неорганических веществ. (Лекция 7)
Синтез наночастиц неорганических веществ. (Лекция 7) 3 Стехиометрические законы
3 Стехиометрические законы Спирты Предельные одноатомные спирты
Спирты Предельные одноатомные спирты Ступенчатые процессы получения полимеров: полиприсоединение, поликонденсация
Ступенчатые процессы получения полимеров: полиприсоединение, поликонденсация Презентация по Химии "Цветная металлургия" - скачать смотреть
Презентация по Химии "Цветная металлургия" - скачать смотреть  Химические свойства карбоновых кислот
Химические свойства карбоновых кислот Основы коррозии и защиты металлов
Основы коррозии и защиты металлов