Содержание
- 2. Содержание Энтропия Второе начало термодинамики Энергия Гиббса. Термодинамическая возможность прохождения химической реакции Влияние температуры на направление
- 3. Энтропия (S) Предложена Клаузиусом как функция, изменение которой равно отношению теплоты, поглощенной системой, к абсолютной температуре:
- 4. Термодинамическая вероятность состояния Состояние системы можно характеризовать значениями параметров (температура, давление, объем), которые определяют макросостояние системы
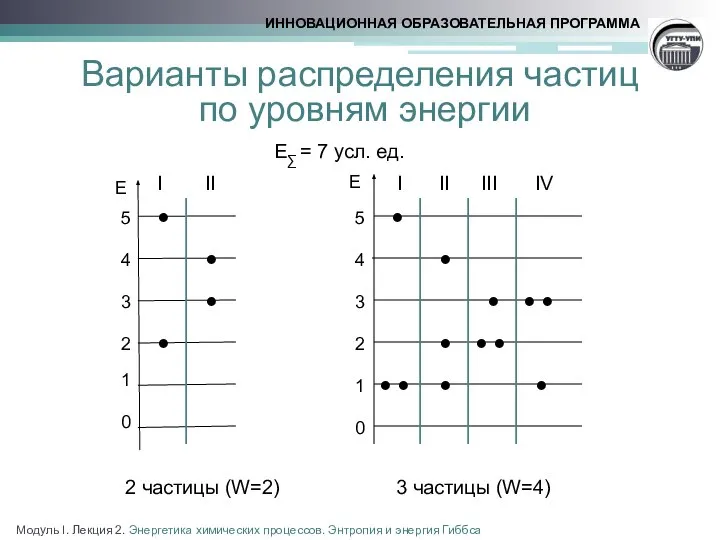
- 5. Варианты распределения частиц по уровням энергии E∑ = 7 усл. ед. 2 частицы (W=2) 3 частицы
- 6. Энтропия - мера термодинамической вероятности состояния системы Формула Больцмана: k – постоянная Больцмана R – универсальная
- 7. Уменьшением энтропии сопровождаются процессы, связанные с увеличением упорядоченности: охлаждение, кристаллизация, конденсация веществ; реакции с уменьшением объема
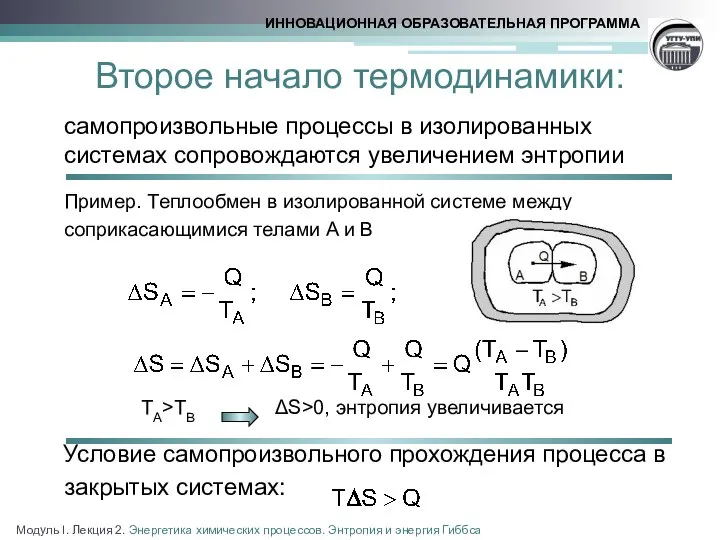
- 8. Второе начало термодинамики: самопроизвольные процессы в изолированных системах сопровождаются увеличением энтропии Пример. Теплообмен в изолированной системе
- 9. Расчет изменения энтропии химической реакции в стандартных условиях Энтропия реакции равна разности сумм энтропий продуктов реакции
- 10. Энергия Гиббса Самопроизвольное прохождение химической реакции в закрытой системе (р, Т = const) возможно при условии
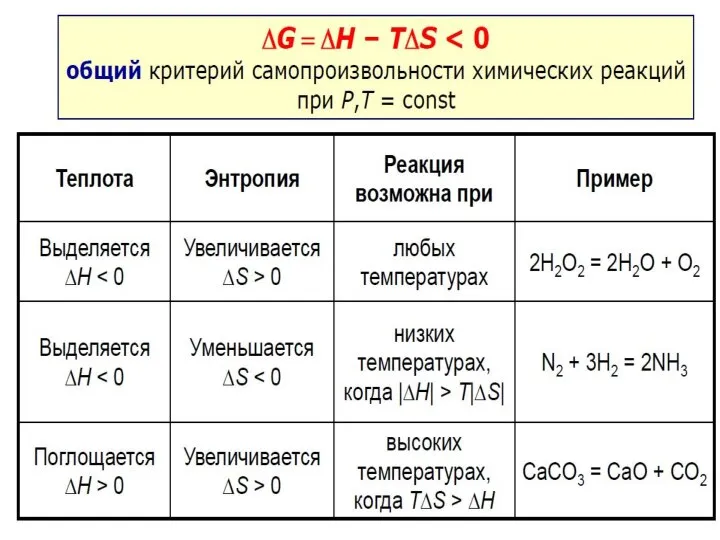
- 11. Энергия Гиббса – критерий возможности самопроизвольного прохождения химических реакций Процессы, для которых ΔG ΔG>0 – термодинамически
- 12. Влияние температуры на направление химической реакции 1. ΔH Пример: N2 + 3H2 = 2NH3 2. ΔH>0,
- 14. Расчет стандартной энергии Гиббса химической реакции В справочниках – значения стандартных энергий Гиббса образования веществ (ΔG0обр,
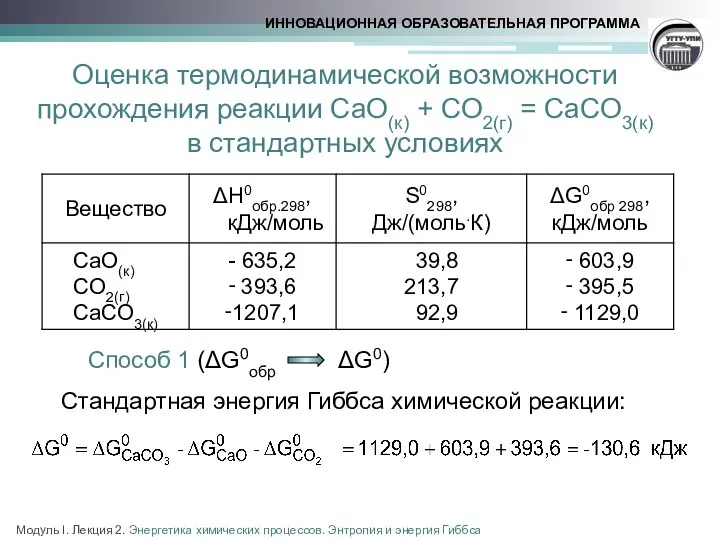
- 15. Оценка термодинамической возможности прохождения реакции CaO(к) + CO2(г) = CaCO3(к) в стандартных условиях Способ 1 (ΔG0обр
- 16. Оценка термодинамической возможности прохождения реакции CaO(к) + CO2(г) = CaCO3(к) в стандартных условиях Способ 2 (ΔH0обр
- 17. Заключение Согласно II началу термодинамики самопроизвольные процессы в изолированных системах сопровождаются увеличением энтропии Энтропия по своему
- 19. Скачать презентацию












 Презентация по Химии "«Закон сохранения массы вещества»" - скачать смотреть
Презентация по Химии "«Закон сохранения массы вещества»" - скачать смотреть  Інсектициди для захисту сливи та персеку
Інсектициди для захисту сливи та персеку Способы получения металлов. (11 класс)
Способы получения металлов. (11 класс) Алюминий и его соединения
Алюминий и его соединения II главная подгруппа ПС: Be, Mg, Ca, Sr, Ba, Ra
II главная подгруппа ПС: Be, Mg, Ca, Sr, Ba, Ra Соединения серы. Серная кислота. Важнейшие соединения серы
Соединения серы. Серная кислота. Важнейшие соединения серы Организация физической защиты ДРМ
Организация физической защиты ДРМ Комплексні сполуки
Комплексні сполуки Электростатические взаимодействия, как фактор, определяющий структуру и реакционную способность органических соединений
Электростатические взаимодействия, как фактор, определяющий структуру и реакционную способность органических соединений Основы теории сплавов. Типы сплавов (твердые растворы, сплавы-смеси, сплавы- химические соединения. Диаграммы
Основы теории сплавов. Типы сплавов (твердые растворы, сплавы-смеси, сплавы- химические соединения. Диаграммы Химия. Дисперсные системы. Растворы
Химия. Дисперсные системы. Растворы Обмен железа и его нарушения
Обмен железа и его нарушения Углеводы. Сукралоза
Углеводы. Сукралоза Презентация по Химии "Получение сложнооксидных нано- и микроматериалов методом пиролиза полимерно-солевых композиций" - скач
Презентация по Химии "Получение сложнооксидных нано- и микроматериалов методом пиролиза полимерно-солевых композиций" - скач Високомолекулярні сполуки
Високомолекулярні сполуки Краткая история химии
Краткая история химии Битумы природного происхождения
Битумы природного происхождения Исследовательская работа по теме: « Волшебные жидкости – вещества определители или как определить вкус веществ не пробуя их»
Исследовательская работа по теме: « Волшебные жидкости – вещества определители или как определить вкус веществ не пробуя их»  Кремний и его соединения
Кремний и его соединения Понятие о химической реакции. Реакции без изменения состава веществ
Понятие о химической реакции. Реакции без изменения состава веществ Решение задач Скорость химических реакций 11 класс
Решение задач Скорость химических реакций 11 класс  Презентация по Химии "Полимеры" - скачать смотреть
Презентация по Химии "Полимеры" - скачать смотреть  Тотықтырғыштар
Тотықтырғыштар Кафедра общей и биоорганической химии
Кафедра общей и биоорганической химии Химический состав и пищевая ценность кофе
Химический состав и пищевая ценность кофе Углерод. Химические свойства
Углерод. Химические свойства Аттестацианная работа. Основы исследовательской деятельности по химии
Аттестацианная работа. Основы исследовательской деятельности по химии Неорганические соединения. Тест
Неорганические соединения. Тест