Содержание
- 2. Щоб пізнати – треба навчитися спостерігати
- 3. М е т а ознайомитися із основними фізико-хімічними властивостями, будовою та застосуванням етилену і ацетилену; навчитися
- 4. План 1. Поняття про ненасичені вуглеводні. Номенклатура. 2. Будова молекул етену та етину. 3. Фізичні властивості,
- 5. Ненасичені вуглеводні – органічні сполуки, що мають кратні зв’язки між атомами Карбону (подвійні – С =
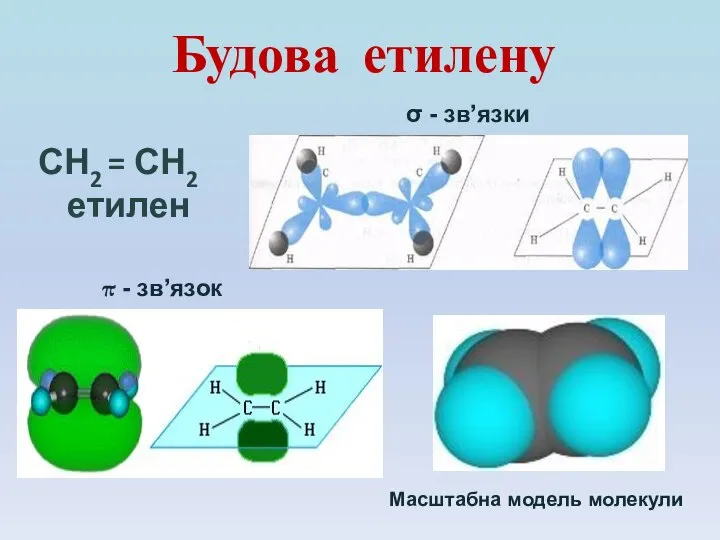
- 6. Будова етилену СН2 = СН2 етилен σ - зв’язки π - зв’язок Масштабна модель молекули
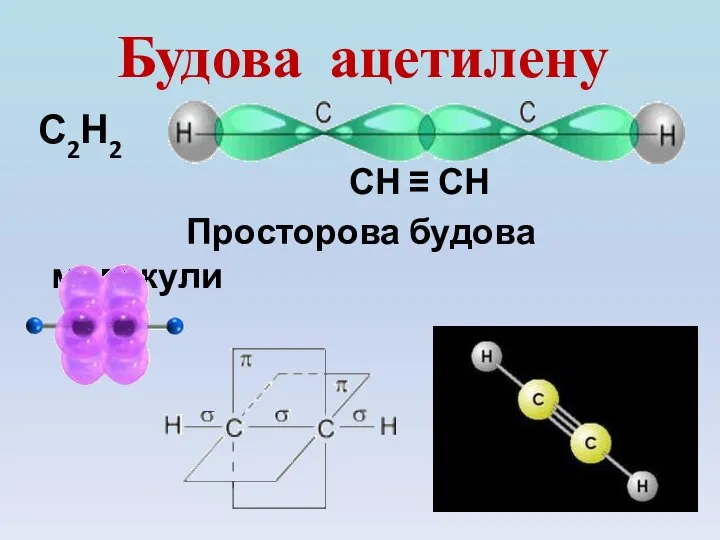
- 7. Будова ацетилену С2Н2 СН ≡ СН Просторова будова молекули
- 8. Фізичні властивості етилену С2Н4 безбарвний газ; добре розчинний в органічних розчинниках; tплавл = - 169,2 ̊С;
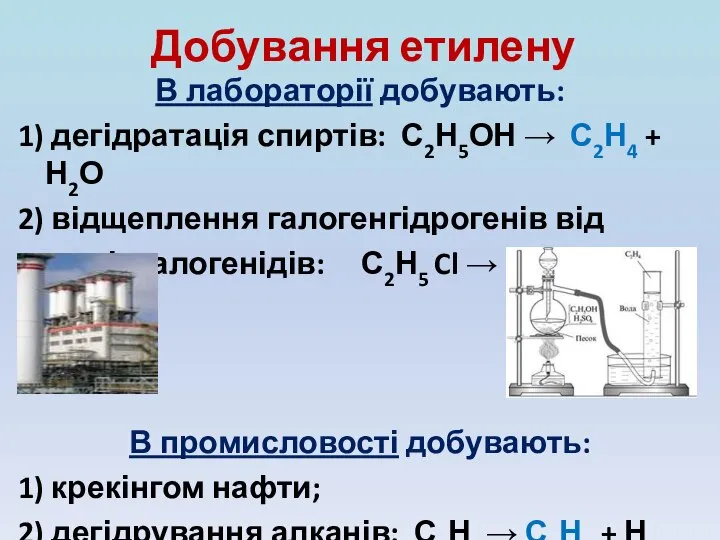
- 9. Добування етилену В лабораторії добувають: 1) дегідратація спиртів: С2Н5ОН → С2Н4 + Н2О 2) відщеплення галогенгідрогенів
- 10. Фізичні властивості С2Н2 безбарвний газ; майже без запаху; малорозчинний у воді, але під тиском добре розчиняється
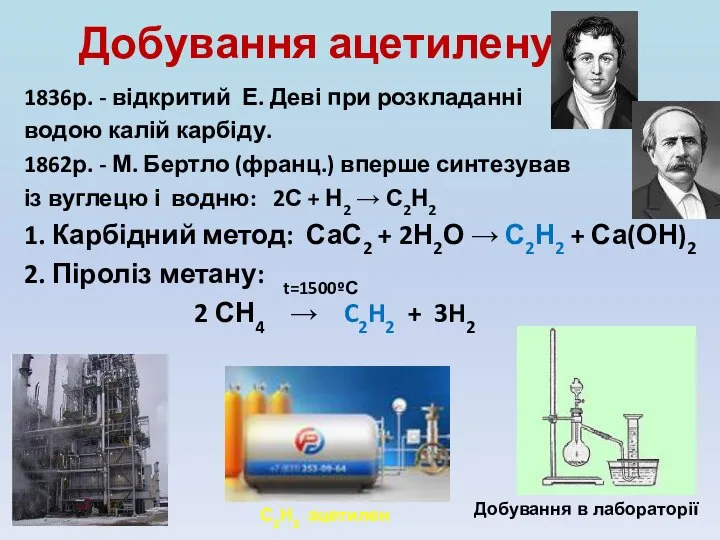
- 11. Добування ацетилену 1836р. - відкритий Е. Деві при розкладанні водою калій карбіду. 1862р. - М. Бертло
- 12. Хімічні властивості етилену Горіння (з виділенням великої кількості теплоти): С2Н4 + 3O2 → 2СО2 +2Н2О 2.
- 13. Хімічні властивості ацетилену Горіння (яскравим кіптявим полум’ям): 2С2Н2 + 5O2 → 4СО2 +2Н2О 2. Реакції приєднання
- 14. Застосування Етилен Ацетилен Висока реакційна здатність зумовлює використання в хімічній промисловості для добування етанолу та етиленгліколю
- 15. Дайте відповіді на питання 1. Ацетилен у лабораторії добувають взаємодією: а) кальцій силікату і води; б)
- 16. Заплановані результати Я ЗНАЮ Я МОЖУ Я ВМІЮ - будову молекул етену, ацетилену; - типи реакцій,
- 18. Скачать презентацию










 Информационные технологии на уроках химии
Информационные технологии на уроках химии Способы переработки нефти
Способы переработки нефти Пластические массы
Пластические массы Правила безпечного використання засобів побутової хімії
Правила безпечного використання засобів побутової хімії  Теория электролитической диссоциации
Теория электролитической диссоциации Тема: «Самородные металлы».
Тема: «Самородные металлы». Энергетика химических процессов
Энергетика химических процессов Вплив фосфатної побутової хімії на організм людини.
Вплив фосфатної побутової хімії на організм людини.  Решение задач по теме «Растворы»
Решение задач по теме «Растворы» Химическая термодинамика и кинетика
Химическая термодинамика и кинетика соединения АЗОТА Материал для повторения и подготовки к ГИА Учитель химии МОУ «Гимназия №1»г. Саратова Шишкина И.Ю.
соединения АЗОТА Материал для повторения и подготовки к ГИА Учитель химии МОУ «Гимназия №1»г. Саратова Шишкина И.Ю. Основные свойства кристаллов
Основные свойства кристаллов Презентация по Химии "Етери та естери" - скачать смотреть бесплатно
Презентация по Химии "Етери та естери" - скачать смотреть бесплатно Поліетелен. Застосування поліетилену
Поліетелен. Застосування поліетилену Гипер-гипофосфатемия
Гипер-гипофосфатемия Ультразвук к в химической технологии. Лекция 5
Ультразвук к в химической технологии. Лекция 5 Класифікація пластмас
Класифікація пластмас  Дисциплина: Химия. Лекция 1. Растворы
Дисциплина: Химия. Лекция 1. Растворы Подготовка к ГИА. Тренажер по химии
Подготовка к ГИА. Тренажер по химии Ферменттер. Зерттелу тарихы
Ферменттер. Зерттелу тарихы Важнейшие кислоты и кислотные остатки. (Леция 1)
Важнейшие кислоты и кислотные остатки. (Леция 1) Углеводы. Строение углеводов
Углеводы. Строение углеводов Презентация по Химии "Горение кислорода" - скачать смотреть
Презентация по Химии "Горение кислорода" - скачать смотреть  Застосування нових сучасних матеріалів з оригінльними властивостями
Застосування нових сучасних матеріалів з оригінльними властивостями  Непредельные углероды. Алкены
Непредельные углероды. Алкены Синтетические моющие средства
Синтетические моющие средства Конденсация. Капельная и пленочная конденсация
Конденсация. Капельная и пленочная конденсация Імунопатологія. Імунопрофілактика і імунотерапія інфекційних захворювань. Засоби імунокорекції
Імунопатологія. Імунопрофілактика і імунотерапія інфекційних захворювань. Засоби імунокорекції