Содержание
- 2. 1. Элемент № 8 2. Oxygenium - Кислород 3. Джозеф Пристли 4. Карл Вильгельм Шееле 5.
- 3. ( продолжение ) 18. Некоторые реакции, идущие с образованием кислорода 19. Получение кислорода в промышленности 20.
- 4. Элемент № 8 OXYGENIUM КИСЛОРОД
- 5. Oxygenium C лат. оxygenium – “ рождающий кислоту” С греч. oxygenes – “ образующий кислоты” Название
- 6. Английский ученый. В 1774 году разложением oксида ртути ( II ) получил кислород и изучил его
- 7. Шведский ученый. В 1771 году провел опыты по разложению оксида ртути ( II ), изучил свойства
- 8. 1743 - 1794 1743 - 1794 С целью проверки опытов Шееле и Пристли в 1774 году
- 9. Голландский алхимик и технолог. Получил кислород примерно за 150 лет до Пристли и Шееле при нагревании
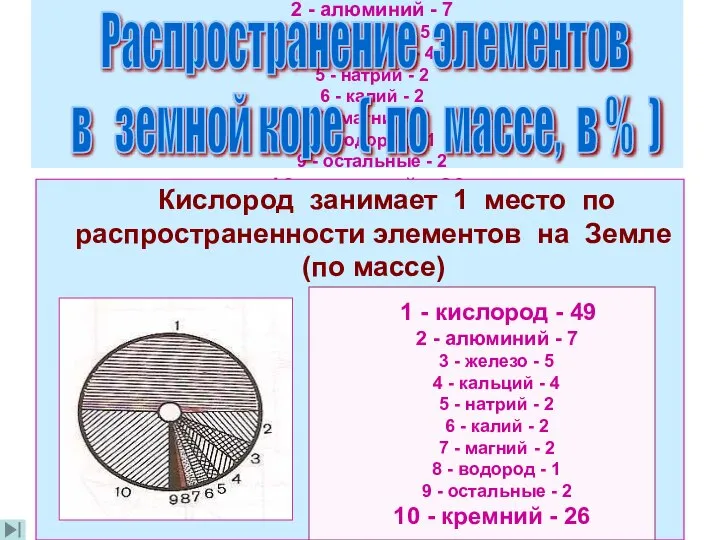
- 10. 1 - кислород - 49 2 - алюминий - 7 3 - железо - 5 4
- 11. В земной коре – 49 % (атмосфера, литосфера, гидросфера) В воздухе – 20,9 % ( по
- 12. В 1774 г. А. Лавуазье доказал, что воздух – это смесь в основном двух газов -
- 13. 1 – Кислород 16% 2 – Углекислый газ 4% 3 – Остальное: азот, водяные пары и
- 14. Отличается от лесного воздуха наличием выбросов: ( загрязняющих и ухудшающих воздух ) от автотранспорта ( в
- 15. Химический знак – О Относительная атомная масса: Ar = 16 Изотопы кислорода – ( 99,75 %),
- 16. Из О2 (при грозе; возд. УФ-Солнца) Газ Синий (г) Резкий, раздражающий 48 1,78 - 192,5 -
- 17. Жидкий озон имеет вид индиго Озон Жидкий озон имеет вид индиго Простейший озонатор Внутрь широкой стеклянной
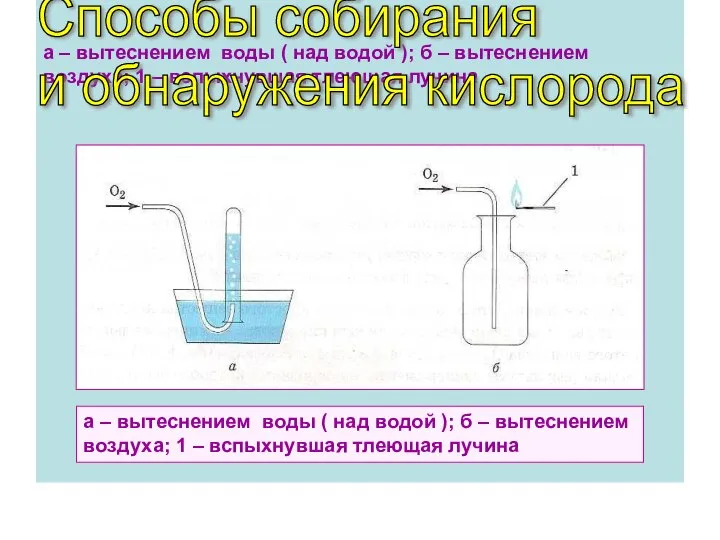
- 18. а – вытеснением воды ( над водой ); б – вытеснением воздуха; 1 – вспыхнувшая тлеющая
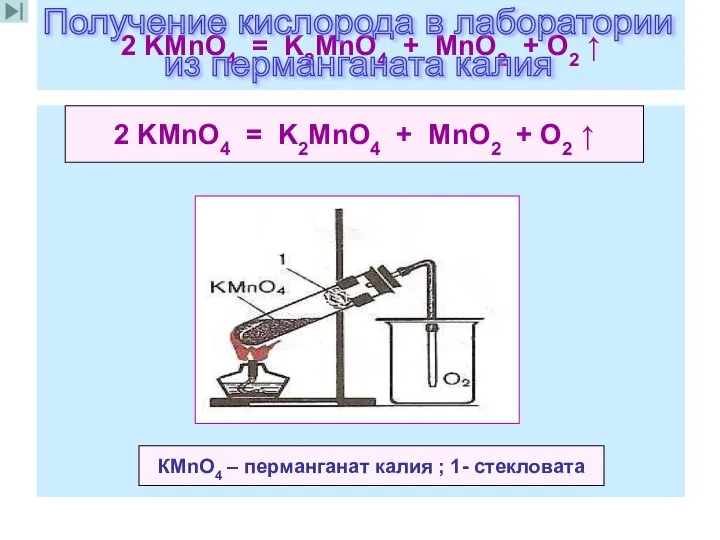
- 19. 2 KMnO4 = K2MnO4 + MnO2 + O2 ↑ 2 KMnO4 = K2MnO4 + MnO2 +
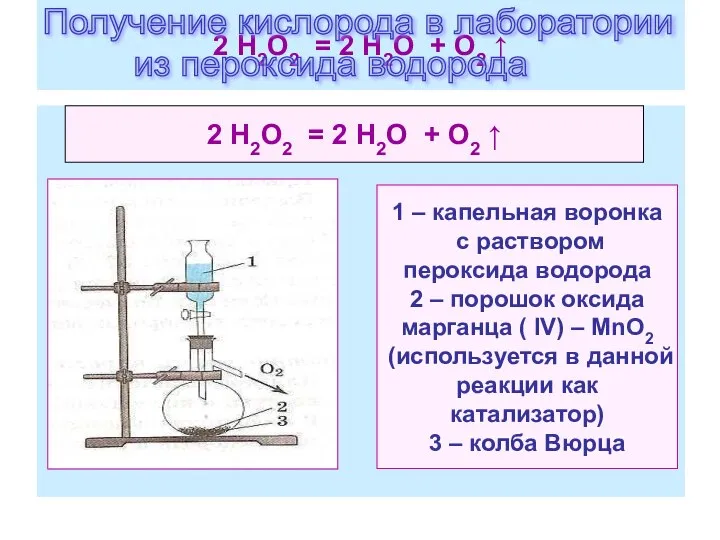
- 20. 2 Н2O2 = 2 Н2O + O2 ↑ 2 Н2O2 = 2 Н2O + O2 ↑
- 21. Условия реакций – нагревание ( t ) 2 КМnО4 = К2МnО4 + МnO2 + О2 ↑
- 22. Кислород получают из воздуха газовой ректификацией Воздух охлаждают примерно до – 200 0С и под давлением
- 23. С + О2 ═ СО2 + Q S + О2 ═ SО2 + Q 4Р +
- 24. 2. Отношение к сложным веществам При полном сгорании углеводородов образуются оксиды - углекислый газ и вода:
- 25. О - как окислитель : О0 + 2 → О–2 (1) ( как правило ) О
- 26. 1. Прекратить доступ к горючему веществу кислорода 2. Охладить вещество ниже температуры воспламенения Условия, способствуюшие возникновению
- 27. Медленное окисление - химический процесс медленного взаимодействия вещества с кислородом без воспламенения вещества В ходе этого
- 28. Реакции веществ с кислородом - реакции окисления. Реакции окисления – составная часть окислительно – – восстановительных
- 29. Кислород входит в состав воды, которая составляет большую часть массы живых организмов и является внутренней средой
- 30. Кислород на Земле является окислителем № 1, т.к он обеспечивает протекание таких важных процессов, как: дыхание
- 31. Кислород используют В чистом виде: В металлургии – при получении чугуна, стали, цветных металлов ( для
- 32. Кислород расходуется в природе на процессы окисления (дыхания, гниения, горения) Масса кислорода в воздухе пополняется в
- 33. Приложение 1 «Вопросник к теме «Кислород» 1. Назовите восьмой элемент «Периодической системы химических элементов Д.И.Менделеева» (слайд
- 34. Приложение 1 «Вопросник к теме «Кислород» ( продолжение) 12. Как кислород получают в лаборатории? (слайды №
- 36. Скачать презентацию





























 Готовимся к экзамену по химии. 9 класс
Готовимся к экзамену по химии. 9 класс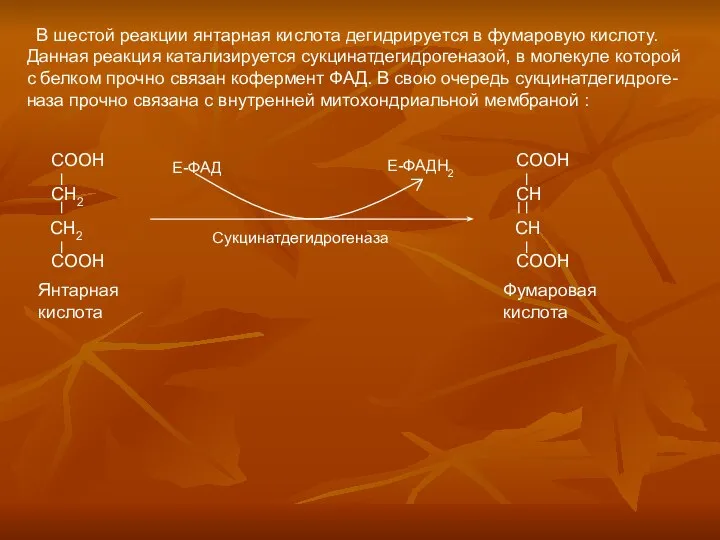 Аэробное окисление углеводов. (Часть 2)
Аэробное окисление углеводов. (Часть 2) Оксиды азота
Оксиды азота Классификация кислот
Классификация кислот Қатты күйдегі препараттар
Қатты күйдегі препараттар Полиамиды. Классификация по методу получения
Полиамиды. Классификация по методу получения Химический элемент платина
Химический элемент платина Щелочные металлы
Щелочные металлы Растворы (дисперсные системы)
Растворы (дисперсные системы) Тақырыпқа байланысты білімді жүйелеу
Тақырыпқа байланысты білімді жүйелеу II главная подгруппа ПС: Be, Mg, Ca, Sr, Ba, Ra
II главная подгруппа ПС: Be, Mg, Ca, Sr, Ba, Ra Выращивание кристалла медного купороса CuSO4*5Н2О в разных условиях
Выращивание кристалла медного купороса CuSO4*5Н2О в разных условиях Генетичний зв'язок
Генетичний зв'язок Презентация по Химии "РАСТВОРЫ" - скачать смотреть бесплатно
Презентация по Химии "РАСТВОРЫ" - скачать смотреть бесплатно Органічні розчинники. Їх застосування
Органічні розчинники. Їх застосування Получение этилена и опыты с ним. (Практическая работа 2)
Получение этилена и опыты с ним. (Практическая работа 2) Презентация по Химии "Ковалентная химическая связь" - скачать смотреть бесплатно
Презентация по Химии "Ковалентная химическая связь" - скачать смотреть бесплатно Основы химической термодинамики
Основы химической термодинамики Определение свободной поверхностной энергии тонких пленок оксидов
Определение свободной поверхностной энергии тонких пленок оксидов Внеурочная работа по химии. Краеведение
Внеурочная работа по химии. Краеведение Азотная кислота
Азотная кислота Жоғары температурағы асқын өткізгіштер
Жоғары температурағы асқын өткізгіштер Введение в биоорганическую химию. Пространственное и электронное строение органических соединений
Введение в биоорганическую химию. Пространственное и электронное строение органических соединений Исследовательская работа на тему: Удивительные свойства воды
Исследовательская работа на тему: Удивительные свойства воды “Кількість речовини. Молярна маса. Молярний об’єм” Урок хімії у 8 класі КЗ Верхівцевського НВК Учитель Кукса Наталія Миколаївна.
“Кількість речовини. Молярна маса. Молярний об’єм” Урок хімії у 8 класі КЗ Верхівцевського НВК Учитель Кукса Наталія Миколаївна.  Степень окисления
Степень окисления Презентация по Химии "Щавелевая кислота" - скачать смотреть
Презентация по Химии "Щавелевая кислота" - скачать смотреть  Количества вещества
Количества вещества