Содержание
- 2. ТЕРМОХИМИЯ Это раздел химии, изучающий тепловые эффекты химических реакций. Эндотермические реакции протекают с поглощением тепла. Экзотермические
- 3. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Она рассматривает приложение термодинамических законов и принципов к химическим процессам: Исследует энергетические ресурсы системы;
- 4. Позволяет определить направление протекания процессов; Так же позволяет учесть влияние различных факторов на протекание реакций.
- 5. ОСНОВНЫЕ ПОНЯТИЯ ТЕРМОДИНАМИКИ Термодинамическая система- изолированная часть пространства ,содержащая совокупность тел или тело с большим числом
- 6. ОНИ ДЕЛЯТСЯ НА Изолированные Закрытые Открытые
- 7. Изолированная- система, у которой отсутствует масса и телообмен со средой. Закрытая- система, которая обменивается со средой
- 8. ВИДЫ СИСТЕМ Гомогенная система- она состоит из одной фазы. Гетерогенная система- состоит из нескольких фаз.
- 9. Внутренняя энергия зависит от природы вещества, его количества, от его условий существования. При одинаковых условиях –
- 10. ЭНЕРГИЯ ГИББСА Самопроизвольное протекание изобарно – изотермического процесса определяется двумя факторами: энтальпийным, связанным с уменьшением энтальпии
- 11. При постоянном давлении и температуре (р=const, T=const) реакция самопроизвольно протекает в том направлении, которому отвечает убыль
- 12. Если ∆G > 0, то самопроизвольное протекание процесса в прямом направлении в данных условиях невозможно, а
- 13. При химическом взаимодействии одновременно изменяется энтальпия, характеризующая теплосодержание системы, и энтропия, характеризующая стремление системы к беспорядку.
- 14. Вклад энтальпийного и энтропийного Факторов в величину изобарно-изотермического потенциала во многом определяется температурой: При низких температурах
- 16. Скачать презентацию













 Простые вещества, металлы
Простые вещества, металлы Глобальні екологічні проблеми повязані з добуванням та переробкою вуглеводної сировини Підготувала учениця 11-А класу Гребі
Глобальні екологічні проблеми повязані з добуванням та переробкою вуглеводної сировини Підготувала учениця 11-А класу Гребі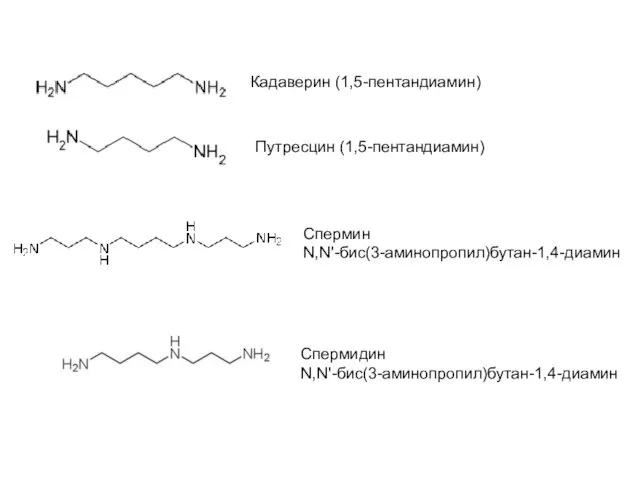 Бетаин (триметилглицин)
Бетаин (триметилглицин) Обобщающий урок по теме: Простые вещества Учитель химии I квалификационной категории Сучкова Н.В. 2009г.
Обобщающий урок по теме: Простые вещества Учитель химии I квалификационной категории Сучкова Н.В. 2009г. Русские ученые-химики
Русские ученые-химики Оксиды углерода (II) и (IV). Качественная реакция на углекислый газ
Оксиды углерода (II) и (IV). Качественная реакция на углекислый газ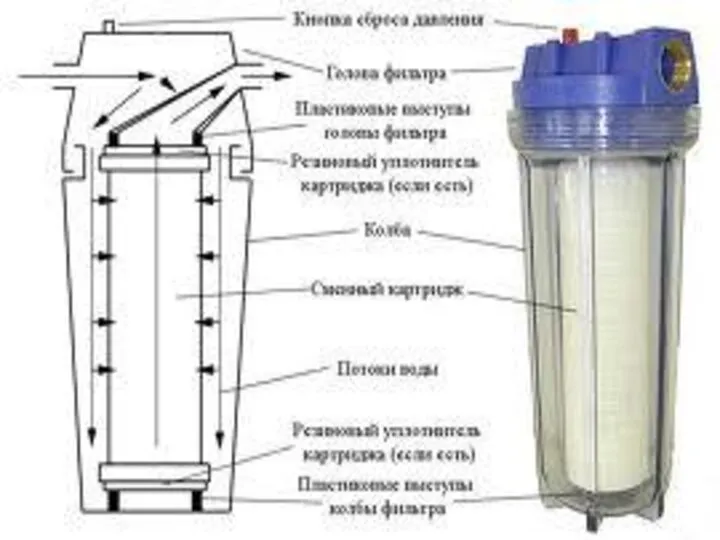 Суды тазарту әдістері
Суды тазарту әдістері Сероводород, сернистый водород
Сероводород, сернистый водород Карбонильные соединения
Карбонильные соединения Презентация на тему "Коллоидная химия"
Презентация на тему "Коллоидная химия" Источники сырья для производства полимера полиуретана, области применения, его свойства, объемы его производства
Источники сырья для производства полимера полиуретана, области применения, его свойства, объемы его производства Ерітінділер. Ерітінділердің химиялық теориясы
Ерітінділер. Ерітінділердің химиялық теориясы Углерод и его соединения
Углерод и его соединения Общая и неорганическая химия
Общая и неорганическая химия Органическая химия: «Жиры» Орлова Ольга Николаевна Школа №357 Приморского р-на.
Органическая химия: «Жиры» Орлова Ольга Николаевна Школа №357 Приморского р-на.  Альдегиды (номенклатура и изомерия)
Альдегиды (номенклатура и изомерия) Присадки к маслам
Присадки к маслам Алканы. Строение и свойства алканов
Алканы. Строение и свойства алканов Карбонові кислоти
Карбонові кислоти Открытия в химии Теория Александра Бутлерова
Открытия в химии Теория Александра Бутлерова Физические методы анализа
Физические методы анализа Презентация по химии Биополимеры и их компоненты
Презентация по химии Биополимеры и их компоненты  Характеристика высших гидроксидов по положению в ПСХЭ
Характеристика высших гидроксидов по положению в ПСХЭ Энергетика химических процессов. Энтропия и энергия Гиббса
Энергетика химических процессов. Энтропия и энергия Гиббса Стеариновая кислота
Стеариновая кислота Основные понятия аналитической химии. Положения теории растворов электролитов и закона действующих масс
Основные понятия аналитической химии. Положения теории растворов электролитов и закона действующих масс Роль химии в нашей жизни
Роль химии в нашей жизни Применение муравьиного спирта
Применение муравьиного спирта