Содержание
- 2. Молибденнің ашылу тарихы «молибден» атауы грек тіліндегі «молибдос»сөзінен шығады, аудармасы қорғасын дегенді білдіреді..
- 3. Вольфрамның ашылу тарихы
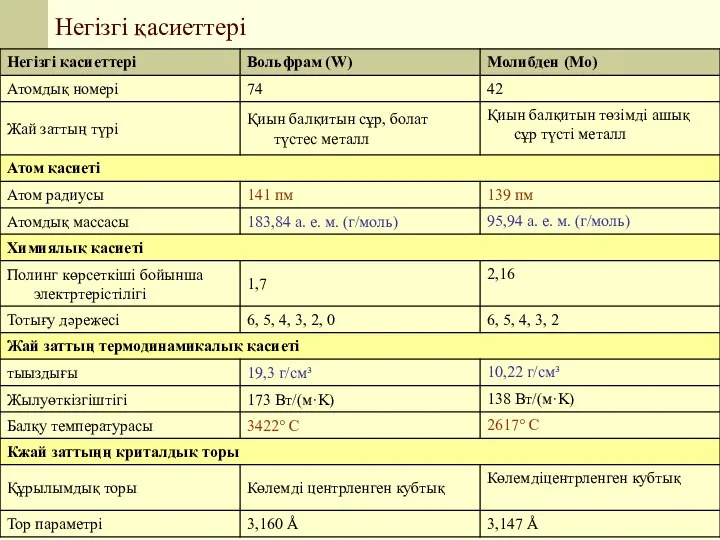
- 4. Негізгі қасиеттері
- 5. Молибденнің негізгі қасиеттері Ауада қалыпты температура кезінде молибден тұрақты. 400 °С температурада тотығады. 600 °С бастап,
- 6. Вольфрамның негізгі қасиеттері Қалыпты кезде вольфрам химиялық тұрақты. 400—500°С WO3-ке дейін тотығады.. 600°С су буы WO2
- 7. Вольфрам химиялық қасиеті 2 және 6 валентті болады.Соның ішіндегі ең тұрақтысы 6 валенттілігі. 3 және 2
- 8. Сутекпен әрекеттесуі Балқу температурасына дейін әрекеттеспейді Азотпен әрекеттесуі t > 2000 0С вольфрама нитридін WN2 түзеді
- 9. Оттекпен және оттекті қосылыстармен әрекеттесуі t =1000 -1200 оС әрекеттеседі WC және W2C түзеді
- 10. Галогенидтермен Фтормен бөлме температурасында Хлормен t = 800 0С Күкіртпен t > 400 0С Химические свойства
- 11. Қышқылдармен әрекеттесуі НF мен HNO3 қоспасында жақсы ериді азот қышқылы мен патша сұйығында тез ериді
- 12. Сілтілермен Сілті ерітіндісінде ерімейді Балқытылған сілтілерде әрекеттеседі
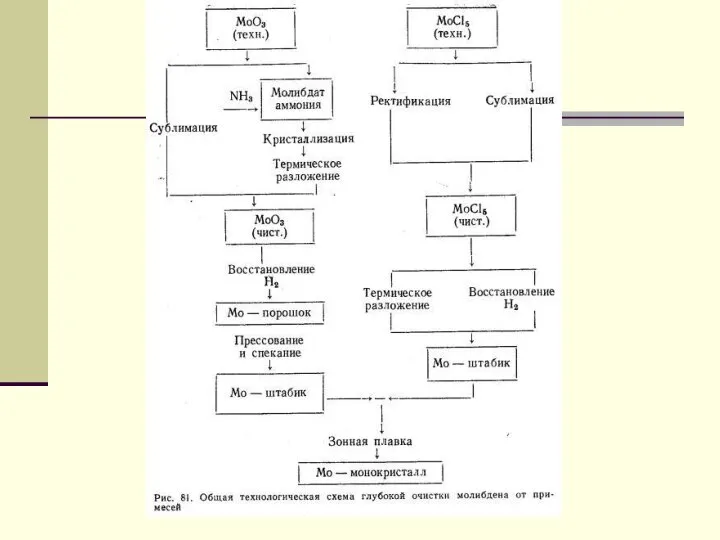
- 13. Молибденді бөліп алу әдістері 1. Экстракция 2. храмотография 3. сорбция 4. тұндыру
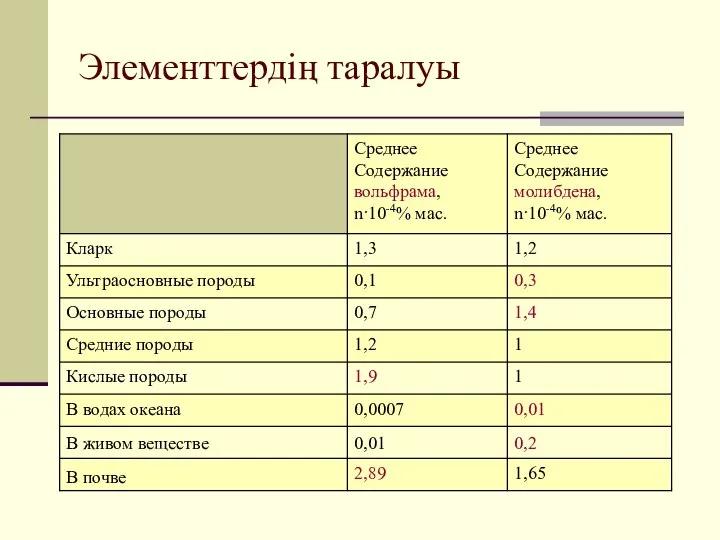
- 15. Элементтердің таралуы
- 16. Молибденнің минералдары Молибденнің 20-дан астам минералы белгілі . Ең көп кездесетіндері: - молибденит МоS2; - повеллит
- 17. Вульфенит PbМо04 Молибденит МоS2 Повеллит СаМо04 1 2 3
- 18. Вольфрама минералдары 20 түрлы минералы бар. Ең көп кездесетін минералы вольфрамитті топтары MnWO4 – FeWO4 және
- 19. Вольфрамит MnWO4 – FeWO4 Шеелит CaWO4 1 2
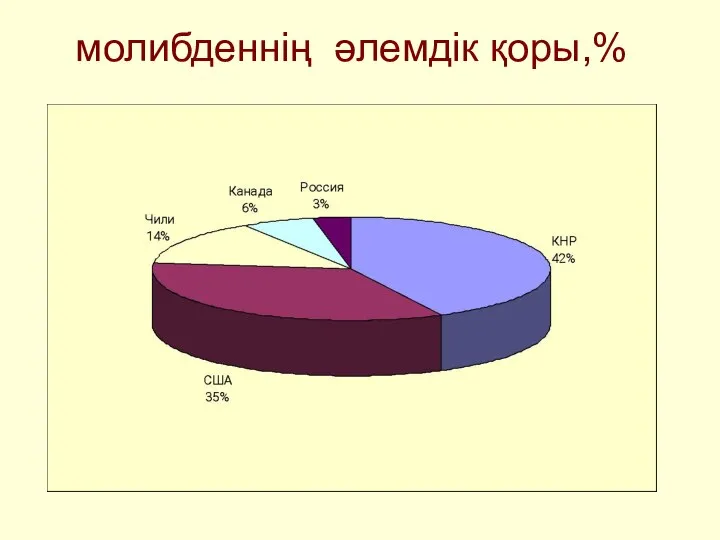
- 20. молибденнің әлемдік қоры,%
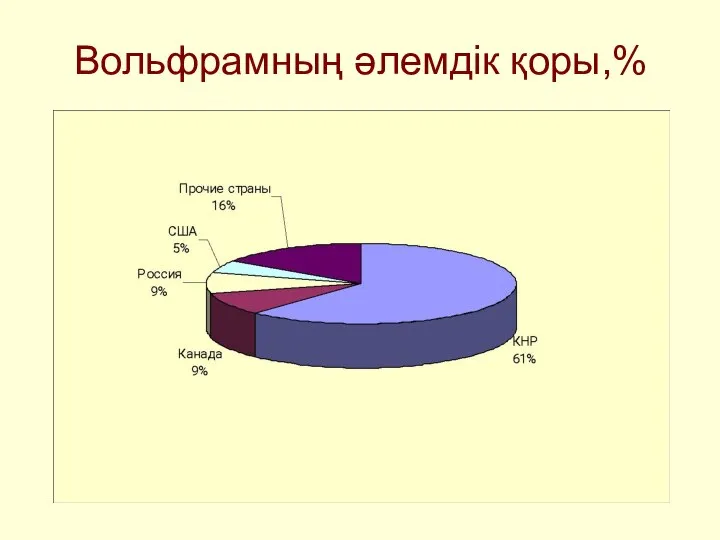
- 21. Вольфрамның әлемдік қоры,%
- 22. Молибденнің қолдану аясы Автомобиль Авиация Инструменттер және бөлшектер Өндірісте Металлдық молибден электрлік лампа Радиоламп Рентгендік түтікше
- 23. Вольфрамның қолдану аясы Металдық вольфрам электролампаларда қолданылатын электрлік жіпше, сваркада электрод ретінде, электрпештерінде қыздырыш ретінде 3000
- 25. Скачать презентацию

















 Презентация по Химии "Презентація про мене" - скачать смотреть
Презентация по Химии "Презентація про мене" - скачать смотреть  Фосфор
Фосфор Хімія у створенні нових матеріалів та побуті
Хімія у створенні нових матеріалів та побуті ОГЭ, вопрос 16 1-4
ОГЭ, вопрос 16 1-4 Начальные этапы обмена липидов
Начальные этапы обмена липидов Полимеры. Пластмассы. Волокна. Цели: - узнать что такое пластмассы, волокна их отличие от полимеров; - изучить классификацию пл
Полимеры. Пластмассы. Волокна. Цели: - узнать что такое пластмассы, волокна их отличие от полимеров; - изучить классификацию пл Презентация по Химии "«Сахароза»" - скачать смотреть бесплатно
Презентация по Химии "«Сахароза»" - скачать смотреть бесплатно Щавелевая кислота
Щавелевая кислота Хімічний елемент Літій
Хімічний елемент Літій Кислородные соединения азота. Азотная кислота
Кислородные соединения азота. Азотная кислота Предельные одноатомные спирты
Предельные одноатомные спирты Серебра нитрат и другие препараты серебра. Ртути окись желтая
Серебра нитрат и другие препараты серебра. Ртути окись желтая Посвящение в химики!
Посвящение в химики! Гормоны, как лекарственные вещества. Анализ, применение и хранение. (Тема 4)
Гормоны, как лекарственные вещества. Анализ, применение и хранение. (Тема 4) Узинская ООШ исслед.работа Лобановой Елизаветы
Узинская ООШ исслед.работа Лобановой Елизаветы ТБ в школе и в быту
ТБ в школе и в быту Твердые тела и их свойства
Твердые тела и их свойства  Геология и геохимия нефти и газа
Геология и геохимия нефти и газа Азотсодержащие органические соединения
Азотсодержащие органические соединения Lekcii_ - 2017-lech_ped 11
Lekcii_ - 2017-lech_ped 11 Юные химики
Юные химики Курсовая работа. Влияние микроэлементов на физиологические процессы
Курсовая работа. Влияние микроэлементов на физиологические процессы Материаловедение. Текстильные волокна, пряжа и ткань
Материаловедение. Текстильные волокна, пряжа и ткань Electrochemistry. Oxidation-reduction equilibrium in water solutions
Electrochemistry. Oxidation-reduction equilibrium in water solutions Презентация по Химии "Углерод" - скачать смотреть
Презентация по Химии "Углерод" - скачать смотреть  Химически опасные объекты (ХОО)
Химически опасные объекты (ХОО) Теория химического строения А. М. Бутлерова. Часть III
Теория химического строения А. М. Бутлерова. Часть III Платина. Свойства
Платина. Свойства