Содержание
- 2. Дисперсные системы – системы, состоящие из частиц одной фазы, распределенных в другой Диспергирование – процесс измельчения
- 3. Признаки дисперсной системы 1. Гетерогенность 2. Дисперсность С уменьшением размера частиц при дроблении вещества увеличивается дисперсность,
- 4. Свойства коллоидных растворов 1. Все коллоидные растворы способны рассеивать свет, т.е. опалесцировать. Опалесценция становится особенно заметна,
- 5. 2. Диффузия частиц в к.р. протекает медленно. 3. К.р. Имеют низкое осмотическое давление. Два последних свойства
- 6. 5. В отличие от истинных растворов к.р. неустойчивы. Коллоидно растворенное вещество способно выделяться (коагулировать) из раствора
- 7. Коагуляцию может вызвать нагревание, вымораживание, интенсивное перемешивание, введение в к.р. небольших количеств индифферентного электролита, ультразвуковые воздействия.
- 8. Коллоидные системы могут быть твердыми, жидкими и газообразными. Одно и то же вещество в зависимости от
- 9. Кол. Системы можно рассматривать как микрогетерогенные системы с предельной дисперсностью и огромной поверхностью раздела между дисперсной
- 10. Классификация ДС по дисперсности ДС Истинные растворы Меньше 10-7 см Коллоидные системы (золи) 10-7-10-5 см Микрогетерогенные
- 11. Классификация ДС по агрегатному состоянию ДС Т/Т сплавы Т/Ж лиозоли Т/Г, Ж/Г аэрозоли Ж/Ж эмуль сии
- 12. Классификация ДС по взаимодействию между частицами дисперсионной среды 1. Свободнодисперсные: частицы дисперсной фазы не связаны друг
- 13. Переход коллоидной системы из свободнодисперсного состояния в связнодисперсное – гелеобразование, образующиеся при этом структурированные коллоидные системы
- 14. Классификация ДС по межфазному взаимодействию 1. Лиофобные – слабое взаимодействие вещества дисперсной фазы со средой (лиозоли,
- 15. Ультрамикрогенные (коллоидные) системы или золи Признаки 1. Размер частиц дисперсной фазы от 2. Гетерогенность 3. Многокомпонентность
- 16. Ультрамикрогенные (коллоидные) системы или золи Общие условия получения 1. Нерастворимость вещества дисперсной фазы в дисперсионной среде
- 17. Методы получения коллоидных систем 1. Диспергирование – дробление крупных частиц грубодисперсных систем до коллоидной степени дисперсности
- 18. Диспергирование 1. Механическое – раздавливание, дробление, растирание крупных частиц суспензий, эмульсий, порошков 2. Ультразвуковое 3. Электрическое
- 19. Конденсация 1. Конденсация паров 2. Замена растворителя 3. Различные химические реакции
- 20. Очистка коллоидных систем Диализ, электродиализ, ультрафильтрация Основаны на способности молекул разных размеров или ионов проходить через
- 21. Строение коллоидной частицы Для образования коллоидных частиц необходимо три условия: Дисперсная фаза не должна растворяться в
- 22. Твердые частицы коллоидных систем называются мицеллами. Мицеллу образуют: 1. Ядро (агрегат), состоящее из большого числа атомов
- 23. Согласно правилу Фаянса-Пескова: «На поверхности ядра коллоидной частицы адсорбируются те ионы, которые могут достроить кристаллическую решетку
- 24. 3. Вокруг ПОИ располагается часть противоионов электролита –стабилизатора, образующих вместе с ПОИ адсорбционный слой. 4. Ядро
- 25. Двойной электрический слой (ДЭС) ДЭС – это слой, возникающийй на границе твердой и жидкой фазы мицеллы,
- 26. Строение ДЭС Твердая фаза Потенциалобразующие ионы Адсорбционный слой противоионов (слой по Гельмгольцу) Диффузный слой противоионов (слой
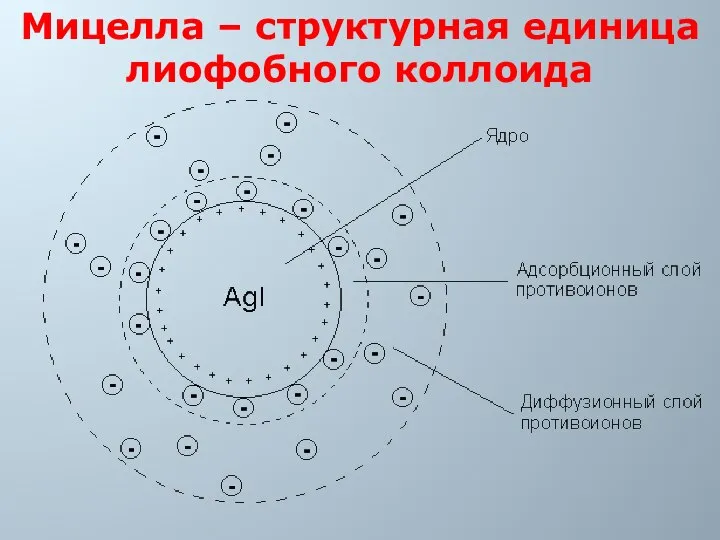
- 27. Мицелла – структурная единица лиофобного коллоида
- 28. Правило Панета-Фаянса-Пескова на поверхности ядра мицеллы адсорбируются ионы, имеющиеся в составе ядра, т.е. адсорбируются ионы, находящиеся
- 29. AgNO3 + KI = AgI + KNO3, {m [AgI]nI־ (n – x)K+}x־ г р а н
- 30. {m[AgI]nAg+(n- x)NO3 ־}x+xNO3־ (гранула положительна) {m[AgI]nI ־(n- x)K+}x־xK+ (гранула отрицательна)
- 31. Устойчивость коллоидных систем Дисперсные системы в отличие от истинных растворов являются термодинамически неустойчивыми. Под устойчивостью дисперсных
- 32. Русский ученый Н. Песков в 1925 году указал на два вида устойчивости: 1 . Кинетическая (седиментационная)
- 33. В 1968 году русский ученый В. Мишин предложил третий вид устойчивости: Конденсационная устойчивость – способность дисперсных
- 34. Седиментация - это явление оседания частиц достаточно большой массы под действием гравитационного поля. Грубодисперсные системы (пыль
- 35. К факторам, определяющим кинетическую устойчивость относят: -степень дисперсности коллоидных частиц - броуновское движение - вязкость дисперсной
- 36. Факторы, определяющие агрегативную устойчивость: - Наличие у коллоидных частиц одноименных зарядов, что мешает им соединиться в
- 37. Коагуляция коллоидных систем Нарушение агрегативной устойчивости коллоидной системы в сторону укрупнения частиц за счет их слипания
- 38. Электролитная коагуляция. Основные правила коагуляции: 1. Все электролиты могут вызвать коагуляцию. Но коагулирующим действием обладает только
- 39. Величина ПК зависит от величины заряда иона-коагулятора. Чем выше его валентность, тем меньшая концентрация электролита соответствует
- 40. Правило Шульце-Гарди Порог коагуляции обратно пропорционален шестой степени электрического заряда ионов-коагуляторов γс = k/Z6, k –
- 41. Порог коагуляции зависит от природы электролита и от валентности коагулирующего иона и вычисляют по формуле: γ
- 42. 3.Коагулирующая способность ионов одинаковой зарядности увеличивается с возрастанием радиуса иона. 4.Коагулирующее действие электролита не сводится только
- 43. Механизм коагуляции электролитами Происходит снятие электрического заряда, т.е. приведение коллоидной частицы в изоэлектрическое состояние (ζ =
- 44. СУСПЕНЗИИ – это взвеси порошков в жидкости (почвы и грунты, глиняное тесто, цементные и известковые растворы,
- 45. Эмульсии – это дисперсные системы, в которых и дисперсная фаза, и дисперсионная среда - жидкие. Степень
- 46. Вода и масло образуют эмульсии двух типов. Первый тип: вода – дисперсионная среда, масло – дисперсная
- 47. Различают эмульсии разбавленные и концентрированные. Разбавленные эмульсии (концентрация дисперсной фазы до 0,1 %) стабилизируются электролитами, создающими
- 48. Эмульгатор выбирается в соответствии с правилом: эмульсии М/В стабилизируются растворимыми в воде ВМС, например, белками, и
- 49. Эмульсии с концентрацией дисперсной фазы более 74 % называют желатинированными. По физическим свойствам они отличаются от
- 50. Пенами являются дисперсные системы, в которых дисперсная фаза – газ, а дисперсионная среда – жидкость, вытянутая
- 51. Для получения устойчивой пены необходимы стабилизаторы – пенообразователи, в качестве которых могут использоваться поверхностно-активные ВМС, мыла
- 52. Пена может быть получена встряхиванием раствора пенообразователя в цилиндре или пропусканием воздуха через пористый фильтр, помещенный
- 53. Время жизни пены определяется временем существования ее определенного объема с момента возникновения до полного разрушения или
- 54. АЭРОЗОЛИ. Аэрозоли играют важную роль в метеорологии, в сельском хозяйстве (дождевание, борьба с вредителями), в военном
- 55. Аэрозоли неустойчивы. Любой аэрозоль со временем разрушается. Грубодисперсные аэрозоли седиментируют. Высокодис аэрозоли разрушаются вследствие частых столкновений
- 57. Скачать презентацию


























![AgNO3 + KI = AgI + KNO3, {m [AgI]nI־ (n –](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1400068/slide-28.jpg)
![{m[AgI]nAg+(n- x)NO3 ־}x+xNO3־ (гранула положительна) {m[AgI]nI ־(n- x)K+}x־xK+ (гранула отрицательна)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1400068/slide-29.jpg)

























 Модифицированные природные полимеры. Их свойства
Модифицированные природные полимеры. Их свойства Химия элементов. Комплексные соединения. Основные понятия координационной теории. Номенклатура. Поведение в растворе
Химия элементов. Комплексные соединения. Основные понятия координационной теории. Номенклатура. Поведение в растворе Методы получения органических галогенидов
Методы получения органических галогенидов Папайя-сarica papaya L. Сырьё - fructus caricae. Семейство кариковые caricaceae
Папайя-сarica papaya L. Сырьё - fructus caricae. Семейство кариковые caricaceae Классификация кислот
Классификация кислот Способы выражения состава раствора. Решение задач
Способы выражения состава раствора. Решение задач Классификация минералов
Классификация минералов Химическая формула. Относительная атомная и относительная молекулярная массы
Химическая формула. Относительная атомная и относительная молекулярная массы Презентация по Химии "Самородки" - скачать смотреть бесплатно__
Презентация по Химии "Самородки" - скачать смотреть бесплатно__ Осадительное титрование
Осадительное титрование ОГЭ, вопрос 16 1-4
ОГЭ, вопрос 16 1-4 АНРИ ЛУИ ЛЕ ШАТЕЛЬЕ Презентацию подготовили: Ефимова Евгения, Муравьева Татьяна, ученицы 11А класса МОУ СОШ № 1 Карасукского рай
АНРИ ЛУИ ЛЕ ШАТЕЛЬЕ Презентацию подготовили: Ефимова Евгения, Муравьева Татьяна, ученицы 11А класса МОУ СОШ № 1 Карасукского рай Альдегіди і кетони аліфатичного ряду. Альдегіди і кетони ароматичного ряду
Альдегіди і кетони аліфатичного ряду. Альдегіди і кетони ароматичного ряду Термодинамика химических процессов
Термодинамика химических процессов Биогеохимические функции и принципы живого вещества
Биогеохимические функции и принципы живого вещества Вивчення особливостей застосування детекторів дорогоцінних каменів та каратомірів
Вивчення особливостей застосування детекторів дорогоцінних каменів та каратомірів Химическая термодинамика и биоэнергетика. Второй закон термодинамики
Химическая термодинамика и биоэнергетика. Второй закон термодинамики Этиленгликоль. Физические свойства
Этиленгликоль. Физические свойства Количественные измерения в химии. Количество вещества. Моль
Количественные измерения в химии. Количество вещества. Моль Карбон қышқылдары
Карбон қышқылдары Гидролиз. Применение гидролиза. (11 класс)
Гидролиз. Применение гидролиза. (11 класс) Жёсткость воды. Способы умягчения воды в быту; на производстве
Жёсткость воды. Способы умягчения воды в быту; на производстве Кислоты
Кислоты Презентація з хімії на тему:”Спирт.Загальні відомості про спирт” підготували: учениці 11-А класу Харківської ЗОШ І-ІІІ ступенів №102 Антіпова Марія і Уськіна Ольга
Презентація з хімії на тему:”Спирт.Загальні відомості про спирт” підготували: учениці 11-А класу Харківської ЗОШ І-ІІІ ступенів №102 Антіпова Марія і Уськіна Ольга  Дисперсные системы и растворы
Дисперсные системы и растворы Интересные факты о нефти
Интересные факты о нефти Подкласс Иносиликаты (цепочечные/ленточные силикаты)
Подкласс Иносиликаты (цепочечные/ленточные силикаты) Актиний. Нахождение в природе
Актиний. Нахождение в природе