Содержание
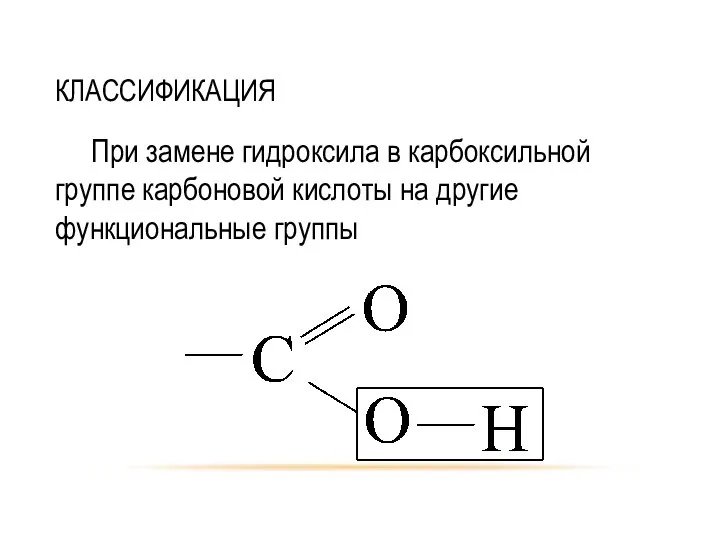
- 2. КЛАССИФИКАЦИЯ При замене гидроксила в карбоксильной группе карбоновой кислоты на другие функциональные группы
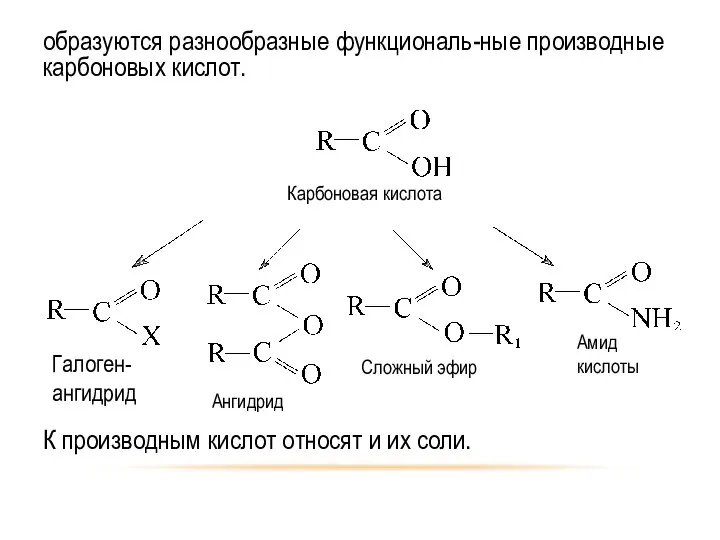
- 3. образуются разнообразные функциональ-ные производные карбоновых кислот. К производным кислот относят и их соли.
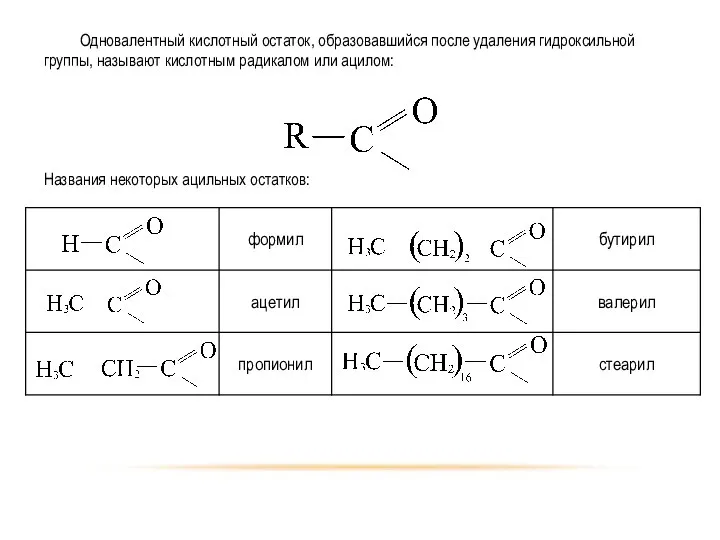
- 4. Одновалентный кислотный остаток, образовавшийся после удаления гидроксильной группы, называют кислотным радикалом или ацилом: Названия некоторых ацильных
- 5. АНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
- 6. ПОЛУЧЕНИЕ Из карбоновых кислот при их термической ангидридизации или при взаимодействии с сильными водоотнимающими реагентами (P2O5,
- 7. ФИЗИЧЕСКИЕ СВОЙСТВА Ангидриды карбоновых кислот являются бесцветными жидкостями или кристаллическими веществами. Первые представители гомологического ряда имеют
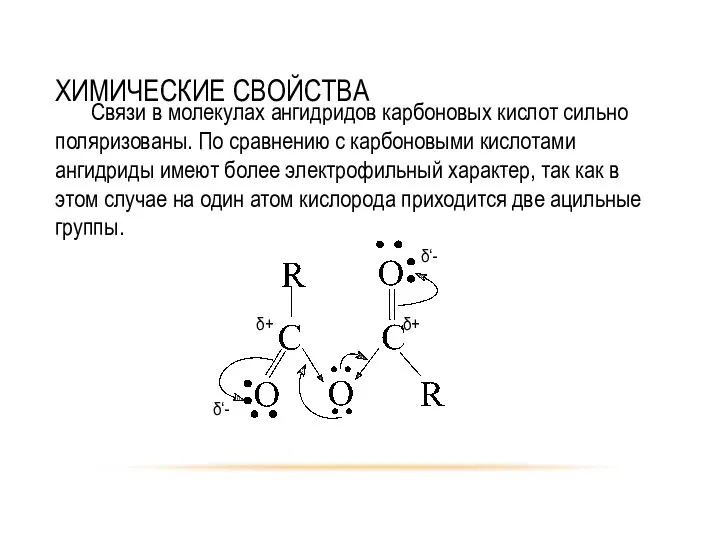
- 8. ХИМИЧЕСКИЕ СВОЙСТВА Связи в молекулах ангидридов карбоновых кислот сильно поляризованы. По сравнению с карбоновыми кислотами ангидриды
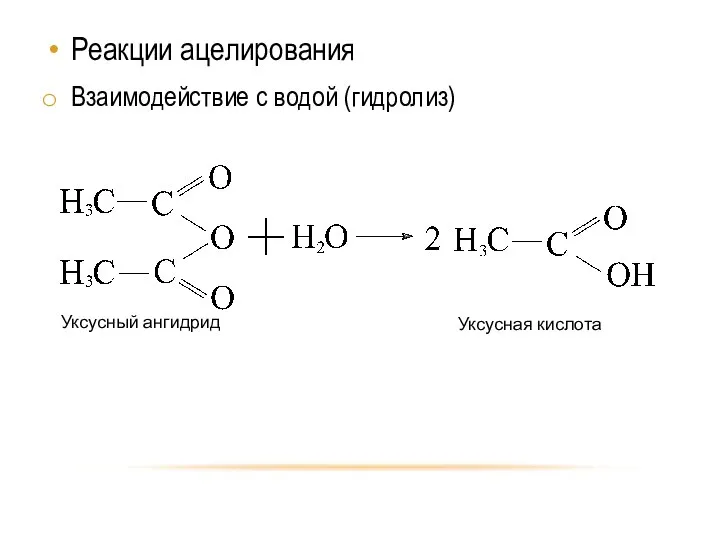
- 9. Реакции ацелирования Взаимодействие с водой (гидролиз)
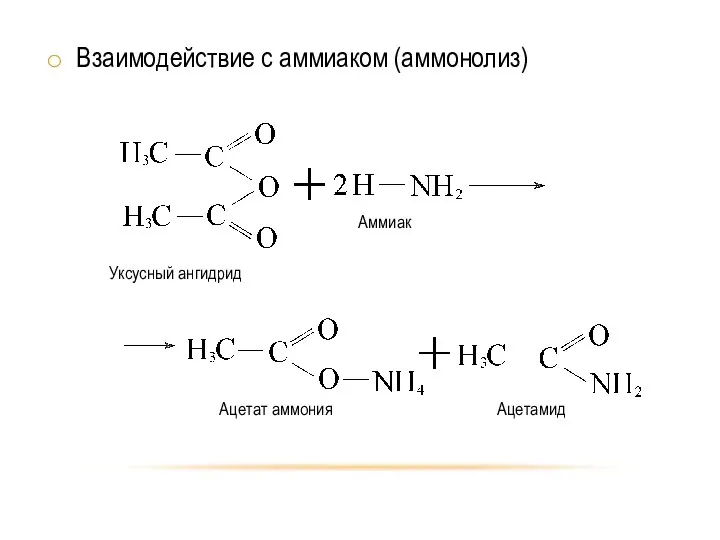
- 10. Взаимодействие с аммиаком (аммонолиз)
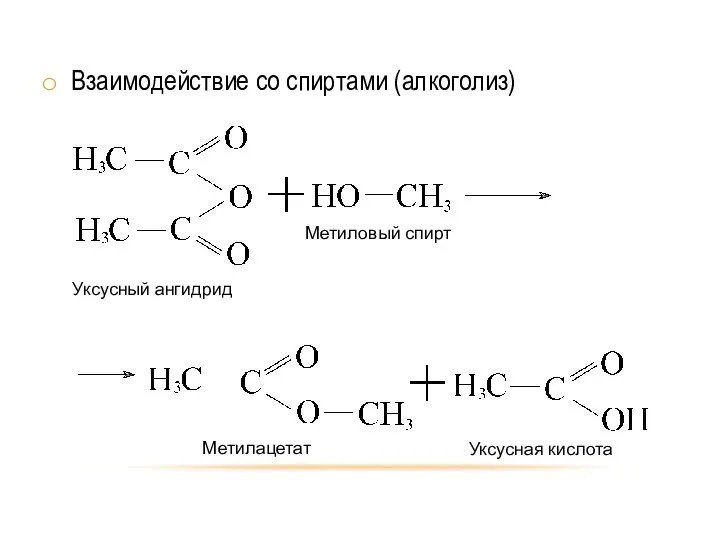
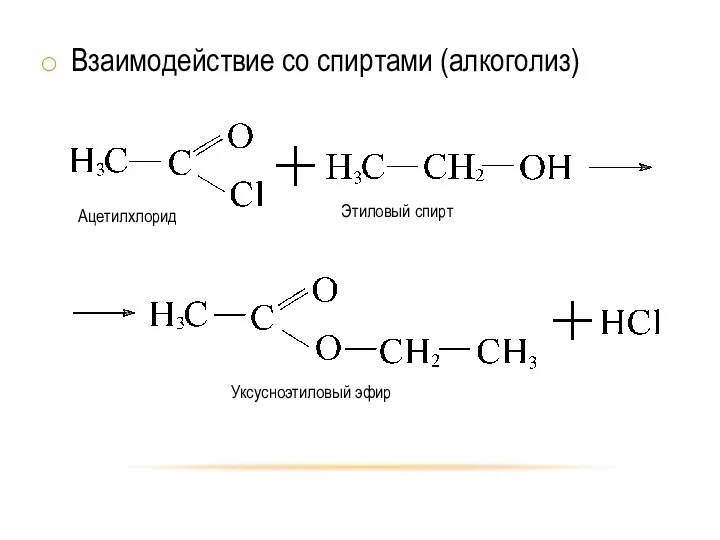
- 11. Взаимодействие со спиртами (алкоголиз)
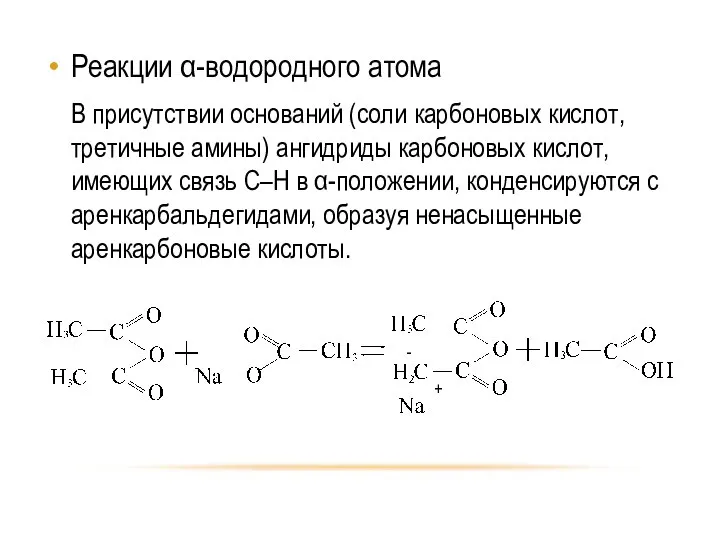
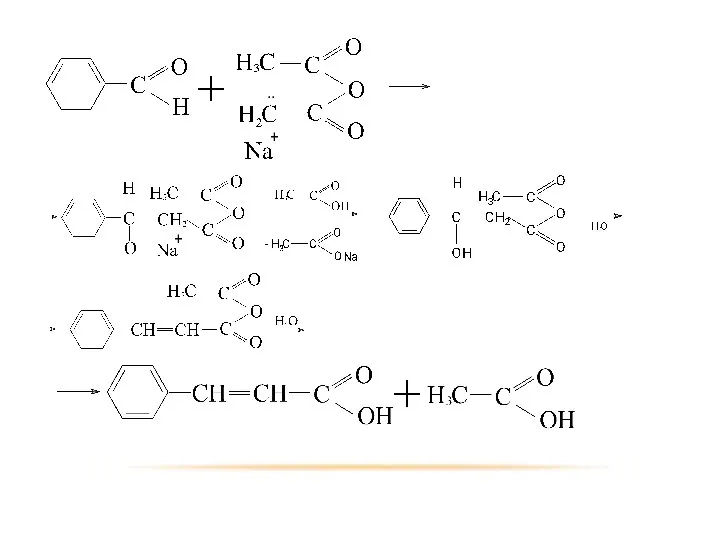
- 12. Реакции α-водородного атома В присутствии оснований (соли карбоновых кислот, третичные амины) ангидриды карбоновых кислот, имеющих связь
- 13. +
- 14. ПРИМЕНЕНИЕ В качестве ацилирующих агентов (получение ацетилцеллюлозы, лекарственных средств) (уксусный ангидрид) Для получения полимеров (сополимеры со
- 15. ГАЛОГЕНАНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
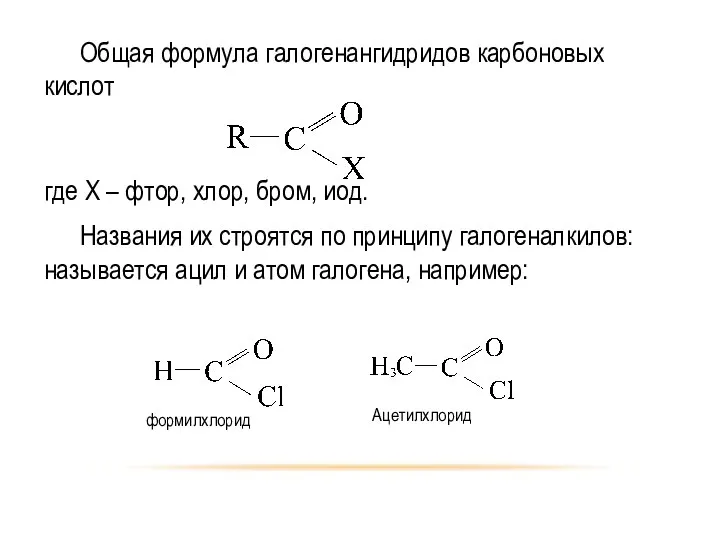
- 16. Общая формула галогенангидридов карбоновых кислот где Х – фтор, хлор, бром, иод. Названия их строятся по
- 17. ПОЛУЧЕНИЕ Галогенангидриды карбоновых кислот образуются при действии галогенидов фосфора (PCl3, PCl5) и тионилхлорида (SOCl2) на кислоты
- 18. ФИЗИЧЕСКИЕ СВОЙСТВА Галогенангидриды карбоновых кислот (ацилгалогениды) представляют собой бесцветные жидкости или кристаллические вещества с острым запахом,
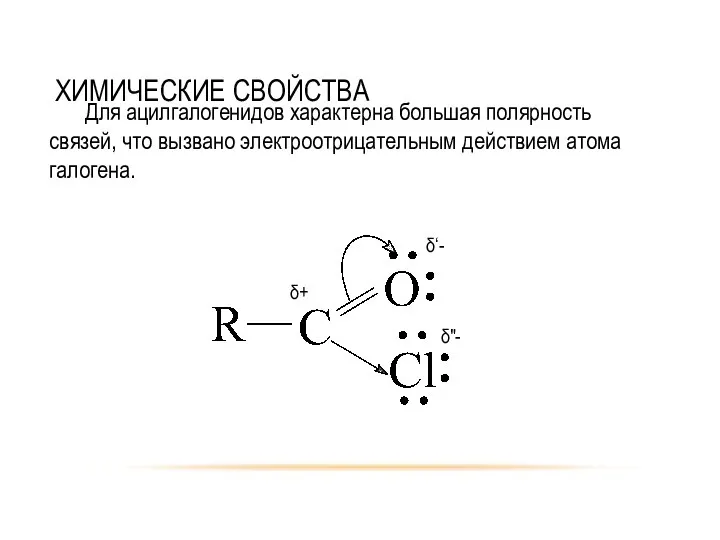
- 19. ХИМИЧЕСКИЕ СВОЙСТВА Для ацилгалогенидов характерна большая полярность связей, что вызвано электроотрицательным действием атома галогена.
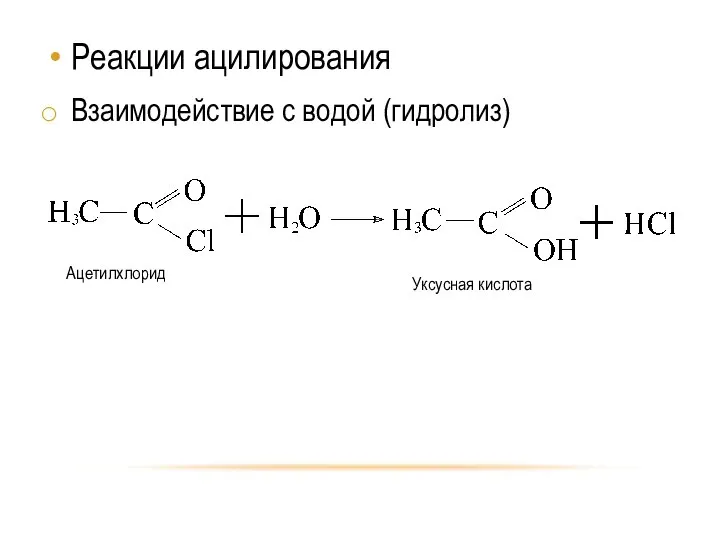
- 20. Реакции ацилирования Взаимодействие с водой (гидролиз)
- 21. Взаимодействие со спиртами (алкоголиз)
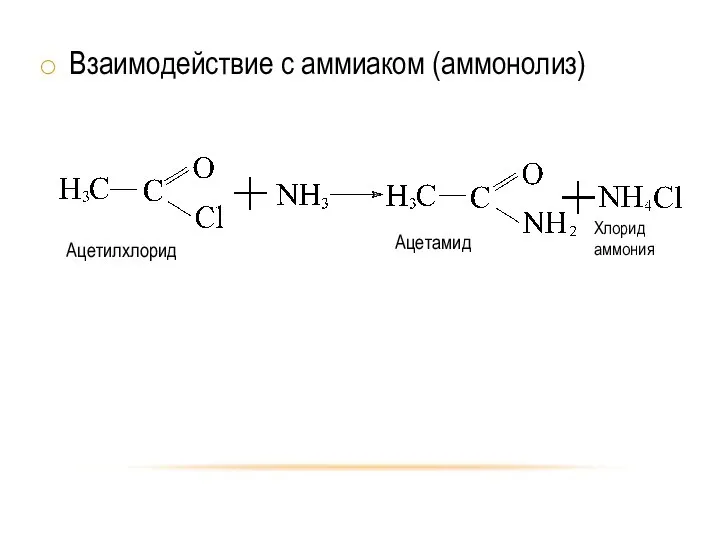
- 22. Взаимодействие с аммиаком (аммонолиз)
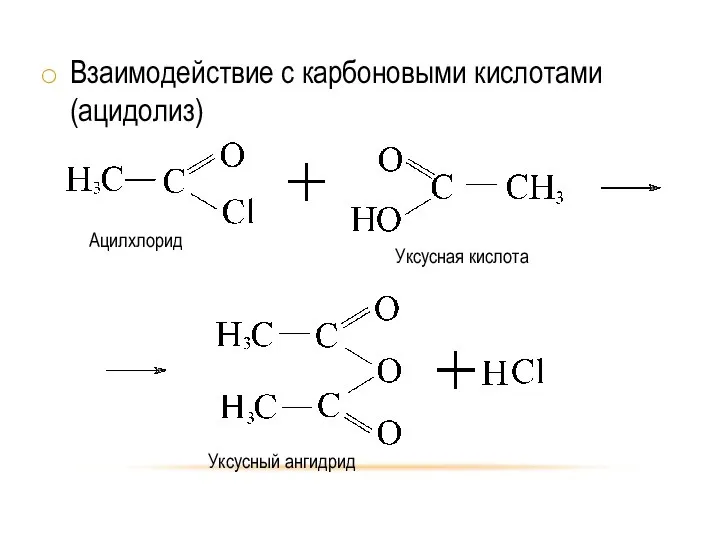
- 23. Взаимодействие с карбоновыми кислотами (ацидолиз)
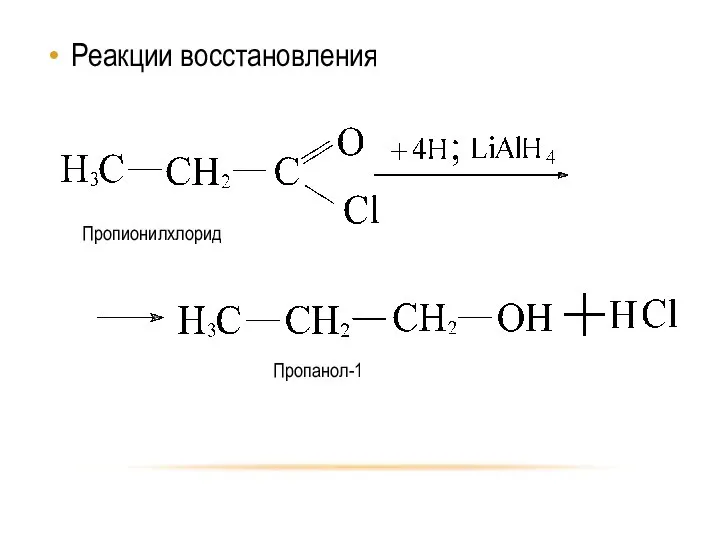
- 24. Реакции восстановления Пропионилхлорид Пропанол-1
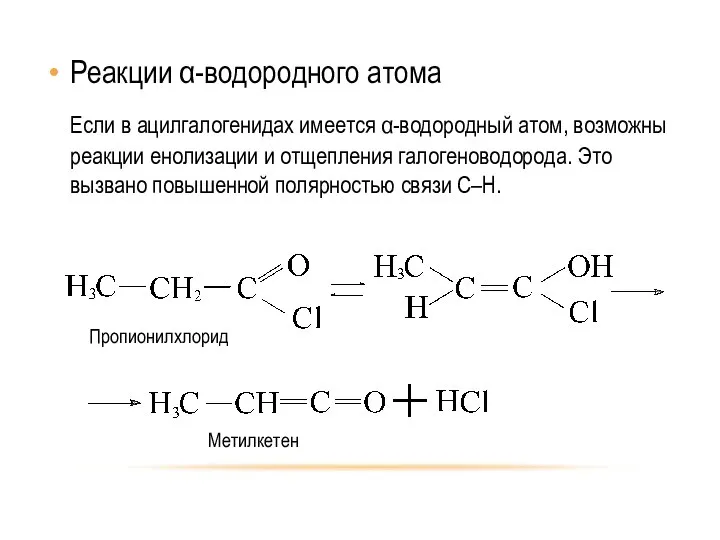
- 25. Реакции α-водородного атома Если в ацилгалогенидах имеется α-водородный атом, возможны реакции енолизации и отщепления галогеноводорода. Это
- 26. ПРИМЕНЕНИЕ Ацилгалогениды применяются в основном для органического синтеза.
- 27. АМИДЫ КАРБОНОВЫХ КИСЛОТ
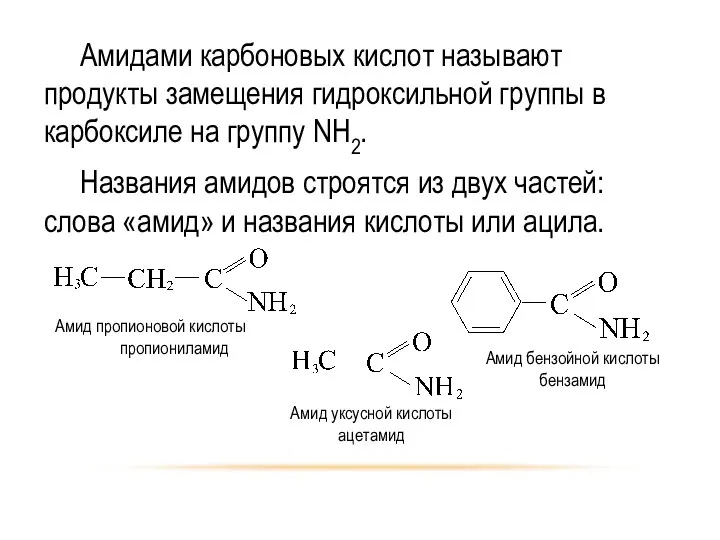
- 28. Амидами карбоновых кислот называют продукты замещения гидроксильной группы в карбоксиле на группу NH2. Названия амидов строятся
- 29. СПОСОБЫ ПОЛУЧЕНИЯ Действие аммиака на хлорангидриды карбоновых кислот. (см. химические свойства галогенангидридов карбоновых кислот). Сухая перегонка
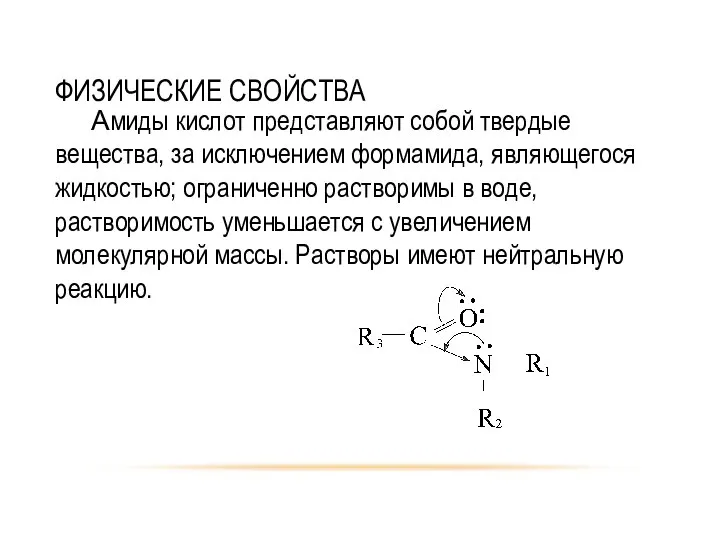
- 30. ФИЗИЧЕСКИЕ СВОЙСТВА Амиды кислот представляют собой твердые вещества, за исключением формамида, являющегося жидкостью; ограниченно растворимы в
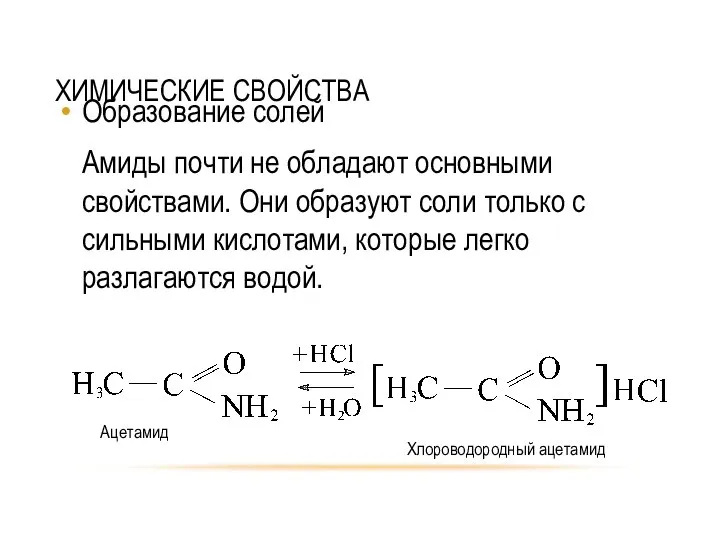
- 31. ХИМИЧЕСКИЕ СВОЙСТВА Образование солей Амиды почти не обладают основными свойствами. Они образуют соли только с сильными
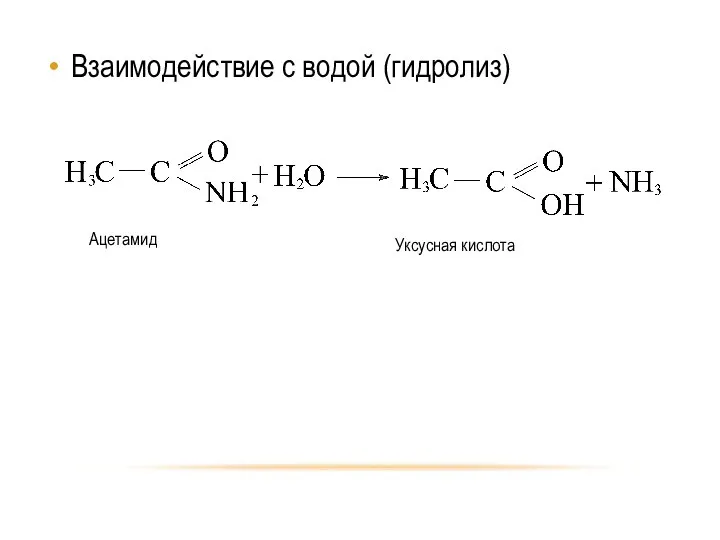
- 32. Взаимодействие с водой (гидролиз)
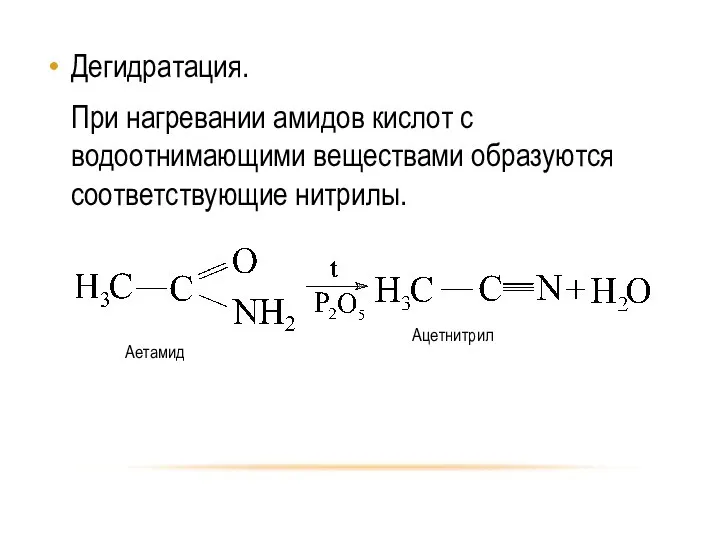
- 33. Дегидратация. При нагревании амидов кислот с водоотнимающими веществами образуются соответствующие нитрилы.
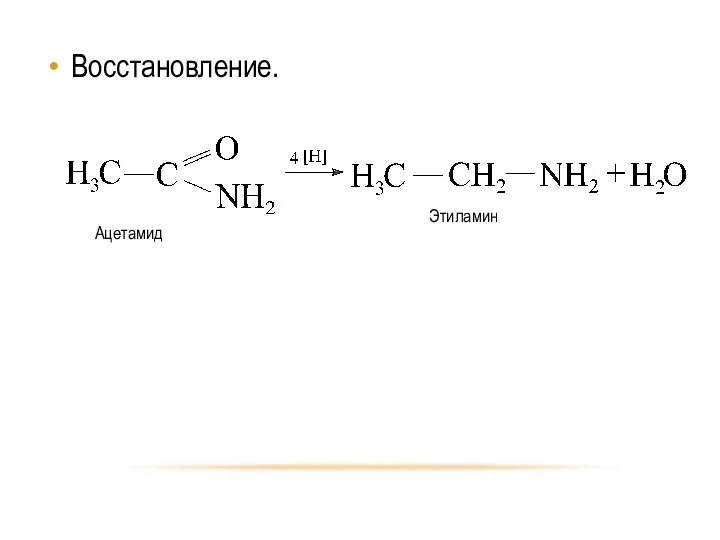
- 34. Восстановление.
- 35. СЛОЖНЫЕ ЭФИРЫ КАРБОНОВЫХ КИСЛОТ
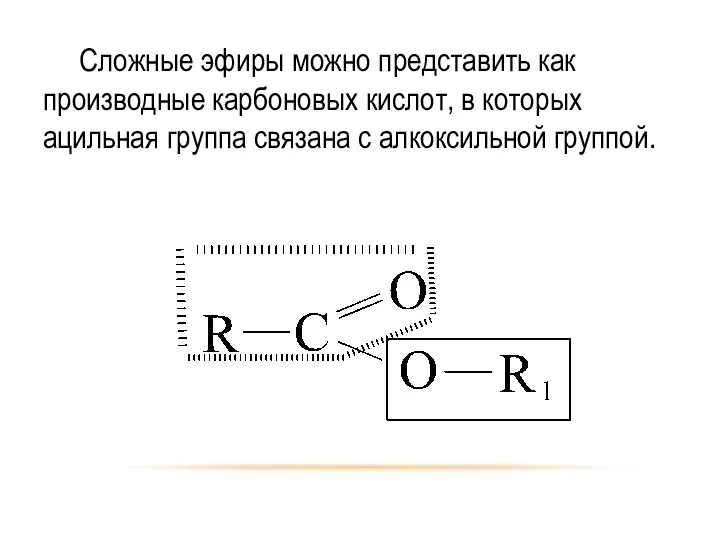
- 36. Сложные эфиры можно представить как производные карбоновых кислот, в которых ацильная группа связана с алкоксильной группой.
- 37. НОМЕНКЛАТУРА По рациональной номенклатуре наименование эфира строится из двух частей: названия кислоты и спиртового радикала. По
- 39. ИЗОМЕРИЯ. Изомерия сложных эфиров определяется изомерией кислотных и спиртовых остатков.
- 40. НАХОЖДЕНИЕ В ПРИРОДЕ. Сложные эфиры широко представлены в природе, но обычно в небольших количествах. Они участвуют
- 41. СИНТЕТИЧЕСКИЕ СПОСОБЫ ПОЛУЧЕНИЯ. Реакция этерификации. (см. химические свойства карбоновых кислот или спиртов) Значительно легче и несравнимо
- 42. Взаимодействие хлорангидридов или ангидридов карбоновых кислот со спиртами или фенолами. (см. химические свойства ацилгалогенидов или ангидридов)
- 43. ФИЗИЧЕСКИЕ СВОЙСТВА. Сложные эфиры низкомолекулярных и среднемолекулярных кислот и спиртов – жидкости с приятным фруктовым запахом,
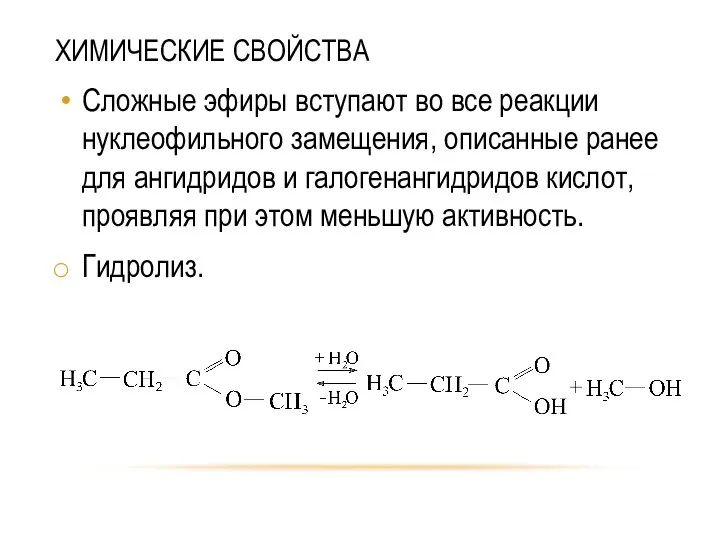
- 44. ХИМИЧЕСКИЕ СВОЙСТВА Сложные эфиры вступают во все реакции нуклеофильного замещения, описанные ранее для ангидридов и галогенангидридов
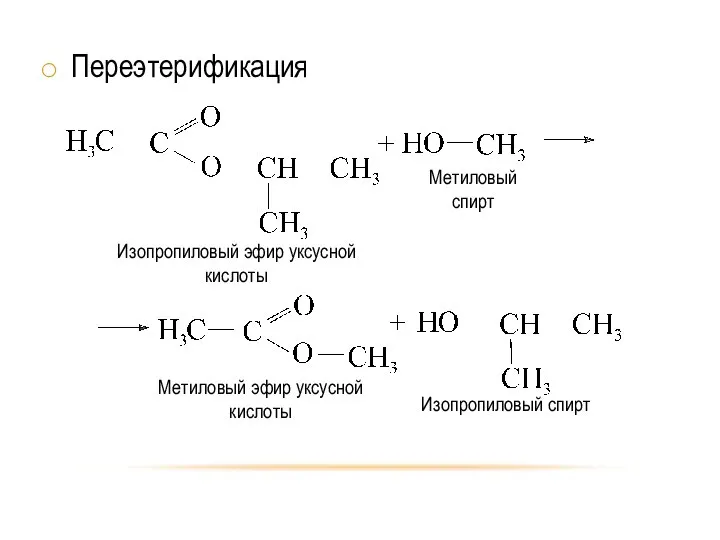
- 45. Переэтерификация
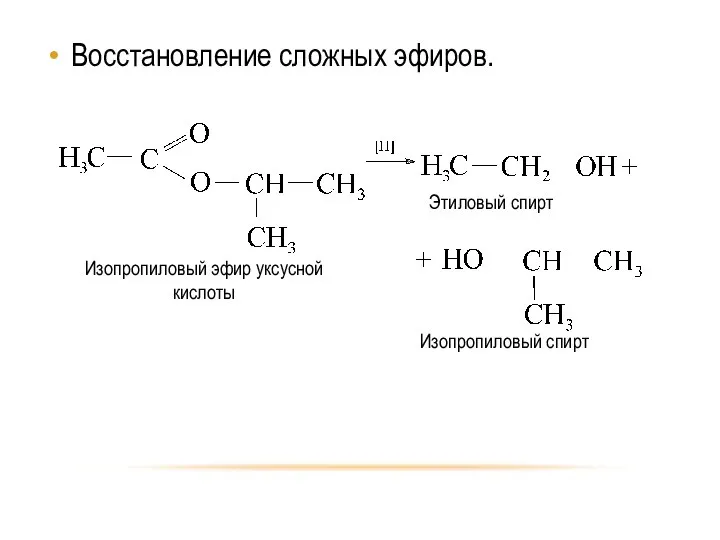
- 46. Восстановление сложных эфиров.
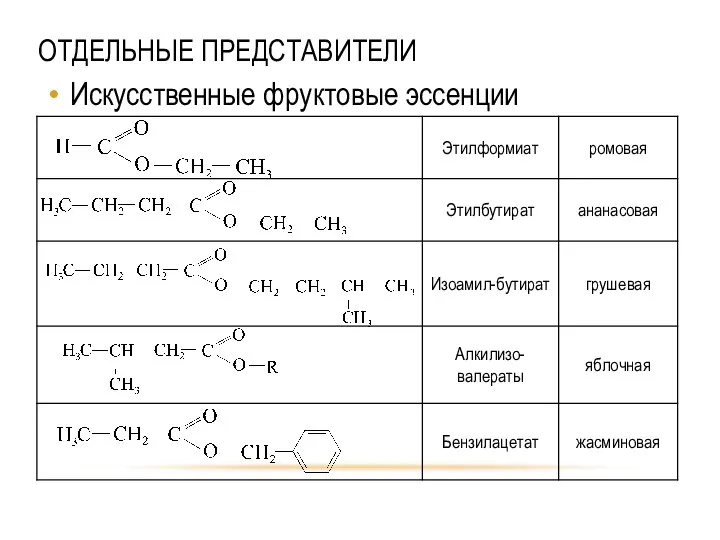
- 47. ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ Искусственные фруктовые эссенции
- 48. Природные сложные эфиры относят к липидам. Различают: Простые липиды – жиры, воски, стеролы и стериды. Сложные
- 49. ПРОСТЫЕ ЛИПИДЫ Жиры и масла – сложные эфиры высших жирных кислот (насыщенных и ненасыщенных) и глицерина.
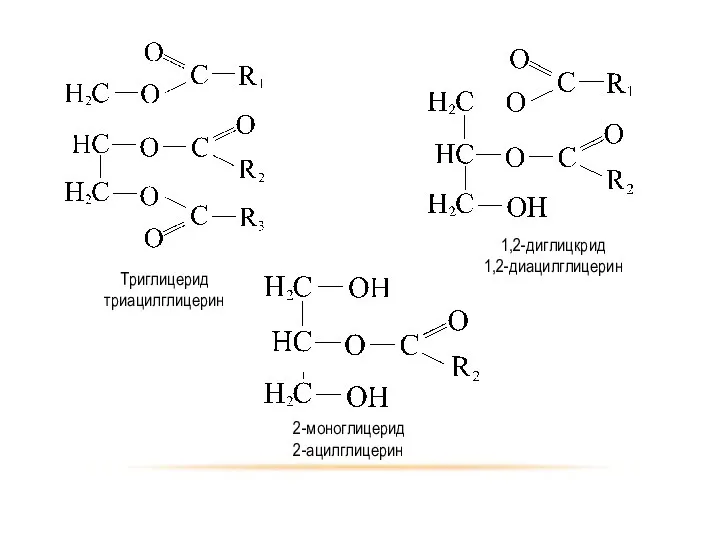
- 50. Триглицерид триацилглицерин 1,2-диглицкрид 1,2-диацилглицерин 2-моноглицерид 2-ацилглицерин
- 51. Кислоты жиров
- 53. ИЗОМЕРИЯ Изомерия глицеридов связана с различным положением ацилов в молекуле, их различным строением, положением двойных связей:
- 54. ФИЗИЧЕСКИЕ СВОЙСТВА Триглицериды – жидкости или твердые вещества без цвета, вкуса и запаха, нерастворимы в воде,
- 55. ХИМИЧЕСКИЕ СВОЙСТВА Глицериды вступают во все реакции характерные для сложных эфиров: Гидролиз. Протекает в присутствии кислот
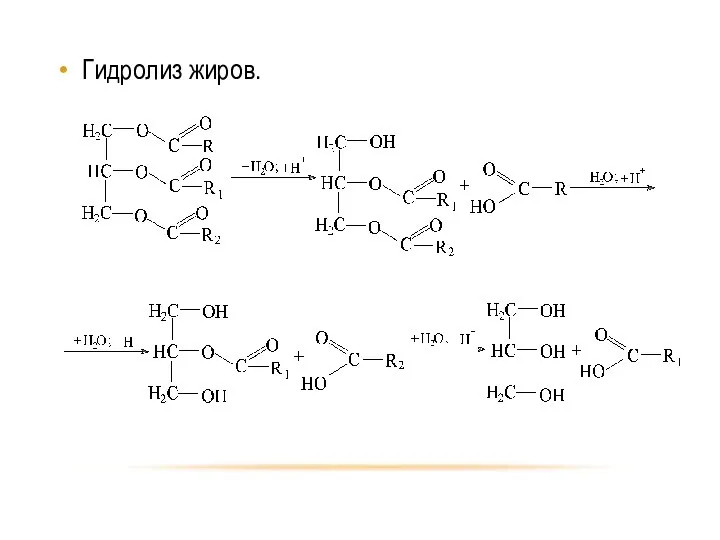
- 56. Гидролиз жиров.
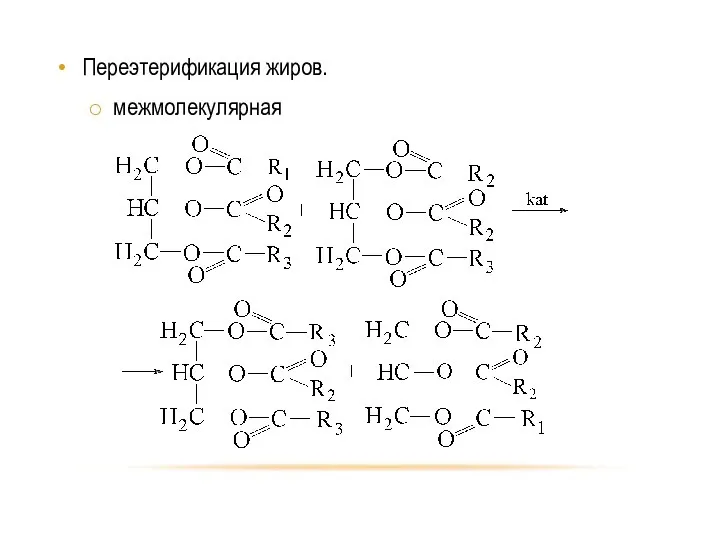
- 57. Переэтерификация жиров. межмолекулярная
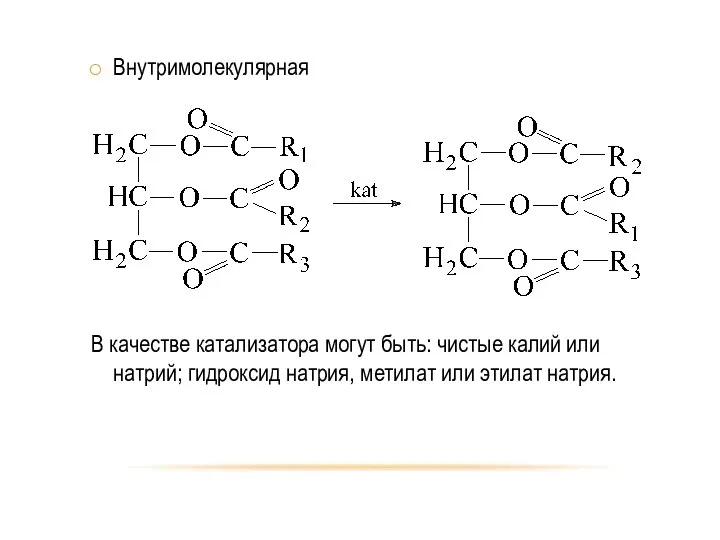
- 58. Внутримолекулярная В качестве катализатора могут быть: чистые калий или натрий; гидроксид натрия, метилат или этилат натрия.
- 59. Алкоголиз жиров.
- 60. В качестве катализаторов при алкоголизе применяют гидроксид натрия, алкоголяты щелочных металлов, серную кислоту, хлороводород. Алкоголиз применяют
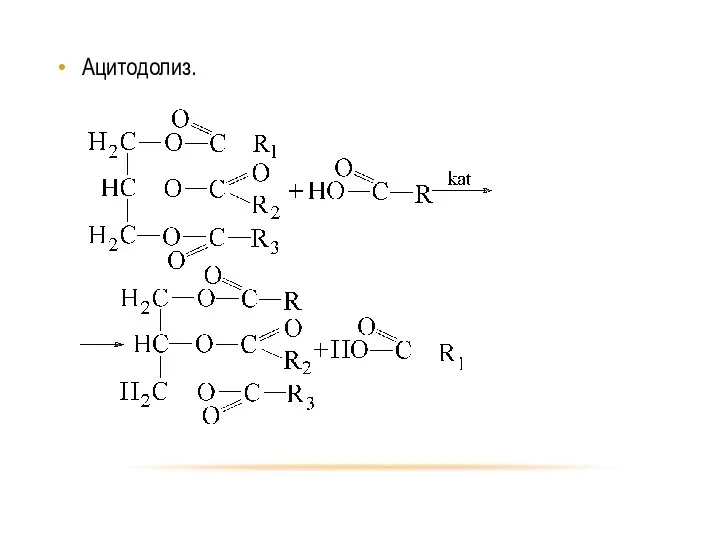
- 61. Ацитодолиз.
- 62. Реакция ацитодолиза протекает в присутствии серной кислоты, воды или трифторида бора. Реакция ускоряется с увеличением силы
- 63. Гидрогенизация жиров. Гидрирование жиров молекулярным водородом в промышленности проводят при температурах 180 ÷ 240°С в присутствии
- 65. Окисление жиров. Жиры и масла, особенно содержащие радикалы ненасыщенных жирных кислот, окисляются кислородом воздуха. Начальными (первичными)
- 66. Воски. Сложные эфиры высокомолекулярных одноосновных карбоновых кислот и однотомных высокомолекулярных спиртов. В состав восков входят главным
- 67. Воски широко распространены в природе. Воски покрывают тонким слоем листья, стебли и плоды растений. Из растительных
- 68. Спермацет – твердый кристаллический продукт белого цвета, состоящий в основном из цетилового эфира пальмитиновой кислоты. Выделяют
- 69. Пчелиный воск получают из пчелиных сот вытапливаемый или экстракцией после удаления меда. Он состоит главным образом
- 70. СЛОЖНЫЕ ЛИПИДЫ Фосфатиды – липиды, дающие при гидролизе глицерин, высшие монокарбоновые кислоты, фосфорную кислоту и аминоспирты
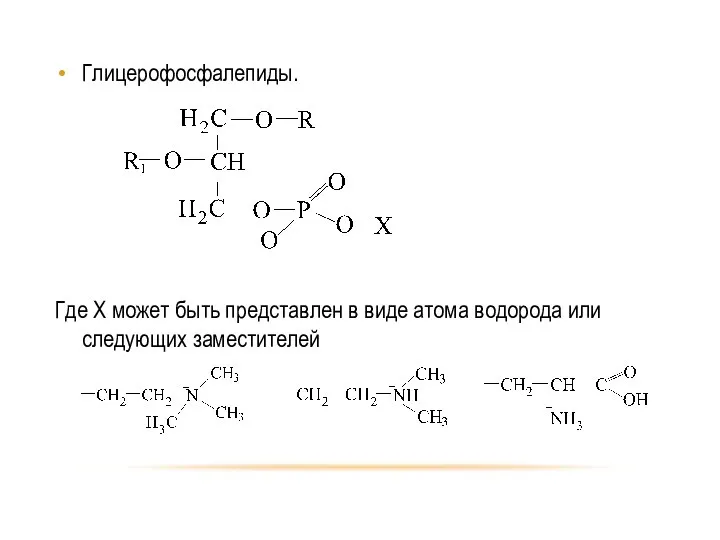
- 71. Глицерофосфалепиды. Где X может быть представлен в виде атома водорода или следующих заместителей
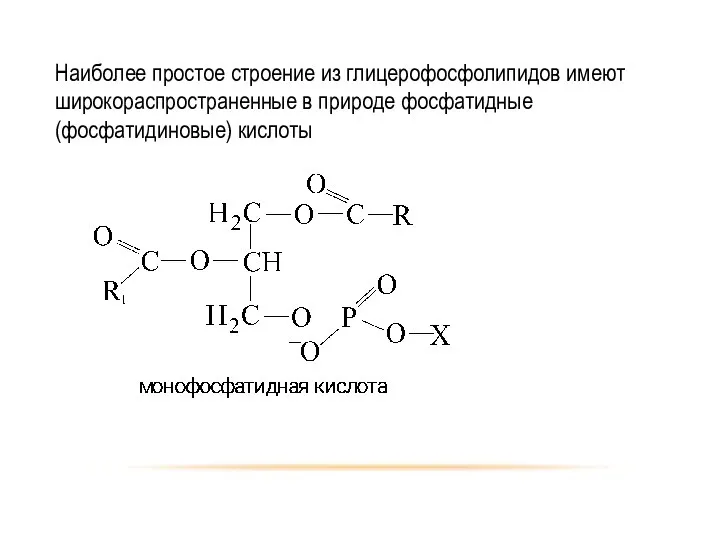
- 72. Наиболее простое строение из глицерофосфолипидов имеют широкораспространенные в природе фосфатидные (фосфатидиновые) кислоты
- 73. В растениях, микроорганизмах и некоторых животных тканях обнаружены молекулы, построенные из нескольких остатков фосфатидных кислот, например
- 74. Наиболее распространены среди фосфолипидов фосфатидилхолины (в их молекулах X представлен остатком аминоспирта холина) и фосфатидиэтаноламины (в
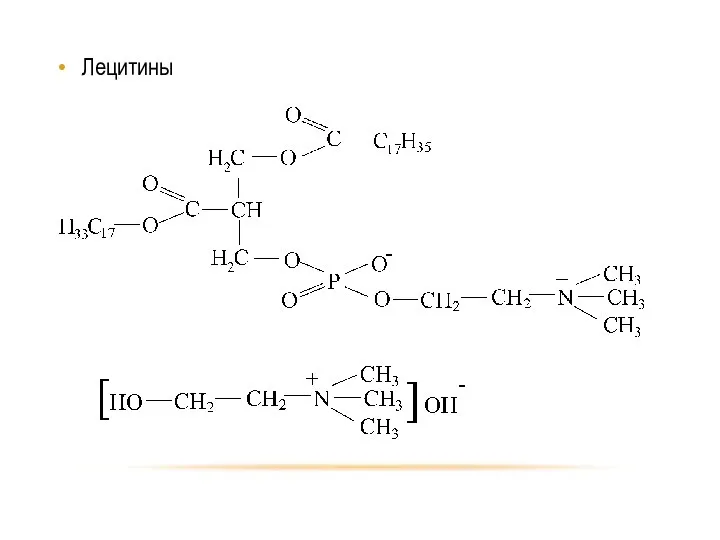
- 75. Лецитины
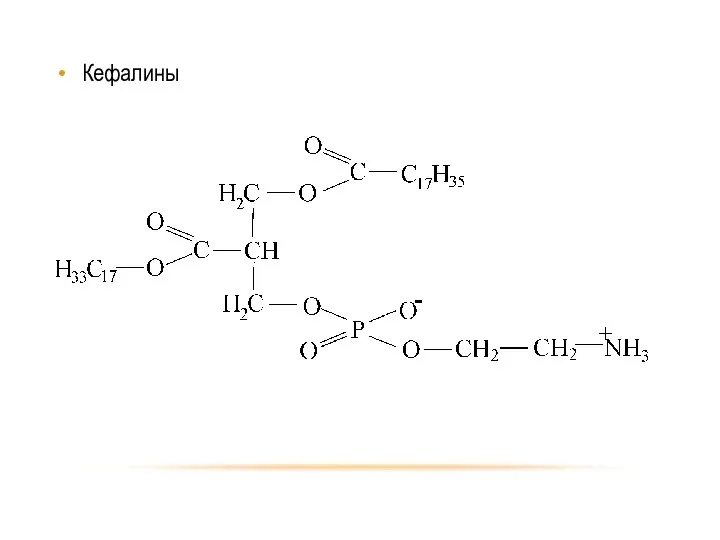
- 76. Кефалины
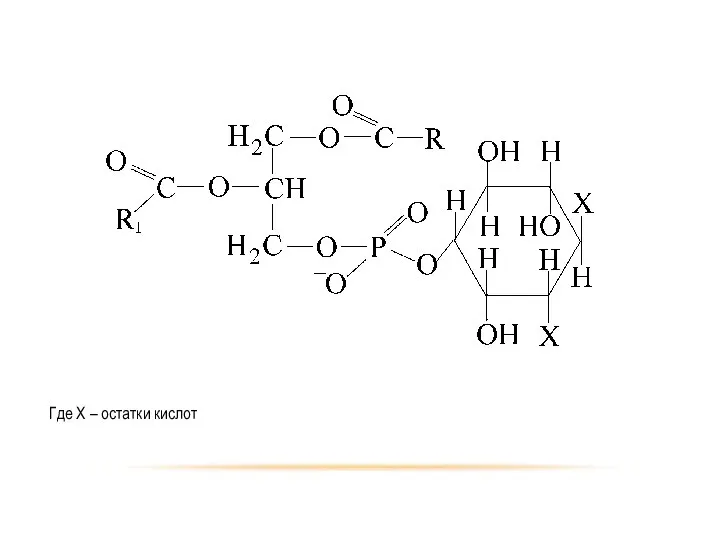
- 77. Инозитфосфатиды. Или фосфатидилинозитах Х представлен остатком циклического спирта – гексаоксициклогексана (инозит). Оксигруппы в миоинозите могут быть
- 78. Где Х – остатки кислот
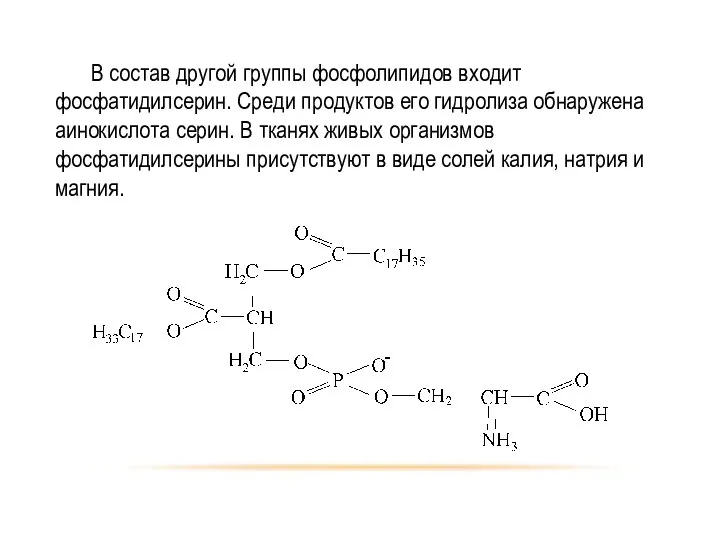
- 79. В состав другой группы фосфолипидов входит фосфатидилсерин. Среди продуктов его гидролиза обнаружена аинокислота серин. В тканях
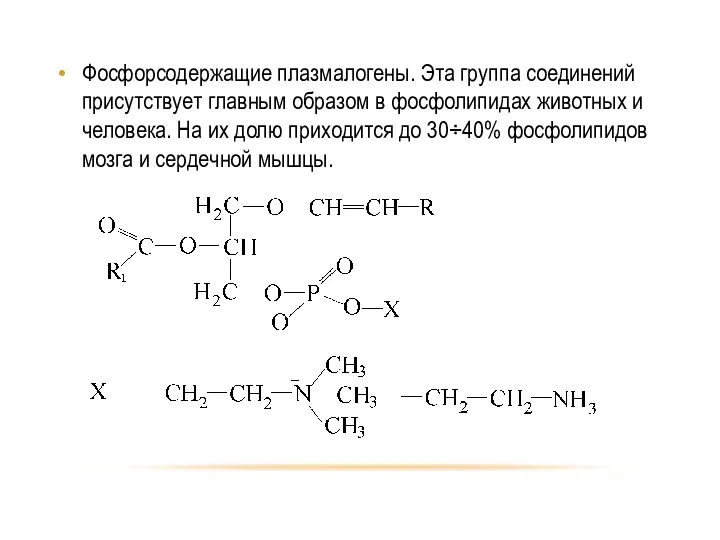
- 80. Фосфорсодержащие плазмалогены. Эта группа соединений присутствует главным образом в фосфолипидах животных и человека. На их долю
- 81. СФИНГОЛИПИДЫ Так называют группу сложных липидов, основой молекулы которых являются алифатические аминоспирты, из которых наиболее распространены
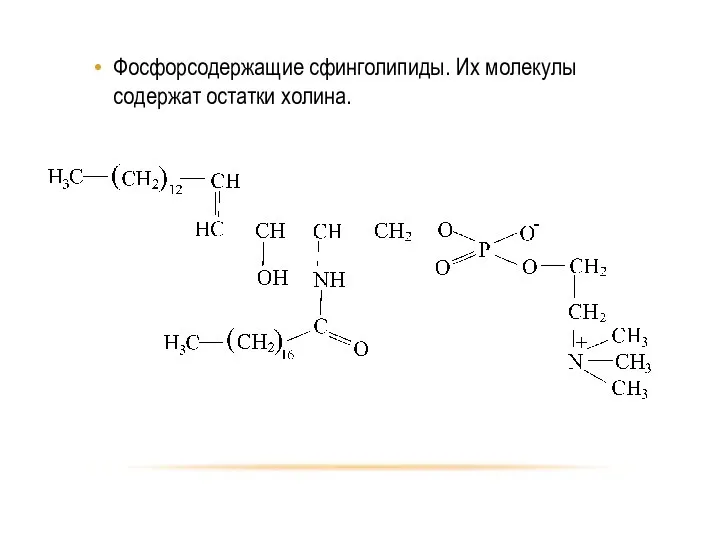
- 82. Фосфорсодержащие сфинголипиды. Их молекулы содержат остатки холина.
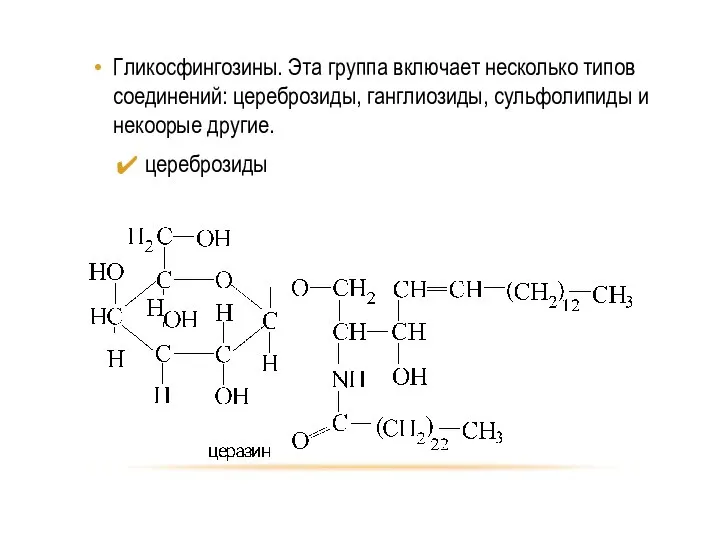
- 83. Гликосфингозины. Эта группа включает несколько типов соединений: цереброзиды, ганглиозиды, сульфолипиды и некоорые другие. цереброзиды
- 84. Ганглиозиды.
- 86. Скачать презентацию









































 Метаболизм липидов. Липолиз. Окисление жирных кислот и глицерола
Метаболизм липидов. Липолиз. Окисление жирных кислот и глицерола Закон сохранения массы веществ Омельянчук Т.Е. учитель химии МАОУ ДСОШ №2 г. Домодедово
Закон сохранения массы веществ Омельянчук Т.Е. учитель химии МАОУ ДСОШ №2 г. Домодедово Получение и исследование свойств хромата калия
Получение и исследование свойств хромата калия Конфигурация макромолекулы
Конфигурация макромолекулы Презентация по Химии "Техника безопасности в кабинете химии" - скачать смотреть
Презентация по Химии "Техника безопасности в кабинете химии" - скачать смотреть  Валентность
Валентность Нафта, сланцевий газ, екологія середовища Підготувала учениця 11 Б класу Кандибка Ольга
Нафта, сланцевий газ, екологія середовища Підготувала учениця 11 Б класу Кандибка Ольга  Алкины
Алкины Алюминий
Алюминий Основные классы неорганических соединений
Основные классы неорганических соединений неметаллы Общая характеристика
неметаллы Общая характеристика Нуклеин қышқылдары
Нуклеин қышқылдары Поверхностные явления. Уравнение Гиббса
Поверхностные явления. Уравнение Гиббса Защита металлов от коррозии
Защита металлов от коррозии Дисахариды Ширяева София ХБ-4 г.Липецк 2012
Дисахариды Ширяева София ХБ-4 г.Липецк 2012 Химический состав клетки. Неорганические вещества клетки
Химический состав клетки. Неорганические вещества клетки Обозначения химического состава и пищевой ценности продовольственных товаров
Обозначения химического состава и пищевой ценности продовольственных товаров Ископаемое топливо
Ископаемое топливо Химическая термодинамика
Химическая термодинамика ПОРТФОЛІО вчителя хімії та біології Турбівської загальноосвітньої школи І – ІІІ ступенів 2014 рік
ПОРТФОЛІО вчителя хімії та біології Турбівської загальноосвітньої школи І – ІІІ ступенів 2014 рік ФИЗИОЛОГИЯ ПИТАНИЯ. Урок по кулинарии. 7 класс. Разработал: учитель технологии Дятлова Елена Владимировна
ФИЗИОЛОГИЯ ПИТАНИЯ. Урок по кулинарии. 7 класс. Разработал: учитель технологии Дятлова Елена Владимировна  Нуклеиновые кислоты
Нуклеиновые кислоты Строение атома
Строение атома Теория строения химических веществ
Теория строения химических веществ Презентация по Химии "АЗОТНАЯ КИСЛОТА И ЕЕ СВОЙСТВА" - скачать смотреть бесплатно
Презентация по Химии "АЗОТНАЯ КИСЛОТА И ЕЕ СВОЙСТВА" - скачать смотреть бесплатно Кислородсодержащие органические соединения. Предельные одноатомные спирты
Кислородсодержащие органические соединения. Предельные одноатомные спирты Обмен холестерола
Обмен холестерола Электролиз
Электролиз