Содержание
- 2. Цис-транс изомерия Характерна для группы полимеров, имеющих в цепи двойные связи
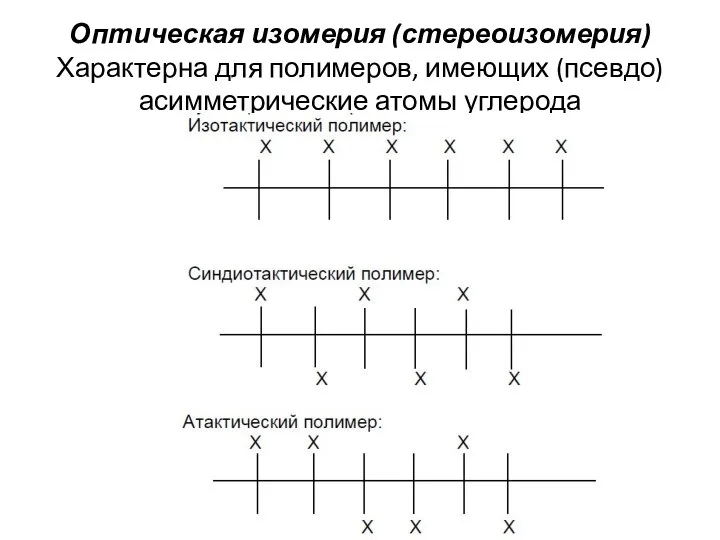
- 3. Оптическая изомерия (стереоизомерия) Характерна для полимеров, имеющих (псевдо)асимметрические атомы углерода
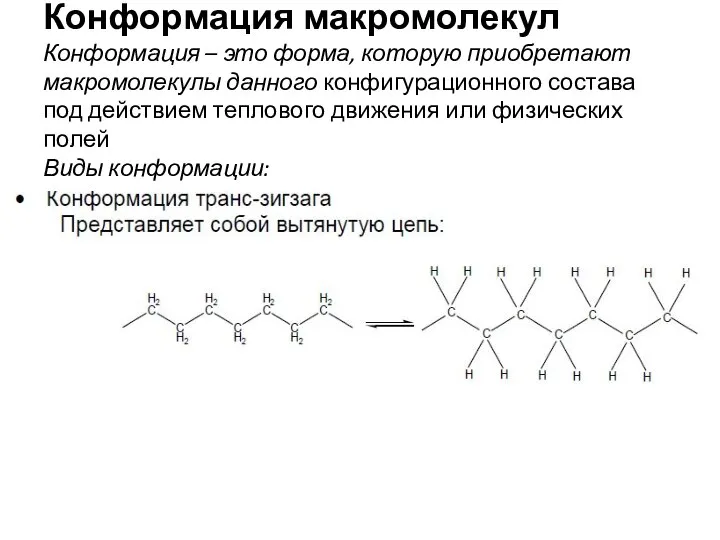
- 4. Конформация макромолекул Конформация – это форма, которую приобретают макромолекулы данного конфигурационного состава под действием теплового движения
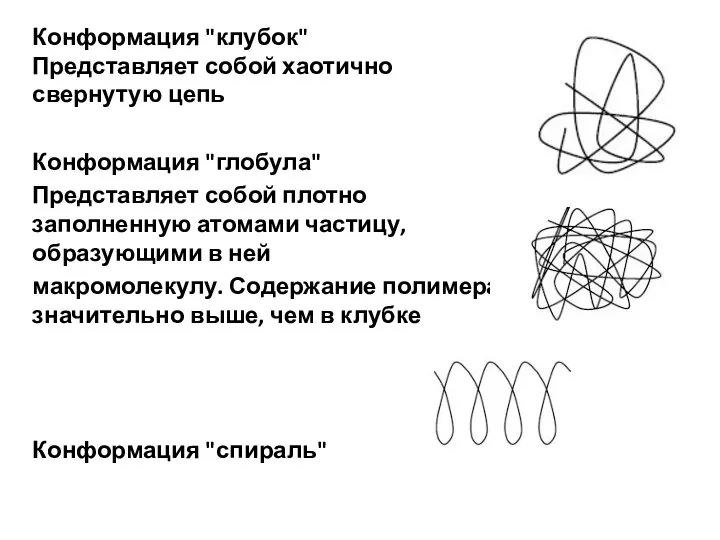
- 5. Конформация "клубок" Представляет собой хаотично свернутую цепь Конформация "глобула" Представляет собой плотно заполненную атомами частицу, образующими
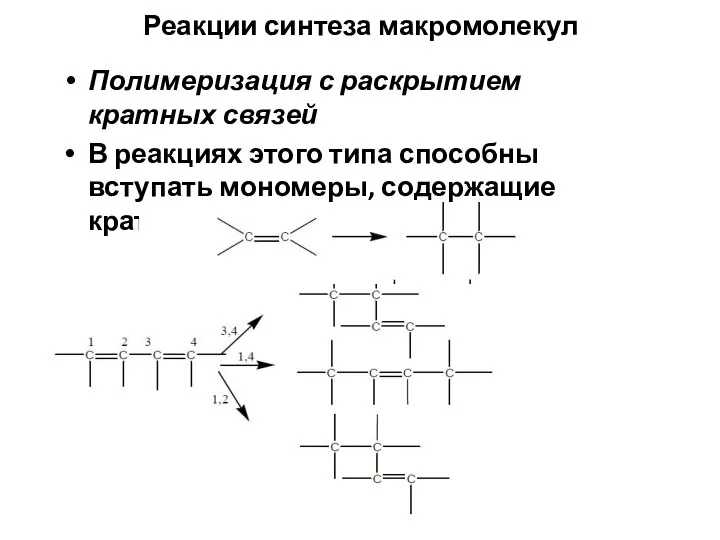
- 6. Реакции синтеза макромолекул Полимеризация с раскрытием кратных связей В реакциях этого типа способны вступать мономеры, содержащие
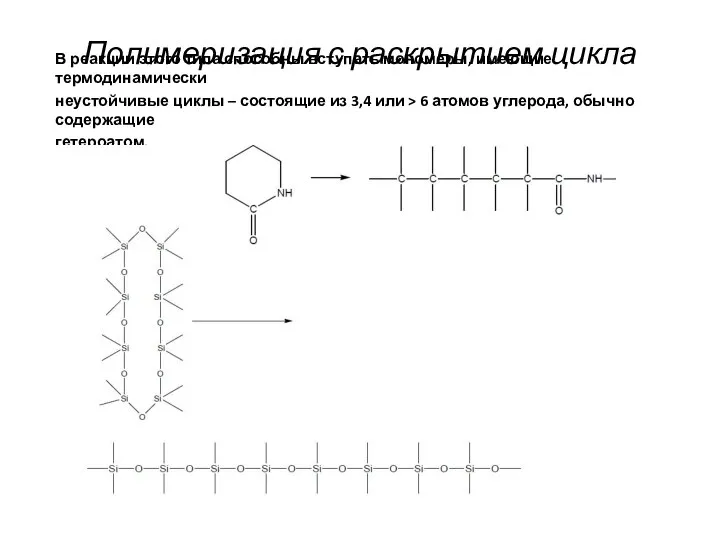
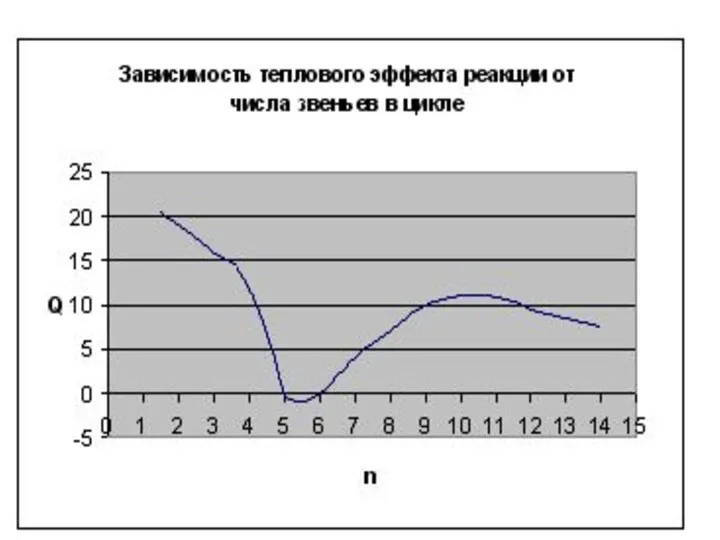
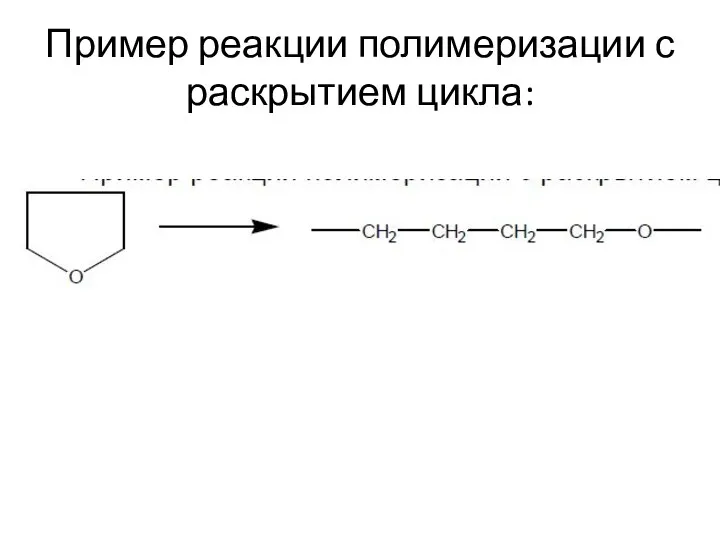
- 7. Полимеризация с раскрытием цикла В реакции этого типа способны вступать мономеры, имеющие термодинамически неустойчивые циклы –
- 8. Поликонденсация и полиприсоединение Поликонденсация – ступенчатый процесс взаимодействия молекул, содержащих функциональные группы, приводящий в результате химического
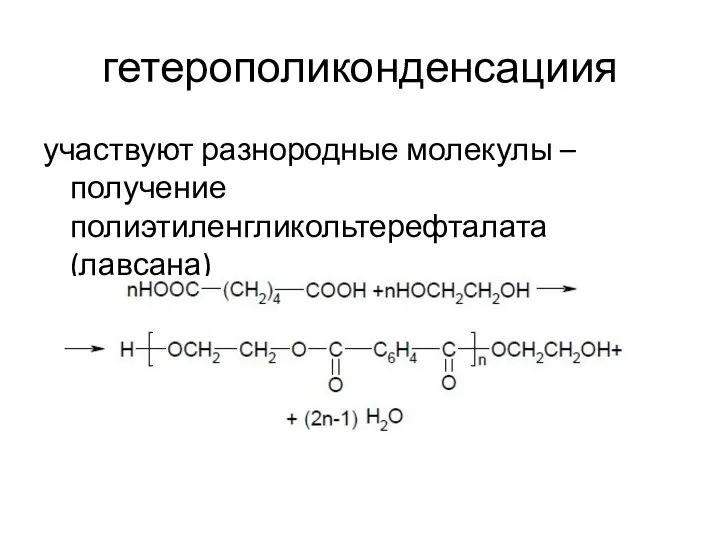
- 9. гетерополиконденсациия участвуют разнородные молекулы – получение полиэтиленгликольтерефталата (лавсана)
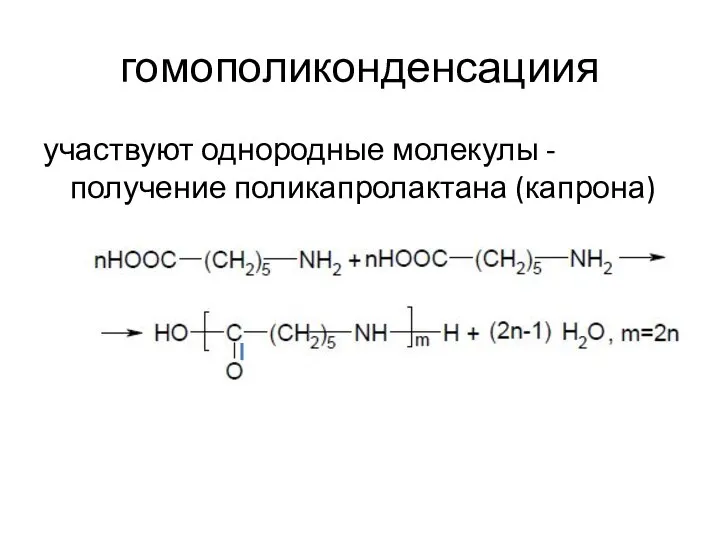
- 10. гомополиконденсациия участвуют однородные молекулы - получение поликапролактана (капрона)
- 11. Радикальная полимеризация Радикальной полимеризацией называется цепная реакция, протекающая через образование свободных радикалов.
- 12. Как всякая цепная реакция, полимеризация состоит в основном из трех элементарных реакций: 1) образование активного центра;
- 13. Общая характеристика элементарных актов цепной полимеризации (ПМ) не отличается от тех же стадий цепных процессов 1.
- 14. Мономеры, способные вступать в реакции радикальной полимеризации В реакции радикальной полимеризации способны вступать мономеры винилового ряда
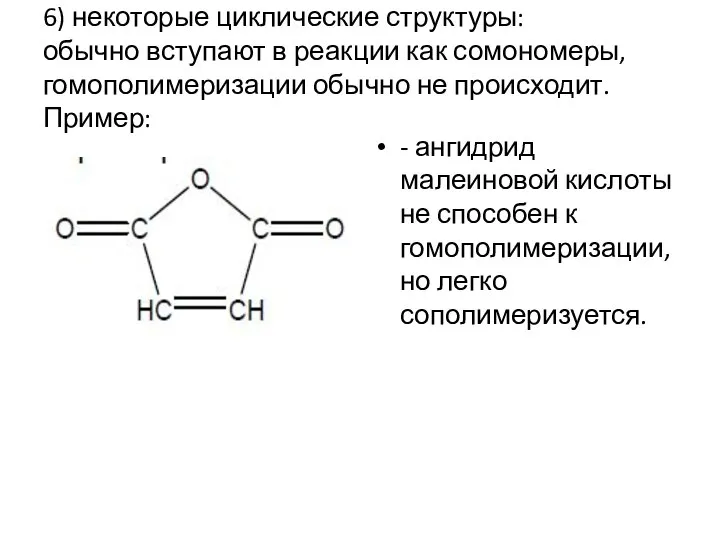
- 16. 6) некоторые циклические структуры: обычно вступают в реакции как сомономеры, гомополимеризации обычно не происходит. Пример: -
- 18. Пример реакции полимеризации с раскрытием цикла:
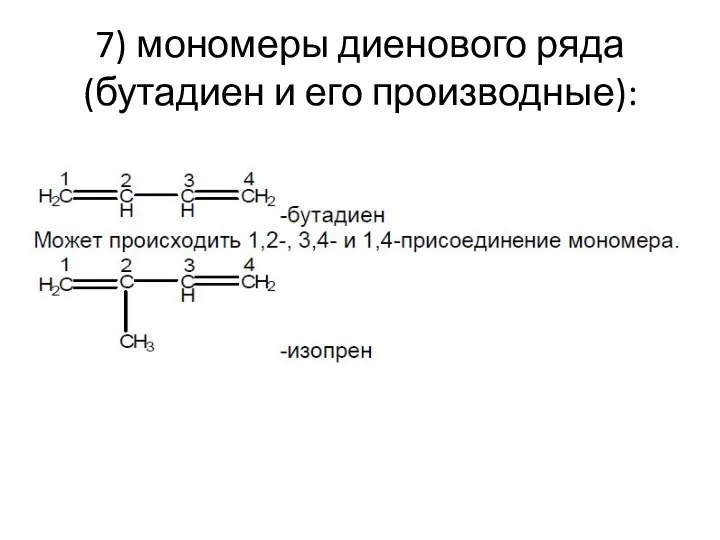
- 19. 7) мономеры диенового ряда (бутадиен и его производные):
- 20. СH2=CH–CH=CH2 полимеризуется; СH2=C(Ph)–CH=CH2 полимеризуется в 10 раз быстрее дивинила; (Ph)CH=CH–CH=CH2 полимеризуется с трудом; (Ph)CH=CH–CH=CH(Ph) не полимеризуется
- 21. Относительная активность производных дивинила в полимеризации
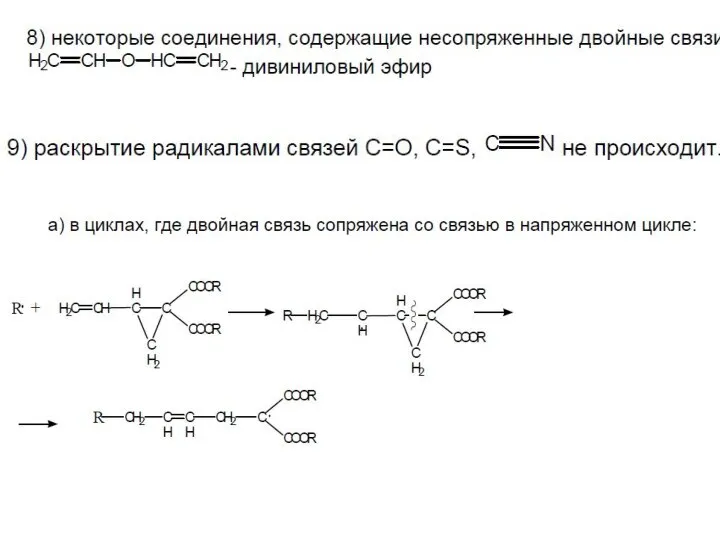
- 23. с очень неустойчивыми циклами: 10) соединения ацетиленового ряда практически не участвуют в реакциях радикальной полимеризации
- 24. Полимеризация Полимеризацией называется реакция соединения мономерных молекул с раскрытием двойной (или тройной) связи, которая не сопровождается
- 25. Процесс полимеризации является цепной реакцией, состоящей из трех элементарных актов: Образования активного центра на мономере Роста
- 26. Радикальная полимеризация Активными центрами являются свободные радикалы. В зависимости от способа образования свободных радикалов инициирование может
- 27. Реакции могут осуществляться различными способами, но соблюдается следующая принципиальная схема процесса. A1→A1* Образование активного центра А1*+А1→А2*
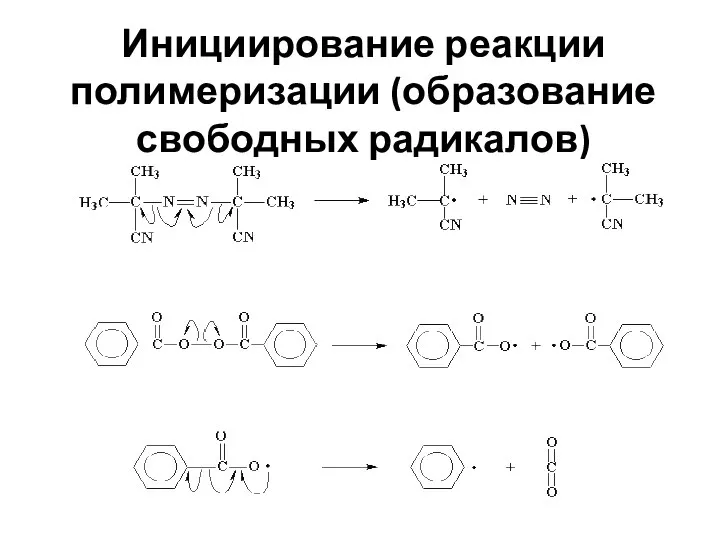
- 28. Инициирование реакции полимеризации (образование свободных радикалов)
- 29. Инициирование реакции полимеризации (взаимодействие радикала с мономером)
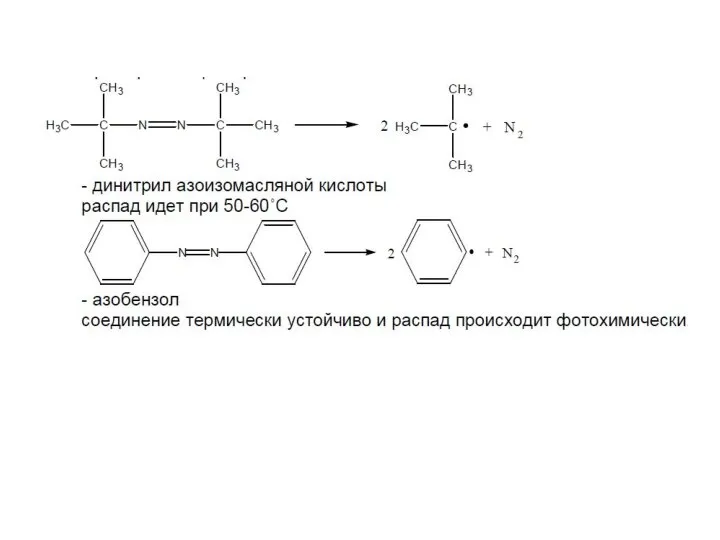
- 34. Соединения, имеющие в своем составе азогруппу
- 36. 1. Способность инициатора распадаться без образования радикалов. 2. Возможность протекания реакции передачи цепи на инициатор. 3.
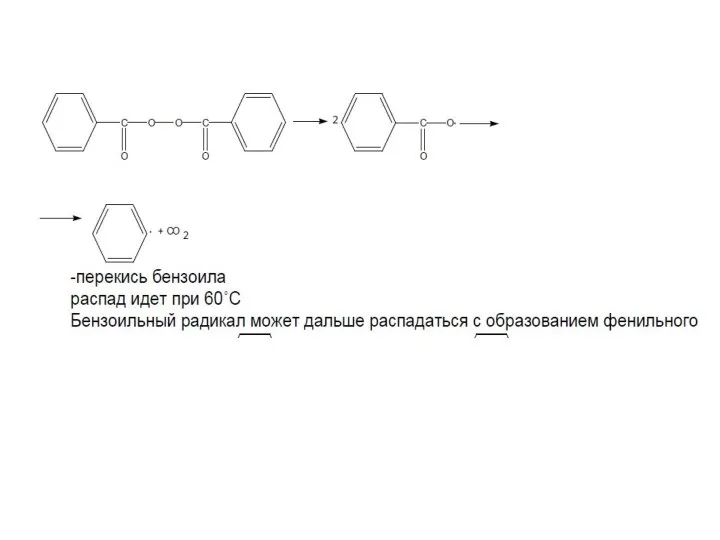
- 37. Эффективность инициаторов Побочные реакции с участием радикалов перекиси бензоила (а) [2С6Н5СО•] → [С6Н5СООС6Н5 + СО2]; (б)
- 38. Эффективность инициирования f= отношение числа радикалов, инициирующих полимеризацию к общему числу радикалов
- 39. Характеристика некоторых инициаторов
- 40. Скорость инициирования представляет собой скорость распада с учетом эффективности инициирования: где f – эффективность инициирования –
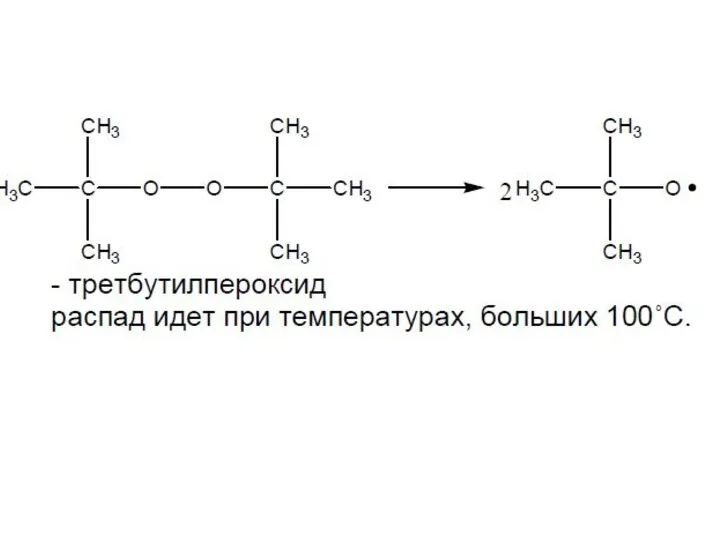
- 41. Влияние температуры на ход процесса Константа скорости распада зависит от температуры по уравнению Аррениуса
- 42. Обратным процессу распада является процесс рекомбинации образовавшихся в системе радикалов. Рекомбинация может протекать в окружении молекул
- 43. Окислительно-восстановительные системы Реактив Фентона: Персульфат – Fe2+:
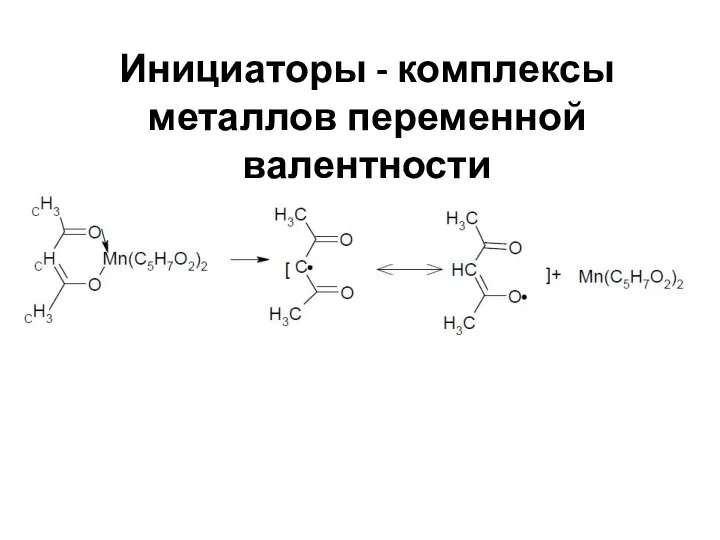
- 44. Инициаторы - комплексы металлов переменной валентности
- 45. Инициирование под действием различных излучений Радиационная химия - может идти инициирование под действием γ-излучения Фотохимия: Инициирование
- 46. Сенсибилизаторы группа соединений, не имеющих связей, способных к разрыву, но, поглотив энергию, они передают ее другим
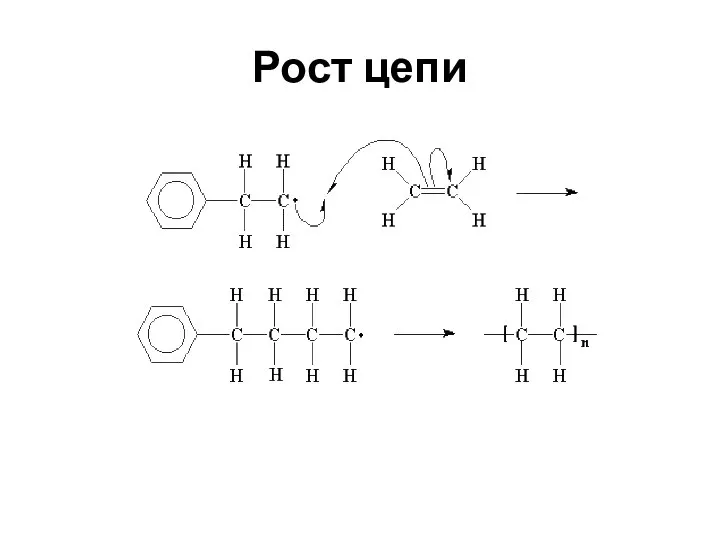
- 47. РОСТ ЦЕПИ Полимерная цепь растет в результате взаимодействия мономера с первоначально образовавшимся или растущим радикалом А1*+А1→А2*
- 48. Рост цепи
- 49. Обрыв цепи Обрыв цепи при радикальной полимеризации может происходить различными путями: реакции рекомбинации и диспропорционирования макрорадикалов,
- 50. Обрыв цепи при радикальной полимеризации может происходить различными путями: реакции рекомбинации и диспропорционирования макрорадикалов, реакции передачи
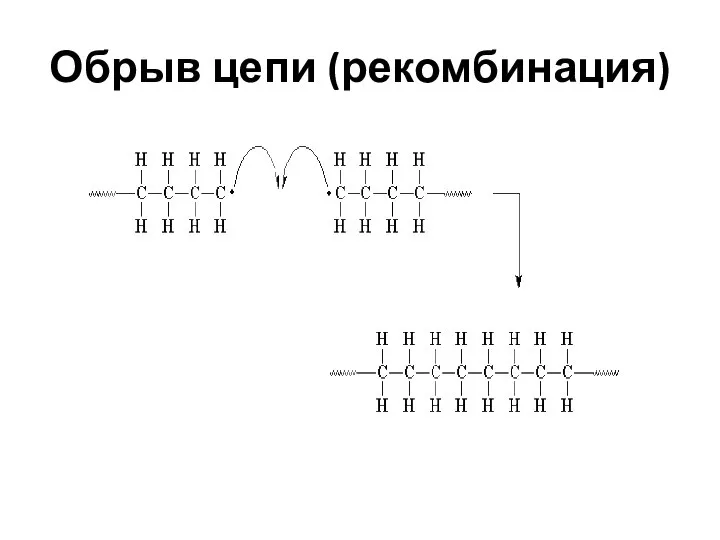
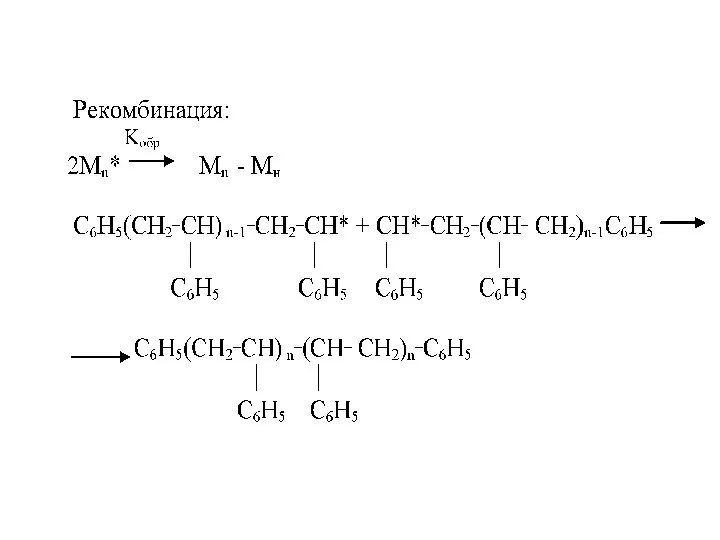
- 51. Обрыв цепи (рекомбинация)
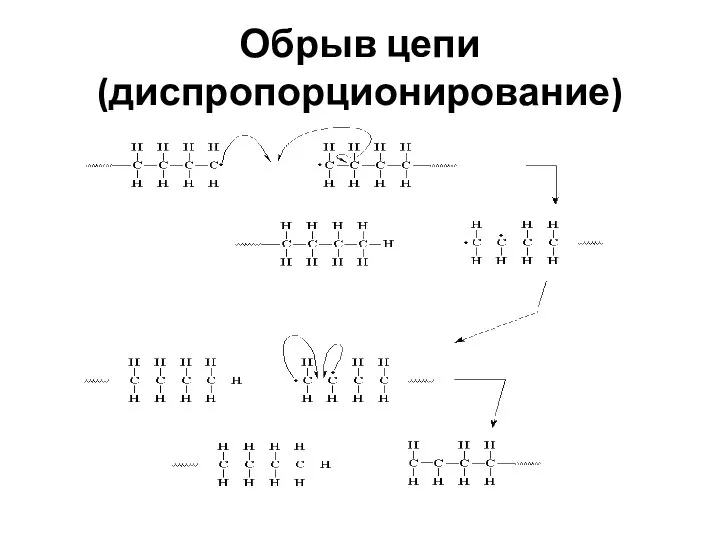
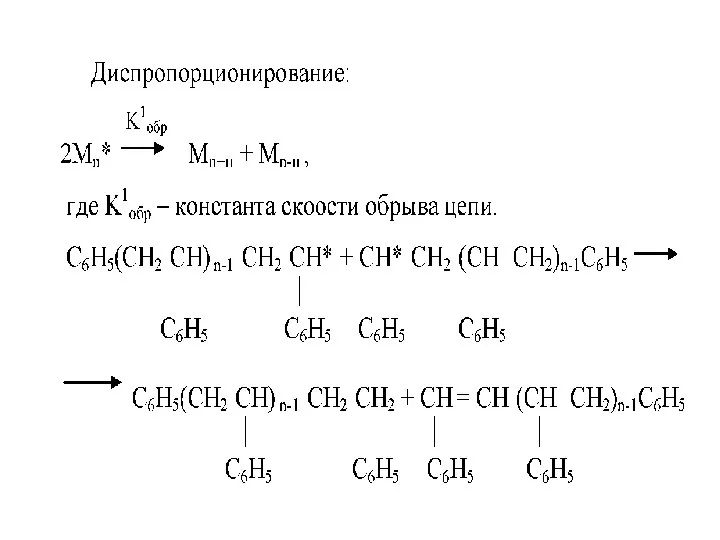
- 52. Обрыв цепи (диспропорционирование)
- 53. Скорость реакции обрыва зависит от концентрации радикалов в системе
- 54. Скорость процесса определяется диффузией Макрорадикалам нужно сблизиться и развернуться в нужном направлении (2 стадии). Лимитирующей стадией
- 55. Гель-эффект
- 56. Гель-эффект При полимеризации винильных мономеров вязкость системы изменяется на много порядков. Когда она возрастает на 4–5
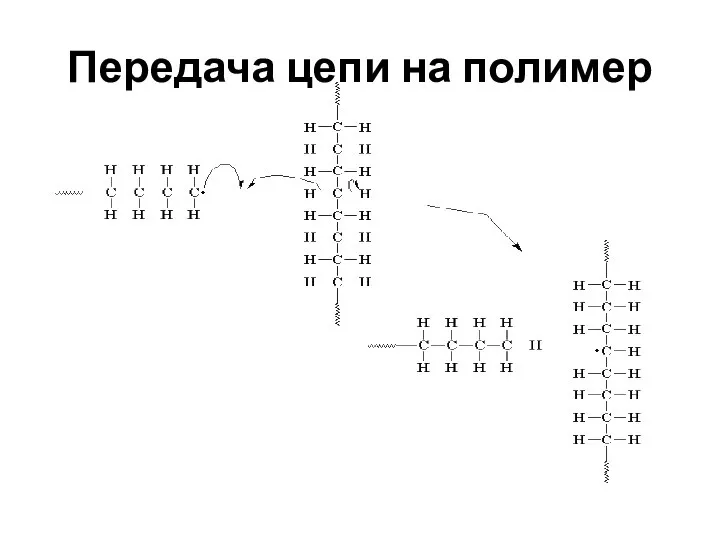
- 57. Передача цепи на полимер
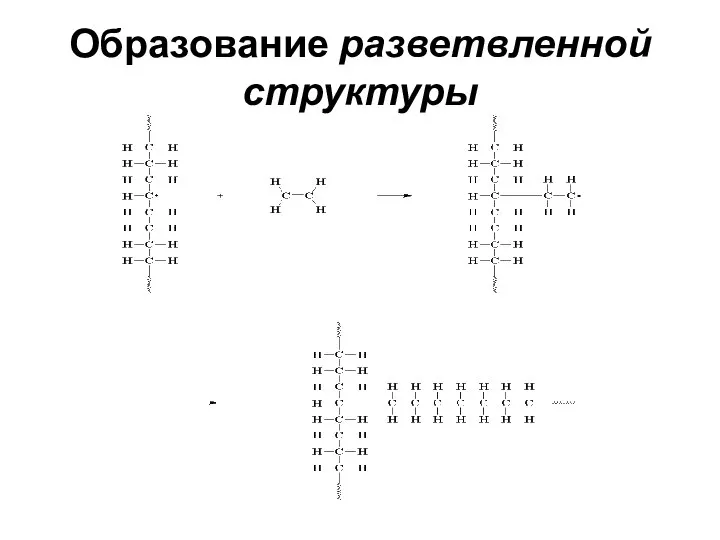
- 58. Образование разветвленной структуры
- 59. Передача цепи через молекулу мономера: через молекулу растворителя: через молекулу инициатора:
- 60. Ингибиторы – вещества, добавление которых к мономеру, вызывает полное прекращение полимеризации. Замедлители - вещества, введение которых
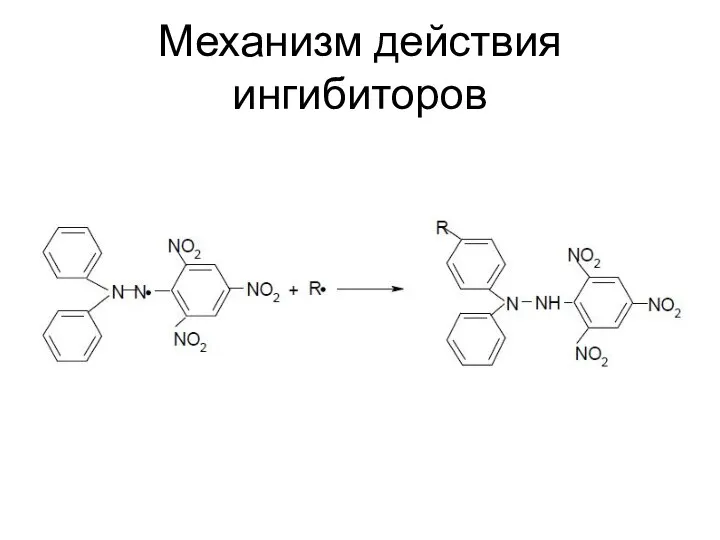
- 61. Механизм действия ингибиторов
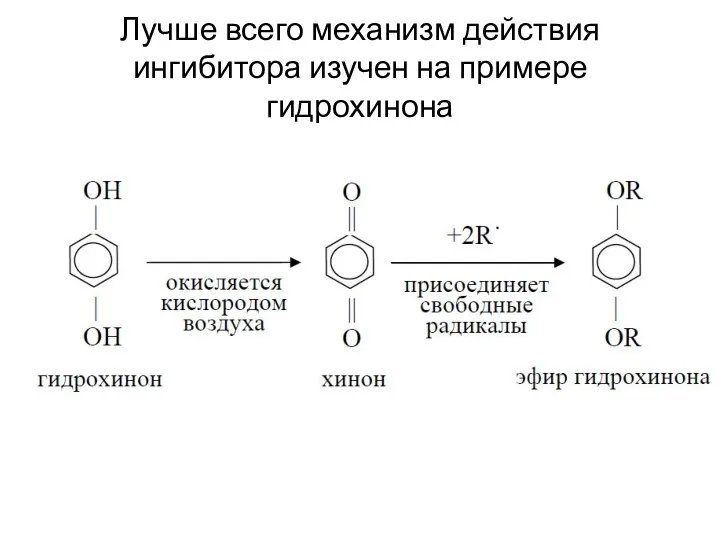
- 62. Лучше всего механизм действия ингибитора изучен на примере гидрохинона
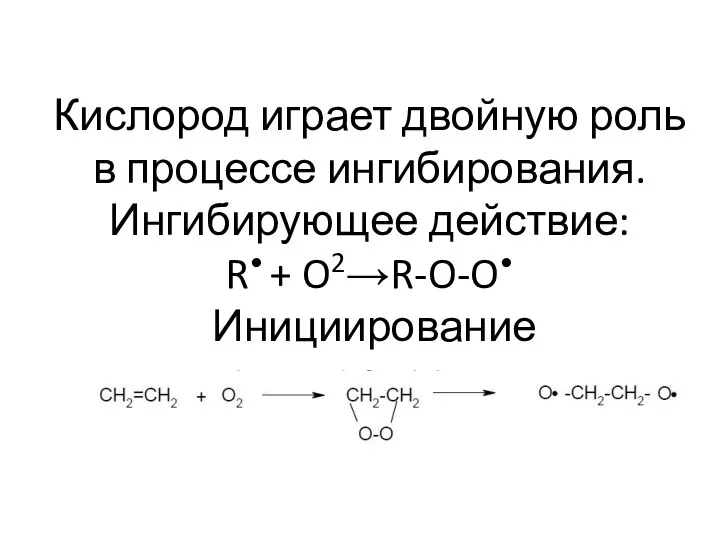
- 63. Кислород играет двойную роль в процессе ингибирования. Ингибирующее действие: R• + O2→R-O-O• Инициирование полимеризации:
- 65. Доля радикалов инициатора, фактически участвующих в инициировании и определяемых скоростью V/, называется эффективностью инициирования f и
- 66. Скорость инициирования
- 68. Скорость превращения мономера есть, практически, скорость роста. Vр= Кр [ M* ] [ M ], где
- 69. При обрыве цепи в системе активные радикалы исчезают или заменяются малоактивными радикалами, неспособными присоединять молекулы мономера.
- 72. Скорость обрыва цепи: Vобр= Кобр [ M* ]2 .
- 73. КИНЕТИКА РАДИКАЛЬНОЙ ПОЛИМЕРИЗАЦИИ Допущения: 1. Реакционная способность радикалов, образующихся в процессе ПМ, не зависит от длины
- 74. Принцип стационарного состояния Боденштейна Скорость реакции в стационарном состоянии равна скорости роста цепи:
- 75. Длина кинетической цепи – среднее число молекул мономера, приходящихся на один образовавшийся активный центр
- 76. Длина кинетической цепи обратно пропорциональна концентрации радикалов или скорости полимеризации. Она при постоянной температуре определяется природой
- 77. Общая скорость полимеризации равна скорости расходования мономера на стадии роста и идентична скорости роста цепи: Vобщ=
- 78. Vин = Vобр , т.е. 2Kин f [ I ] = Kобр [ M*]2, где [
- 79. Средняя степень полимеризации определяется соотношением скорости роста и суммарной скорости обрыва P = Vр / Vобр
- 80. Влияние основных факторов на полимеризацию винильных соединений С повышением температуры скорость полимеризации возрастает, а молекулярная масса
- 81. Чем больше концентрация инициатора, тем выше скорость полимеризации, но ниже молекулярная масса образующегося полимера. С увеличением
- 83. Скачать презентацию



















![Эффективность инициаторов Побочные реакции с участием радикалов перекиси бензоила (а) [2С6Н5СО•]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397431/slide-36.jpg)























![Скорость обрыва цепи: Vобр= Кобр [ M* ]2 .](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397431/slide-71.jpg)





![Vин = Vобр , т.е. 2Kин f [ I ] =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397431/slide-77.jpg)



 03. Знакомство с лаб. оборудованием. Правила техники безопасности
03. Знакомство с лаб. оборудованием. Правила техники безопасности Силикатная промышленность
Силикатная промышленность Жиры Цели урока: Изучить жиры: состав, классификация,физические и химические свойства, переработка, применение, биологич
Жиры Цели урока: Изучить жиры: состав, классификация,физические и химические свойства, переработка, применение, биологич Презентация по Химии "Жиры животных" - скачать смотреть
Презентация по Химии "Жиры животных" - скачать смотреть  Алкілування ізобутану бутенами
Алкілування ізобутану бутенами Аттестационная работа. Исследовательская деятельность на уроках химии (8 -9 классы). Исследование речки Беленькой
Аттестационная работа. Исследовательская деятельность на уроках химии (8 -9 классы). Исследование речки Беленькой Строение электронных оболочек атомов
Строение электронных оболочек атомов Жиры
Жиры Обмен липидов
Обмен липидов Титан және оның қорытпалары
Титан және оның қорытпалары Основы химической термодинамики
Основы химической термодинамики Химическое равновесие. Азот и Фосфор. 9 класс
Химическое равновесие. Азот и Фосфор. 9 класс Неорганические вещества клетки
Неорганические вещества клетки Презентация по Химии "Нефть" - скачать смотреть бесплатно
Презентация по Химии "Нефть" - скачать смотреть бесплатно Презентация по Химии "Карбонові кислоти" - скачать смотреть бесплатно
Презентация по Химии "Карбонові кислоти" - скачать смотреть бесплатно Общая характеристика металлов
Общая характеристика металлов Химическая кинетика. Лекция 9
Химическая кинетика. Лекция 9 Коллоидная химия. Введение
Коллоидная химия. Введение Тема 1. Металлы и сплавы
Тема 1. Металлы и сплавы The way to prepare gold clusters - Every atom makes a difference
The way to prepare gold clusters - Every atom makes a difference Реакции замещения
Реакции замещения Презентация по Химии "В мире веществ и реакций" - скачать смотреть
Презентация по Химии "В мире веществ и реакций" - скачать смотреть  Презентація на тему «Основи»
Презентація на тему «Основи»  Химия. Проверочная
Химия. Проверочная Нанодисперсный политетрафторэтилен. Инертные, антифрикционные, противоизносные покрытия
Нанодисперсный политетрафторэтилен. Инертные, антифрикционные, противоизносные покрытия Электрохимический ряд напряжений металлов
Электрохимический ряд напряжений металлов  Алкены и Алкины
Алкены и Алкины Алкины
Алкины