Содержание
- 2. Строение и свойства атомов Элементы главной подгруппы VII группы Периодической системы Д. И. Менделеева, объединенные под
- 3. Галогены — очень сильные окислители. Фтор в химических реакциях проявляет только окислительные свойства, и для него
- 4. Галогены — простые вещества Все галогены существуют в свободном состоянии в виде двухатомных молекул с ковалентной
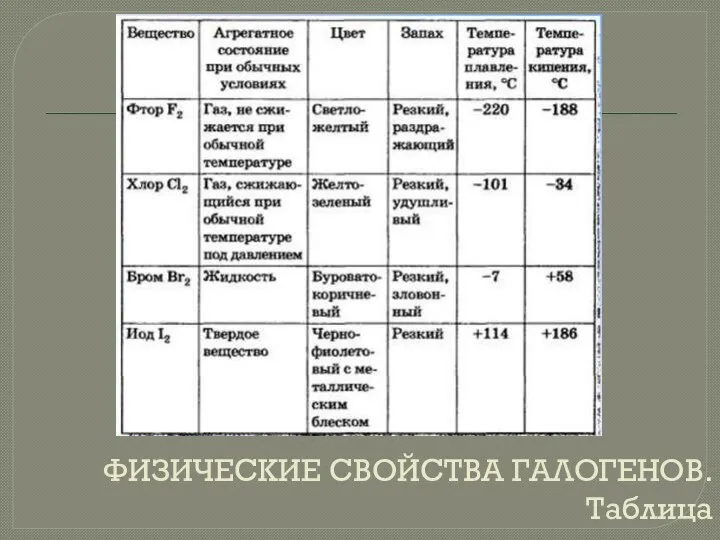
- 5. ФИЗИЧЕСКИЕ СВОЙСТВА ГАЛОГЕНОВ. Таблица
- 6. Окислительные свойства галогенов Каждый галоген является самым сильным окислителем в своем периоде. Окислительные свойства галогенов отчетливо
- 7. Остальные галогены реагируют с металлами в основном при нагревании. Так, в колбе, наполненной хлором, красиво вспыхивают
- 8. Нагретый порошок железа также загорается при взаимодействии С хлором. Опыт МОЖ- Рис. 50. Горение сурьмы но
- 9. Йод окисляет металлы медленнее, но в присутствии воды, которая является катализатором, реакция йода с порошком алюминия
- 10. Об уменьшении окислительных и увеличении восстановительных свойств галогенов от фтора к йоду можно судить и по
- 11. Для фтора эта реакция не характерна, так как она протекает в растворе, а фтор взаимодействует с
- 12. Если фтор взаимодействует с водородом в любых условиях со взрывом, то смесь хлора с водородом реагирует
- 13. Открытие галогенов Фтор в свободном виде получил впервые в 1886 г. французский химик Анри Муассан, который
- 14. Хлор открыт шведским химиком К. Шееле в 1774 г. Элемент получил название за свой цвет (греч.
- 15. Бром открыт в 1826 г. французским химиком А.Баларом. Элемент назван так за свой запах (греч. бромос
- 17. Скачать презентацию













 Коллоидные растворы. Молекулярно-кинетические и оптические свойства. Строение коллоидных частиц
Коллоидные растворы. Молекулярно-кинетические и оптические свойства. Строение коллоидных частиц Празеодим
Празеодим Темір. Жай заттармен
Темір. Жай заттармен Виды пластика, что производят и что можно переработать
Виды пластика, что производят и что можно переработать Комплексный анализ текста ЕГЭ
Комплексный анализ текста ЕГЭ Вклад химиков – органиков в Победу
Вклад химиков – органиков в Победу Тотығу дәрежесі. Тотығу-тотықсыздану реакция теңдеулері
Тотығу дәрежесі. Тотығу-тотықсыздану реакция теңдеулері Неметалічні елементи
Неметалічні елементи Растворы. Квалификации химических веществ:
Растворы. Квалификации химических веществ: Синтетические каучуки
Синтетические каучуки Теория сплавов
Теория сплавов Cложные липиды (липоиды)
Cложные липиды (липоиды) Лужноземельні метали
Лужноземельні метали Электрохимические процессы и явления
Электрохимические процессы и явления Исторические аспекты возникновения и развития. Теории химического строения
Исторические аспекты возникновения и развития. Теории химического строения Лекарственные растения и сырье, содержащие дубильные вещества
Лекарственные растения и сырье, содержащие дубильные вещества Численное моделирование развития возмущений в ударном слое на пластине в потоке смеси колебательно возбужденных газов
Численное моделирование развития возмущений в ударном слое на пластине в потоке смеси колебательно возбужденных газов Фосфор
Фосфор Соли азотной кислоты, применение Девиз урока «Au, Na, Ar, Ne, It, Eu – Os, Ra,U, Db, In, Er, As Ni, Es C, Eu La Ь» Л. Н. Толстой
Соли азотной кислоты, применение Девиз урока «Au, Na, Ar, Ne, It, Eu – Os, Ra,U, Db, In, Er, As Ni, Es C, Eu La Ь» Л. Н. Толстой Чугуны
Чугуны Расчеты, связанные с понятием доля
Расчеты, связанные с понятием доля Презентация по Химии "Анализ тенденций развития химии" - скачать смотреть
Презентация по Химии "Анализ тенденций развития химии" - скачать смотреть  Презентация по Химии "Самородки" - скачать смотреть бесплатно__
Презентация по Химии "Самородки" - скачать смотреть бесплатно__ Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Электрохимия. Электродные потенциалы
Электрохимия. Электродные потенциалы Поверхностное упрочнение деталей. (Лекция 11)
Поверхностное упрочнение деталей. (Лекция 11) Металлические яды, изоляция минерализацией. Применение металлов и их соединений в клинической фармации
Металлические яды, изоляция минерализацией. Применение металлов и их соединений в клинической фармации Химическая связь
Химическая связь