Содержание
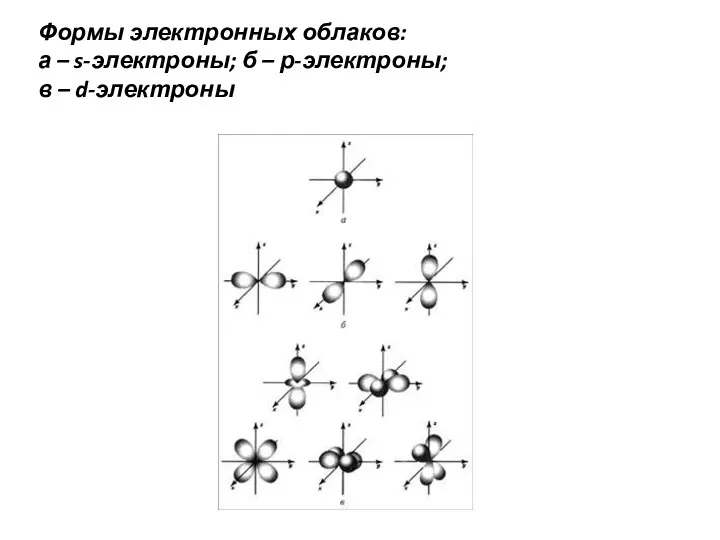
- 2. Формы электронных облаков: а – s-электроны; б – р-электроны; в – d-электроны
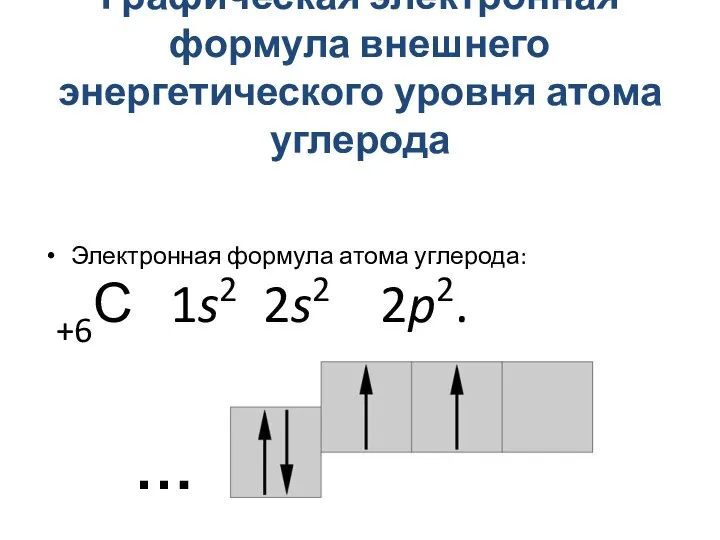
- 3. Графическая электронная формула внешнего энергетического уровня атома углерода Электронная формула атома углерода: +6С 1s2 2s2 2p2.
- 5. Графическая электронная формула внешнего энергетического уровня атома углерода в возбужденном состоянии Атом углерода переходит в возбужденное
- 6. Гибридизация атомных орбиталей – изменение формы и энергии орбиталей атома при образовании ковалентной связи для достижения
- 7. Форма гибридной орбитали за счет комбинации s- и p-атомных орбиталей гибридная орбиталь больше вытянута по одну
- 8. Число гибридных орбиталей равно числу атомных орбиталей. Гибридные орбитали одинаковы по форме электронного облака и по
- 9. 1 s-электрон и 3 p-электрона атома углерода образуют четыре одинаковых гибридных орбитали. Этот тип гибридизации называется
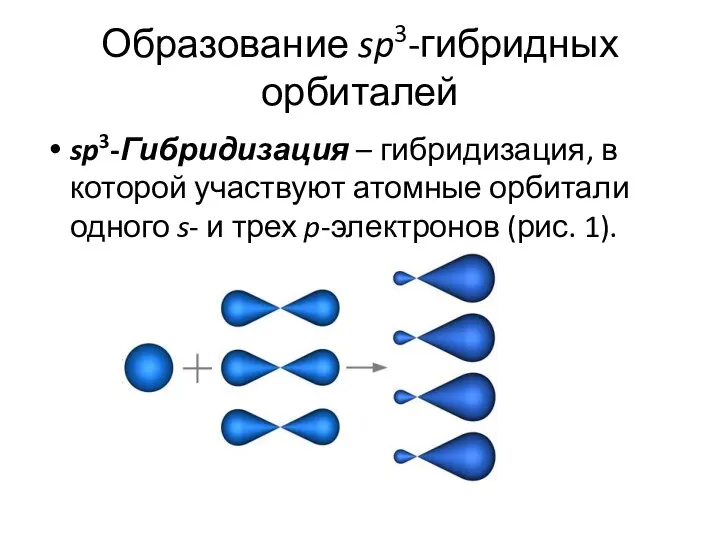
- 10. Образование sp3-гибридных орбиталей sp3-Гибридизация – гибридизация, в которой участвуют атомные орбитали одного s- и трех p-электронов
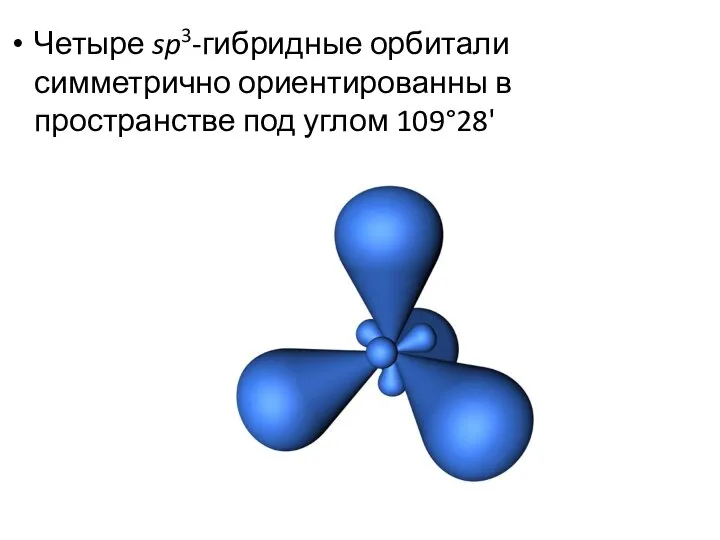
- 11. Четыре sp3-гибридные орбитали симметрично ориентированны в пространстве под углом 109°28'
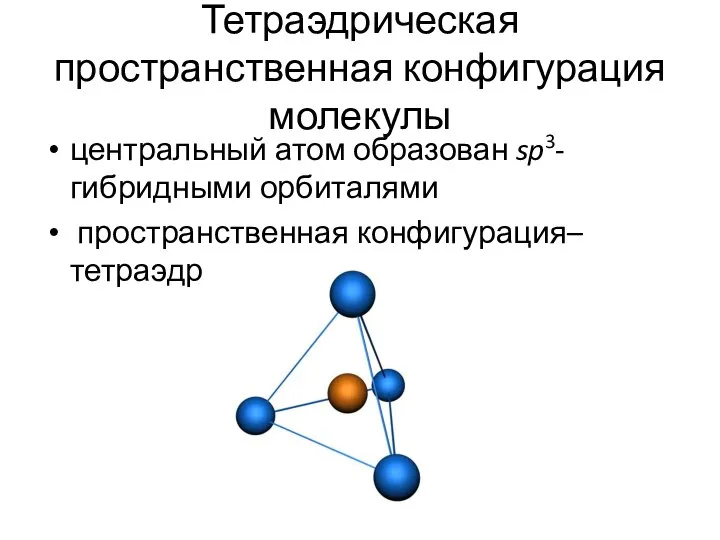
- 12. Тетраэдрическая пространственная конфигурация молекулы центральный атом образован sp3-гибридными орбиталями пространственная конфигурация– тетраэдр
- 13. Модель молекулы метана (CH4) углерода подвергается sp3-гибридизации.
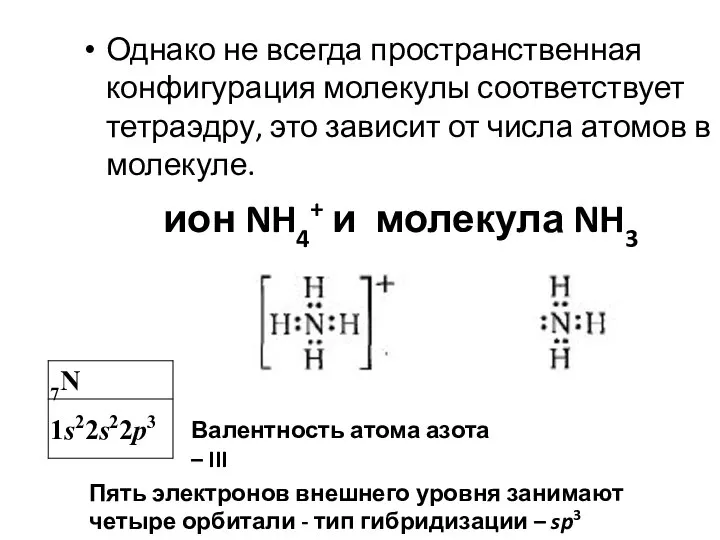
- 14. Однако не всегда пространственная конфигурация молекулы соответствует тетраэдру, это зависит от числа атомов в молекуле. Валентность
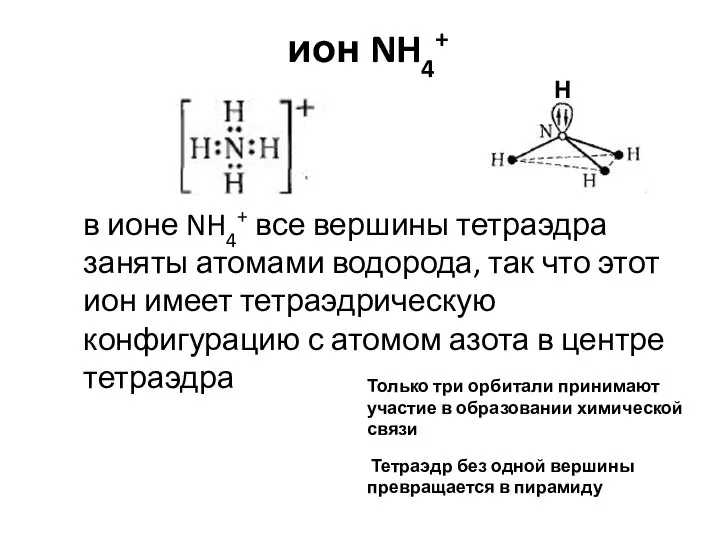
- 15. ион NH4+ Только три орбитали принимают участие в образовании химической связи Тетраэдр без одной вершины превращается
- 16. Mолекула NH3 тригональная пирамида с атомом азота в ее вершине и атомами водорода в вершинах основания
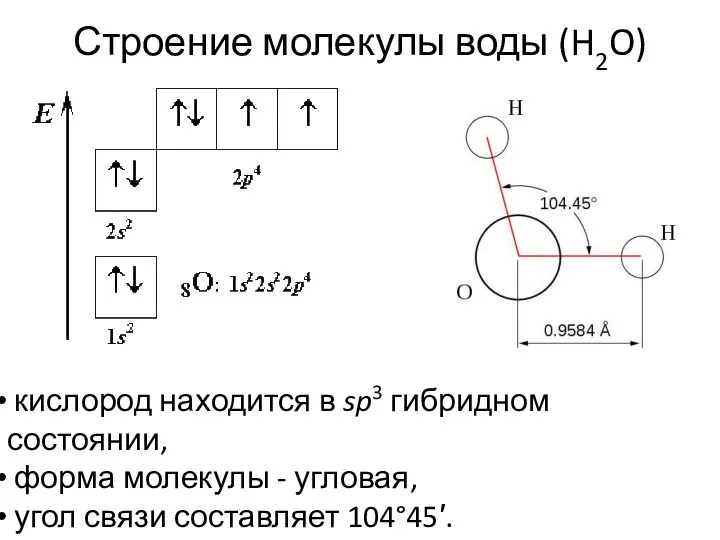
- 17. Строение молекулы воды (H2O) кислород находится в sp3 гибридном состоянии, форма молекулы - угловая, угол связи
- 18. Примеры соединений, для которых характерна sp3-гибридизация: H2O, NH3, POCl3, SO2F2, SOBr2, NH4+, H3O+. предельные углеводороды (алканы,
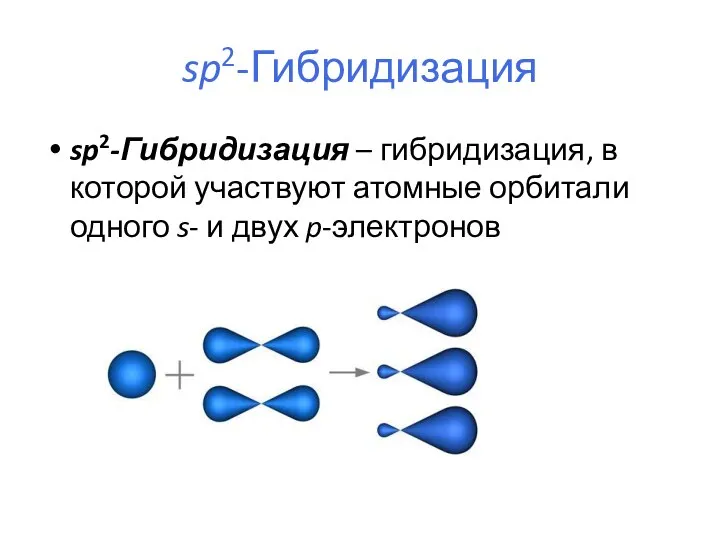
- 19. sp2-Гибридизация sp2-Гибридизация – гибридизация, в которой участвуют атомные орбитали одного s- и двух p-электронов
- 20. образуются три гибридные sp2 орбитали, расположенные в одной плоскости под углом 120° друг к другу
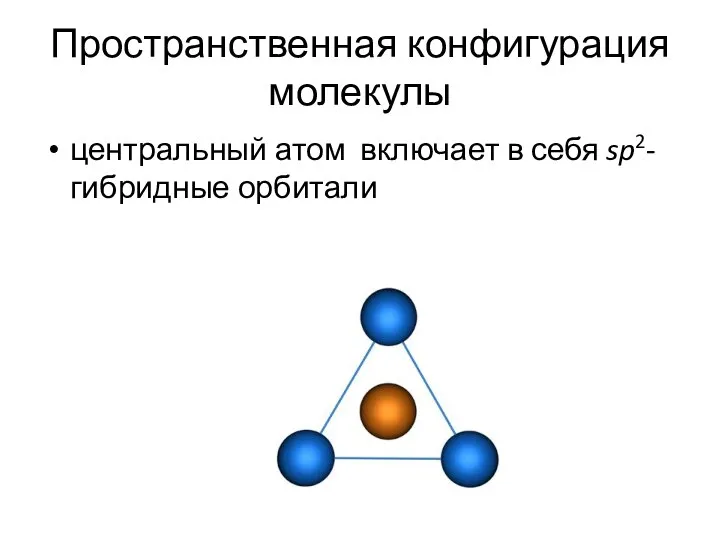
- 21. Пространственная конфигурация молекулы центральный атом включает в себя sp2-гибридные орбитали
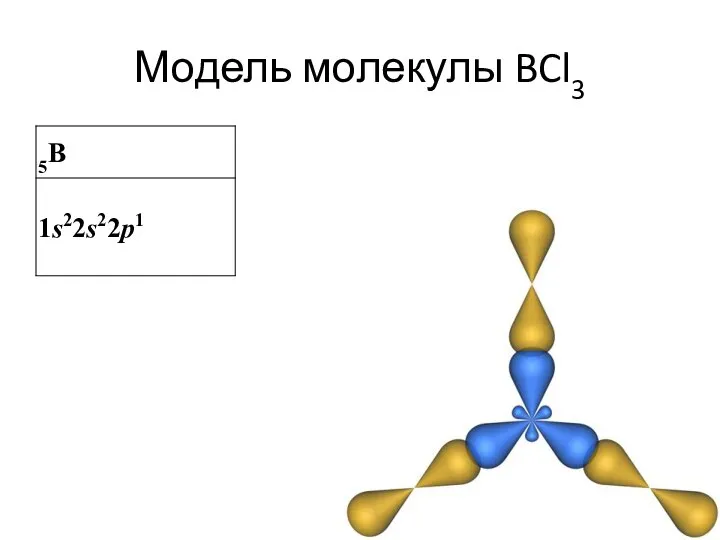
- 22. Модель молекулы BCl3
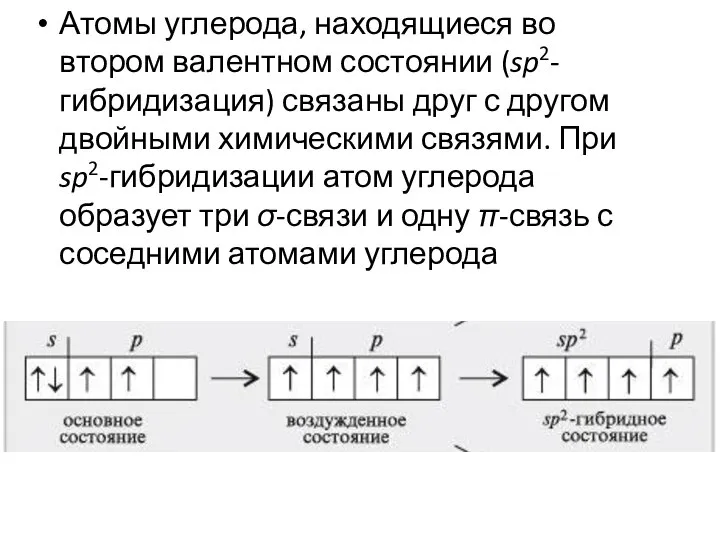
- 23. Атомы углерода, находящиеся во втором валентном состоянии (sp2-гибридизация) связаны друг с другом двойными химическими связями. При
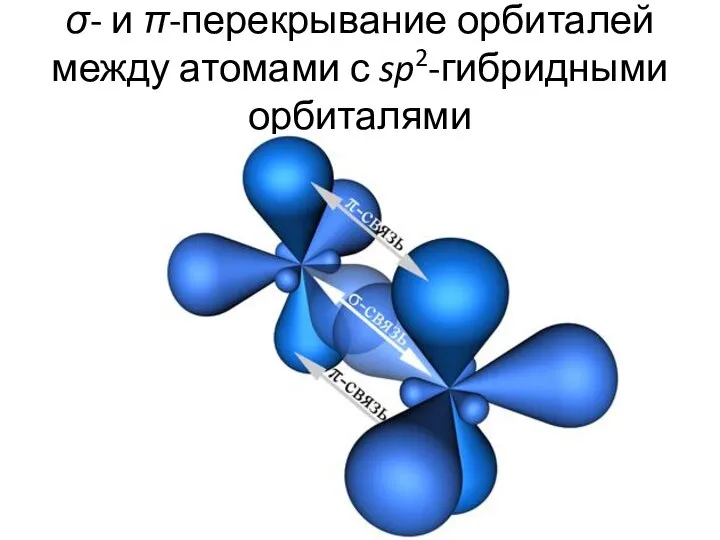
- 24. σ- и π-перекрывание орбиталей между атомами с sp2-гибридными орбиталями
- 25. Примеры соединений, в которых наблюдается sp2-гибридизация: SO3, BCl3, BF3, AlCl3, CO32-, NO3-. все этиленовые углеводороды (алкены)
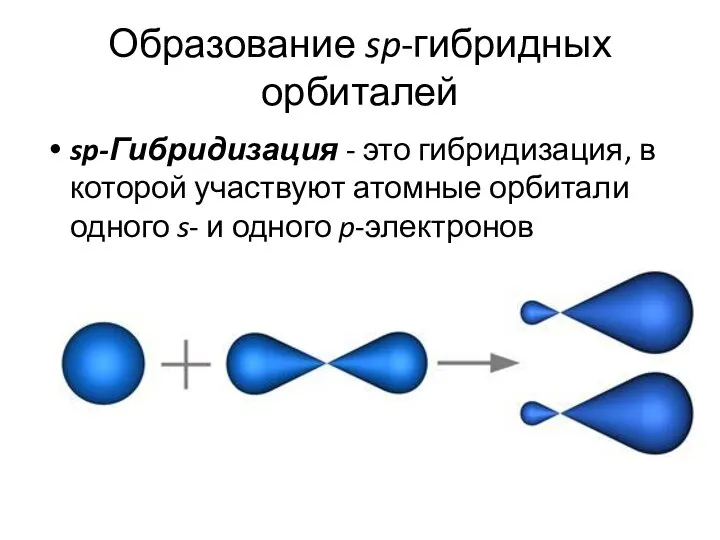
- 26. Образование sp-гибридных орбиталей sp-Гибридизация - это гибридизация, в которой участвуют атомные орбитали одного s- и одного
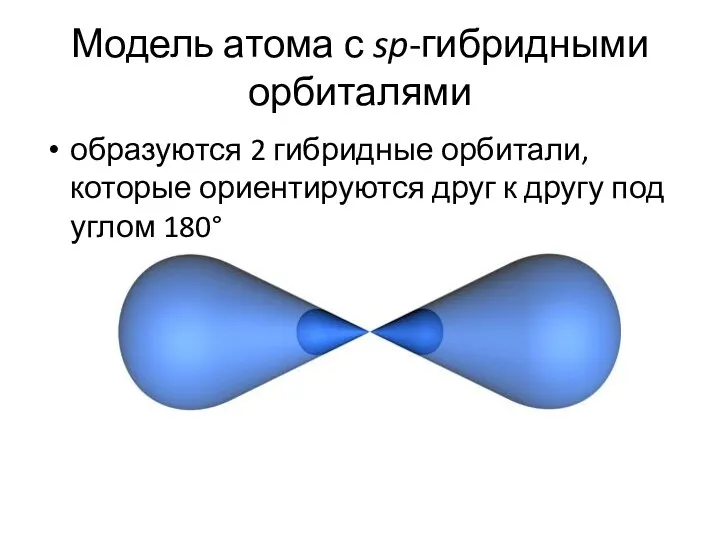
- 27. Модель атома с sp-гибридными орбиталями образуются 2 гибридные орбитали, которые ориентируются друг к другу под углом
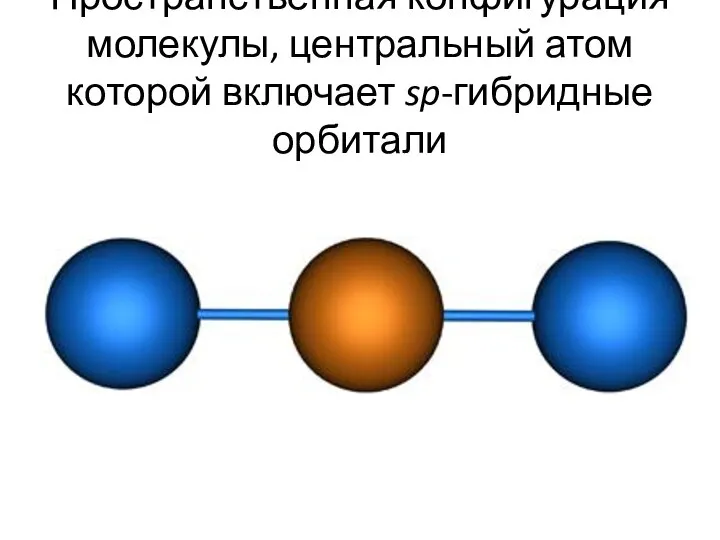
- 28. Пространственная конфигурация молекулы, центральный атом которой включает sp-гибридные орбитали
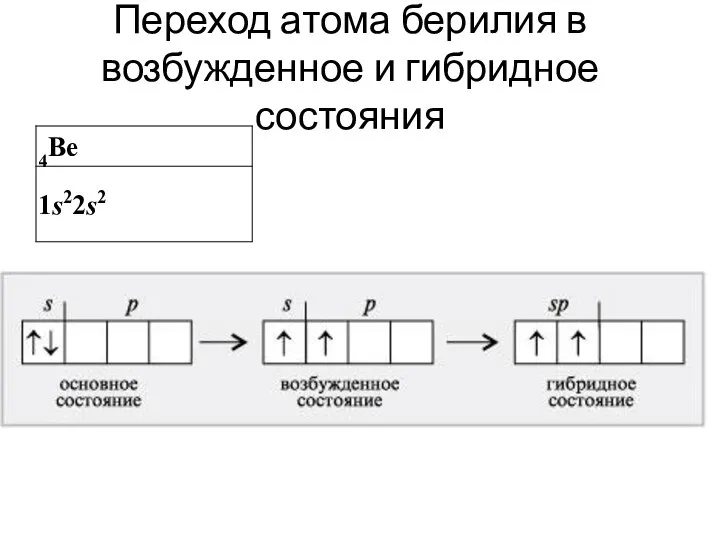
- 29. Переход атома берилия в возбужденное и гибридное состояния
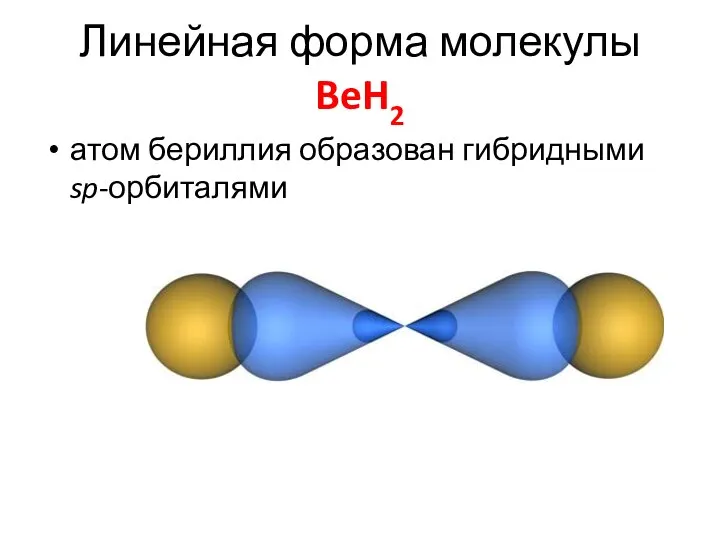
- 30. Линейная форма молекулы BeH2 атом бериллия образован гибридными sp-орбиталями
- 31. Примеры химических соединений, для которых характерна sp-гибридизация: BeCl2, BeH2, CO, CO2, HCN во всех ацетиленовых углеводородах
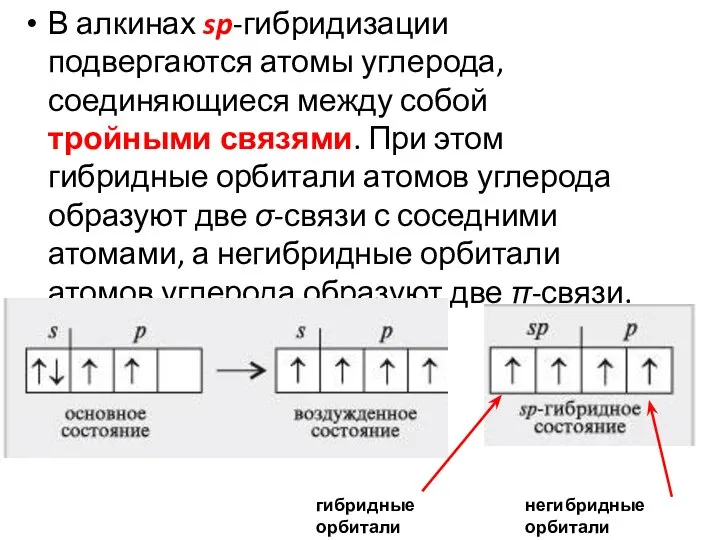
- 32. В алкинах sp-гибридизации подвергаются атомы углерода, соединяющиеся между собой тройными связями. При этом гибридные орбитали атомов
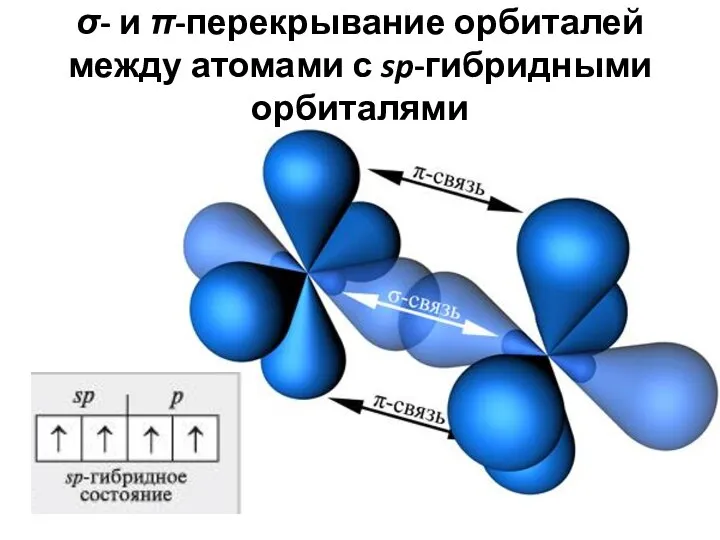
- 33. σ- и π-перекрывание орбиталей между атомами с sp-гибридными орбиталями
- 34. Возможные формы гибридной орбитали за счет комбинации s-, p-,и d-атомных орбиталей Форма этой орбитали зависит от
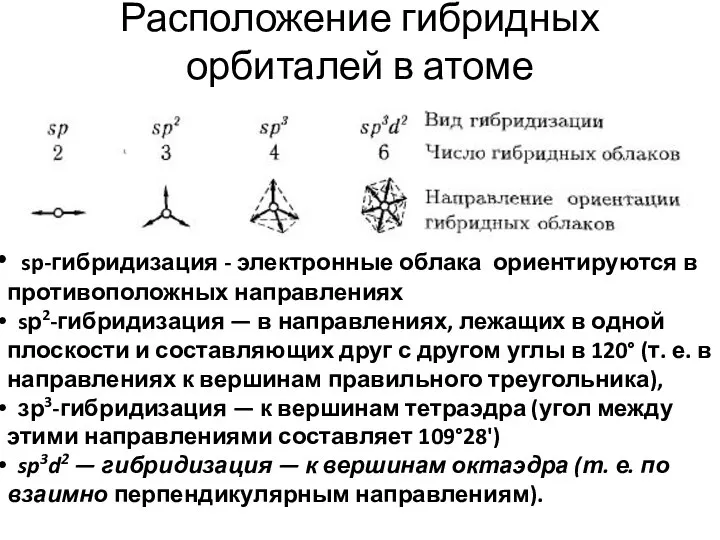
- 35. Расположение гибридных орбиталей в атоме sp-гибридизация - электронные облака ориентируются в противоположных направлениях sр2-гибридизация — в
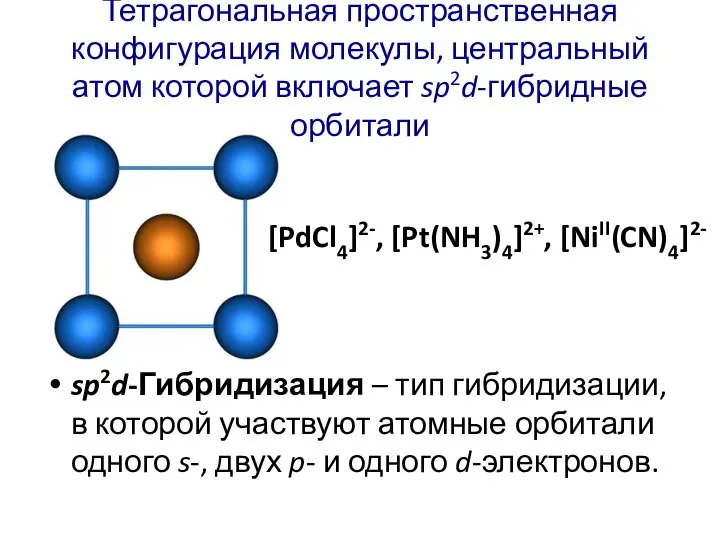
- 36. Тетрагональная пространственная конфигурация молекулы, центральный атом которой включает sp2d-гибридные орбитали sp2d-Гибридизация – тип гибридизации, в которой
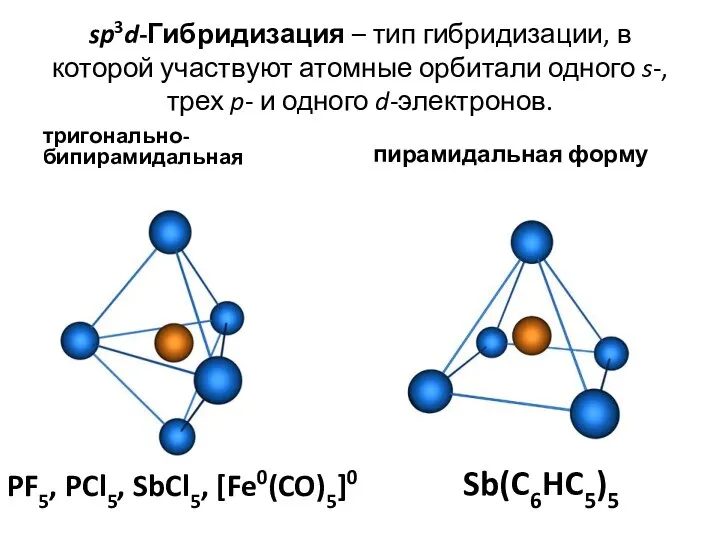
- 37. sp3d-Гибридизация – тип гибридизации, в которой участвуют атомные орбитали одного s-, трех p- и одного d-электронов.
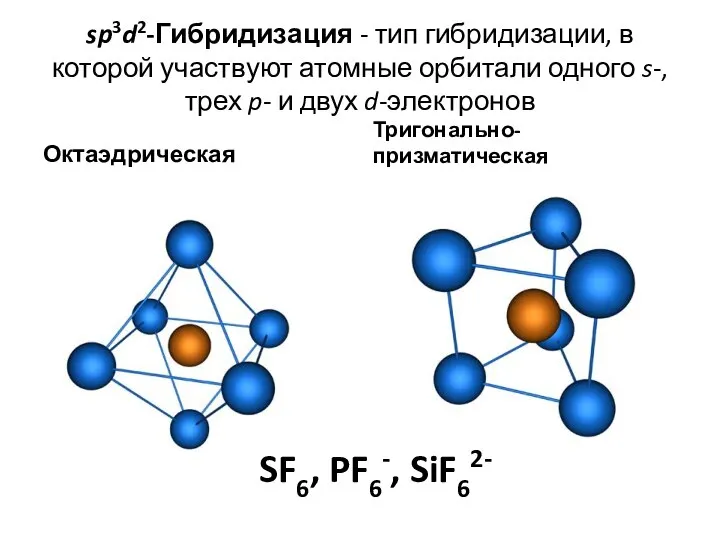
- 38. sp3d2-Гибридизация - тип гибридизации, в которой участвуют атомные орбитали одного s-, трех p- и двух d-электронов
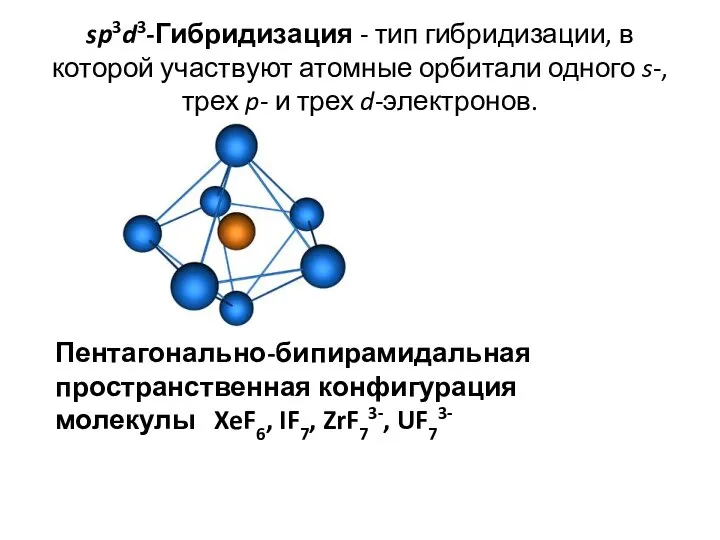
- 39. sp3d3-Гибридизация - тип гибридизации, в которой участвуют атомные орбитали одного s-, трех p- и трех d-электронов.
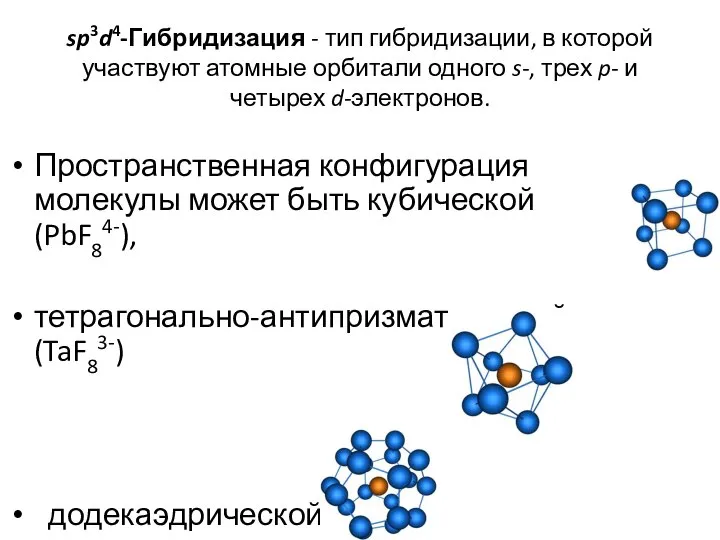
- 40. sp3d4-Гибридизация - тип гибридизации, в которой участвуют атомные орбитали одного s-, трех p- и четырех d-электронов.
- 43. Переход атома углерода в возбужденное и гибридное состояния
- 45. Скачать презентацию
















 Культуральные свойства микроорганизмов. Антибиотики. Методы определения антибиотикорезистентности бактерий
Культуральные свойства микроорганизмов. Антибиотики. Методы определения антибиотикорезистентности бактерий Природные источники углеводородов
Природные источники углеводородов Алканы
Алканы Модифицирование структуры полисахаридов гидрофобными заместителями: твердофазный синтез, исследование структуры и свойств
Модифицирование структуры полисахаридов гидрофобными заместителями: твердофазный синтез, исследование структуры и свойств Химический элемент сера
Химический элемент сера Презентация на тему «Биография Д.И. Менделеева» Работа Ученицы 9 – «А» класса СОШ № 1 Давыдовой Полины Под руководством Конд
Презентация на тему «Биография Д.И. Менделеева» Работа Ученицы 9 – «А» класса СОШ № 1 Давыдовой Полины Под руководством Конд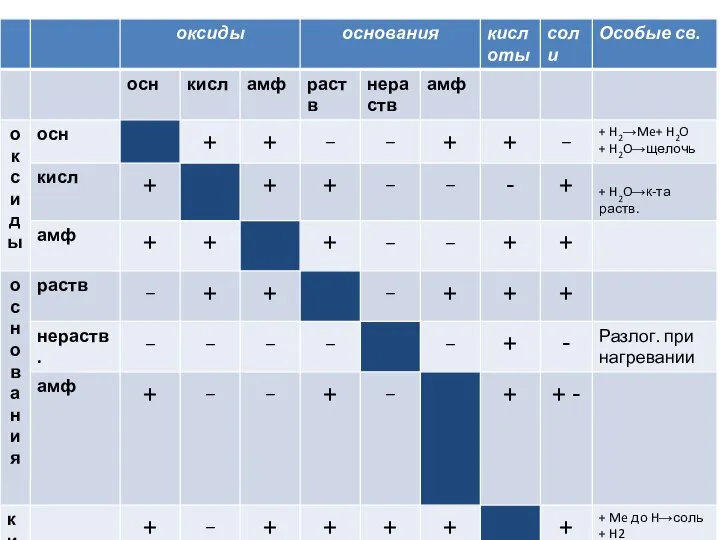 Оксиды, основания, кислоты
Оксиды, основания, кислоты Презентация по Химии "Консерви: користь та шкода" - скачать смотреть бесплатно
Презентация по Химии "Консерви: користь та шкода" - скачать смотреть бесплатно Железо, медь
Железо, медь Виды присадок к моторным топливам. Керосин
Виды присадок к моторным топливам. Керосин 27 февраля 2013
27 февраля 2013 Презентация по Химии "Вплив побутової хімії на здоров'я людини" - скачать смотреть бесплатно
Презентация по Химии "Вплив побутової хімії на здоров'я людини" - скачать смотреть бесплатно Дисперсные
Дисперсные  Строение, свойства и многообразие функций белков
Строение, свойства и многообразие функций белков Титриметрический анализ
Титриметрический анализ Феромагнетики До феромагнетики (ferrum - залізо) належать речовини, магнітна сприйнятливість яких позитивна і досягає значень. Н
Феромагнетики До феромагнетики (ferrum - залізо) належать речовини, магнітна сприйнятливість яких позитивна і досягає значень. Н Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Эндогенная серия. Карбонатитовая группа
Эндогенная серия. Карбонатитовая группа Презентация по Химии "РАЗРАБОТКИ УЛЬТРАДИСПЕРСНЫХ (НАНО-) МАТЕРИАЛОВ И НАНОТЕХНОЛОГИЙ В АТОМНОЙ ОТРАСЛИ" - скачать смотреть б
Презентация по Химии "РАЗРАБОТКИ УЛЬТРАДИСПЕРСНЫХ (НАНО-) МАТЕРИАЛОВ И НАНОТЕХНОЛОГИЙ В АТОМНОЙ ОТРАСЛИ" - скачать смотреть б Химическое равновесие и способы его смещения
Химическое равновесие и способы его смещения Геохимия метасоматтческого процесса. (Лекция 7)
Геохимия метасоматтческого процесса. (Лекция 7) Номенклатура алканов
Номенклатура алканов алгоритм
алгоритм Контрольная работа по химическим реакциям
Контрольная работа по химическим реакциям Упражнения по теме «скорость химической реакции»
Упражнения по теме «скорость химической реакции» Химическая связь
Химическая связь Alkynes
Alkynes №10 зертханалық жұмыс Сірке қышқылы, қасиеттері, алу жолдары
№10 зертханалық жұмыс Сірке қышқылы, қасиеттері, алу жолдары