Слайд 14

СПИСОК ЛИТЕРАТУРЫ
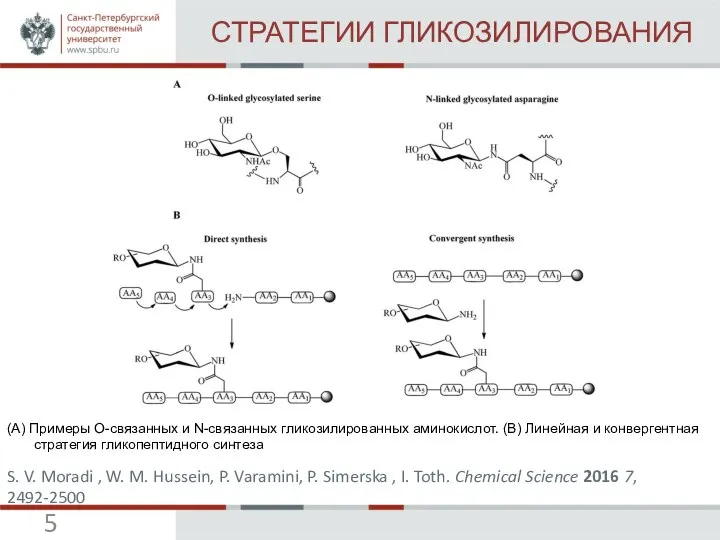
S. V. Moradi , W. M. Hussein, P. Varamini,
P. Simerska and I. Toth. Chemical Science 2016 7, 2492-2500 (IF=9,211).
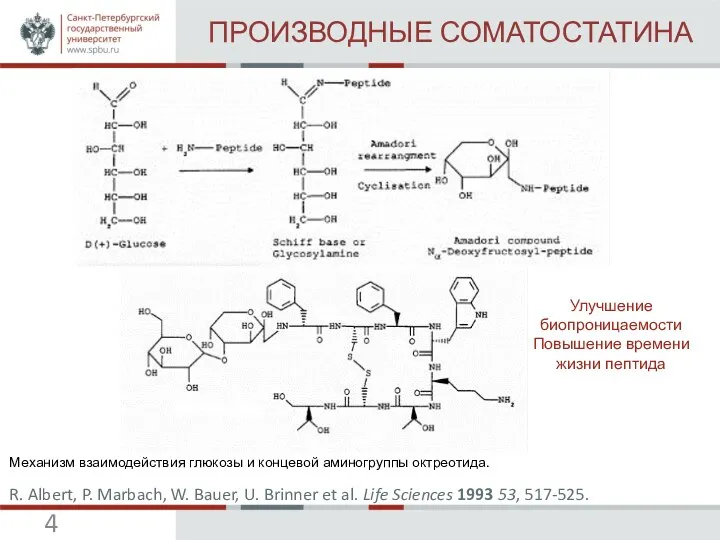
R. Albert, P. Marbach, W. Bauer, U. Brinner et al. Life Sciences 1993 53, 517-525 (IF=2,685).
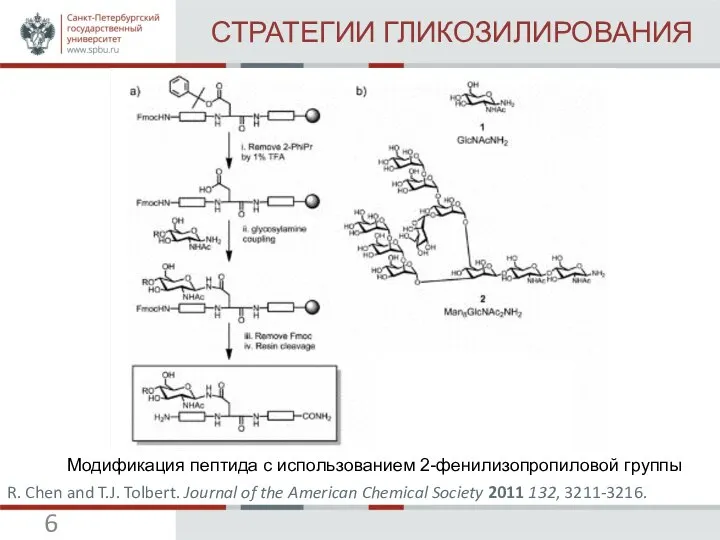
R. Chen and T.J. Tolbert. Journal of the American Chemical Society 2011 132, 3211-3216 (IF=12,113).
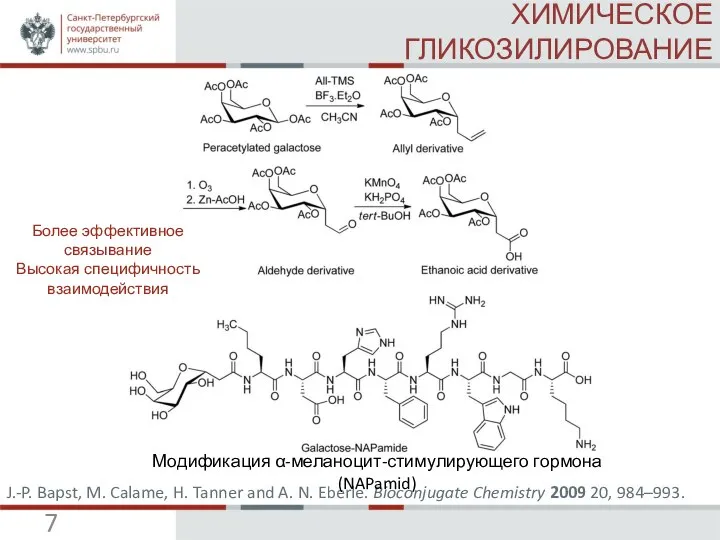
J.-P. Bapst, M. Calame, H. Tanner and A. N. Eberle. Bioconjugate Chemistry 2009 20, 984–993 (IF=4,513).
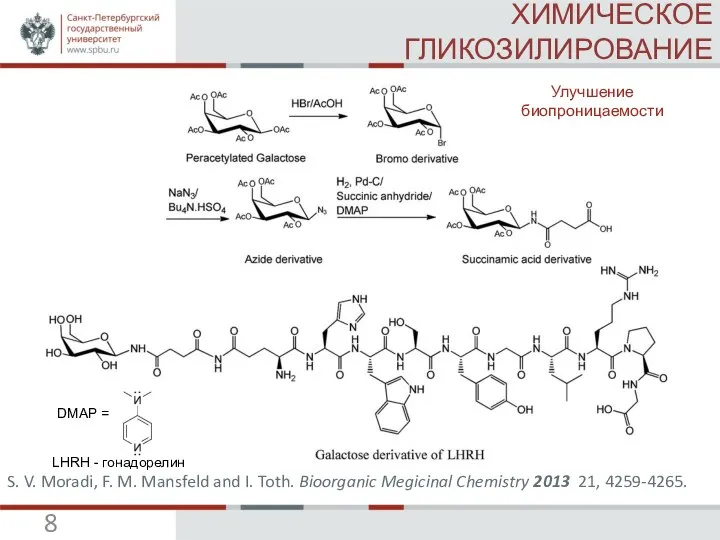
S. V. Moradi, F. M. Mansfeld and I. Toth. Bioorganic Megicinal Chemistry 2013 21, 4259-4265 (IF=2,793).
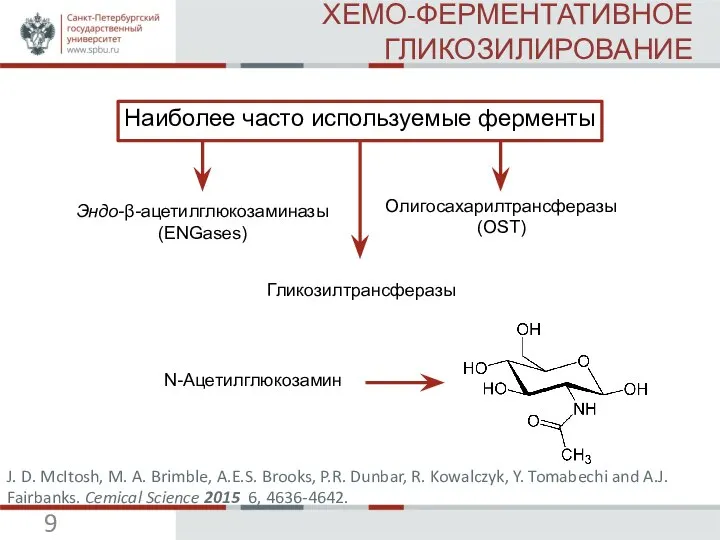
J. D. McItosh, M. A. Brimble, A.E.S. Brooks, P.R. Dunbar, R. Kowalczyk, Y. Tomabechi and A.J. Fairbanks. Chemical Science 2015 6, 4636-4642 (IF=9,211).
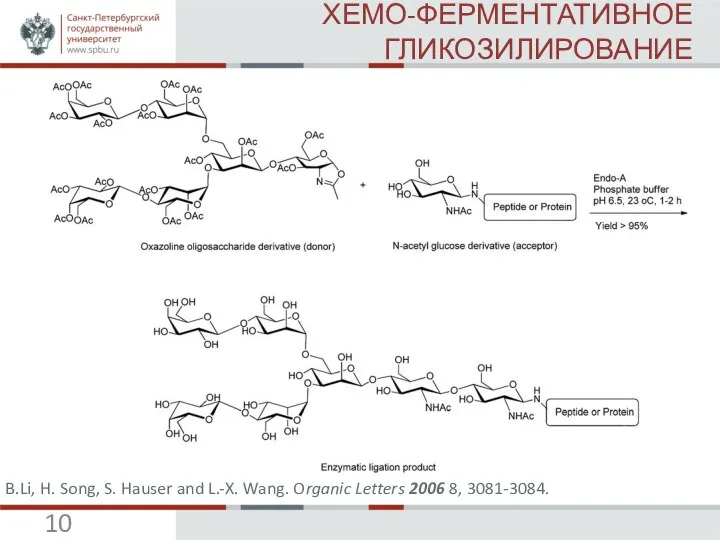
B.Li, H. Song, S. Hauser and L.-X. Wang. Organic Letters 2006 8, 3081-3084 (IF=6,364).
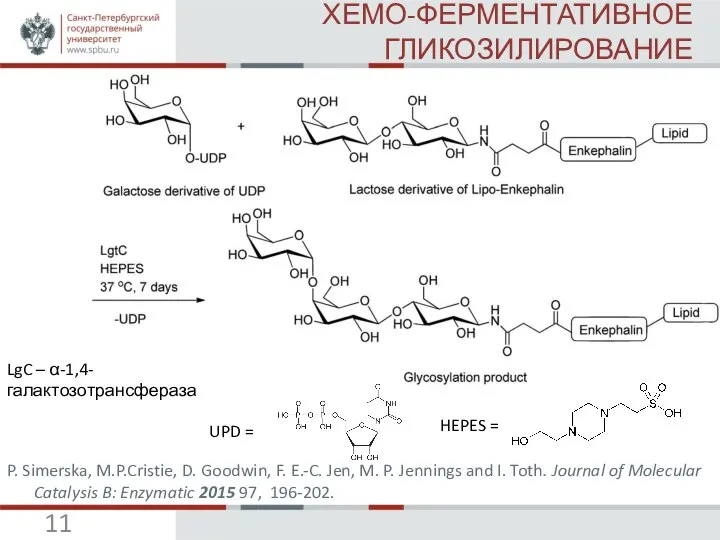
P. Simerska, M.P.Cristie, D. Goodwin, F. E.-C. Jen, M. P. Jennings and I. Toth. Journal of Molecular Catalysis B: Enzymatic 2015 97, 196-202 (IF=2,189).
9. C. Lin, E.H. Chen, L. Y.-L. Lee, R.-L. Hsu, F. Y. Luh. Carbohydrate research 2014 387, 46-53 (IF=2,044).




 Пластмаси, синтетичні каучуки Підготували учениці 11-б класу Оренбургська Марина та Козаренко Таїсія
Пластмаси, синтетичні каучуки Підготували учениці 11-б класу Оренбургська Марина та Козаренко Таїсія  Общая фармакология
Общая фармакология Углерод и его соединения
Углерод и его соединения Обобщающий урок по теме: «Основные классы неорганических соединений. Генетическая связь между классами неорганических соединени
Обобщающий урок по теме: «Основные классы неорганических соединений. Генетическая связь между классами неорганических соединени Урок розв’язування задач
Урок розв’язування задач Ароматичні аміни
Ароматичні аміни Фосфор
Фосфор Углеводы
Углеводы Химическая связь
Химическая связь Мило. Синтетичні миючі засоби.
Мило. Синтетичні миючі засоби.  11 хб
11 хб  Нефелиновые сиениты. Щелочные породы
Нефелиновые сиениты. Щелочные породы Презентация по Химии "Фосфорные удобрения" - скачать смотреть
Презентация по Химии "Фосфорные удобрения" - скачать смотреть  Алкины
Алкины Метаболизм источников энергии
Метаболизм источников энергии Химические волокна
Химические волокна Конструкционные полимеры: классификация, достижения и проблемы
Конструкционные полимеры: классификация, достижения и проблемы Дезодоранты. Выполнили: Ученицы 11-В класса МОУ «Лицей №3» Доровских Алёна Чучуменко Анастасия
Дезодоранты. Выполнили: Ученицы 11-В класса МОУ «Лицей №3» Доровских Алёна Чучуменко Анастасия Поліетелен. Застосування поліетилену
Поліетелен. Застосування поліетилену Аммиак
Аммиак Тотығу-тотықсыздану реакциялары Атырау ХББ НЗМ Косанов Р.П. Химия пәні мұғалімі
Тотығу-тотықсыздану реакциялары Атырау ХББ НЗМ Косанов Р.П. Химия пәні мұғалімі Мило. Мийні засоби
Мило. Мийні засоби Виды присадок к моторным топливам. Керосин
Виды присадок к моторным топливам. Керосин Обобщение и систематизация знаний по теме Химическая связь и строение атома
Обобщение и систематизация знаний по теме Химическая связь и строение атома Химическая промышленность
Химическая промышленность Регуляция обмена веществ
Регуляция обмена веществ Протеины: плюсы и минусы
Протеины: плюсы и минусы Биохимия печени
Биохимия печени