Содержание
- 2. Я скажу себе, друзья, Не боюсь я никогда Ни диктанта, Ни контрольной, Ни стихов и ни
- 3. Содержание презентации 1. История получения аммиака. Строение атома азота. 3. Образование молекулы. 4. Строение молекулы аммиака.
- 4. Аммиак также может быть обязан своим названием оазису бога Аммона в Северной Африке, находящемуся на перекрестке
- 5. По некоторым другим сведениям, аммиак мог получить современное название от древнеегипетского слова «амониан». Так называли всех
- 6. Сокращенное название «аммиак» которым мы всегда пользуемся, ввел в обиход в 1801 году русский ученый-химик, академик
- 7. История открытия аммиака Аммиак был получен в чистом виде в 1774 г. английским химиком Джозефом Луи
- 8. 1723-1802 г. В 1784 французский химик Бертолле разложением аммиака доказал его элементный состав, который в 1787
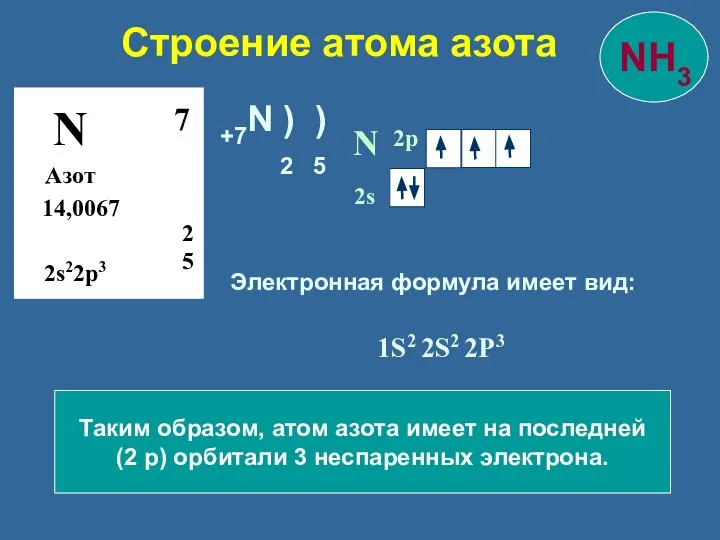
- 9. Строение атома азота N Азот 14,0067 2 5 7 2s22p3 N 2s 2p Таким образом, атом
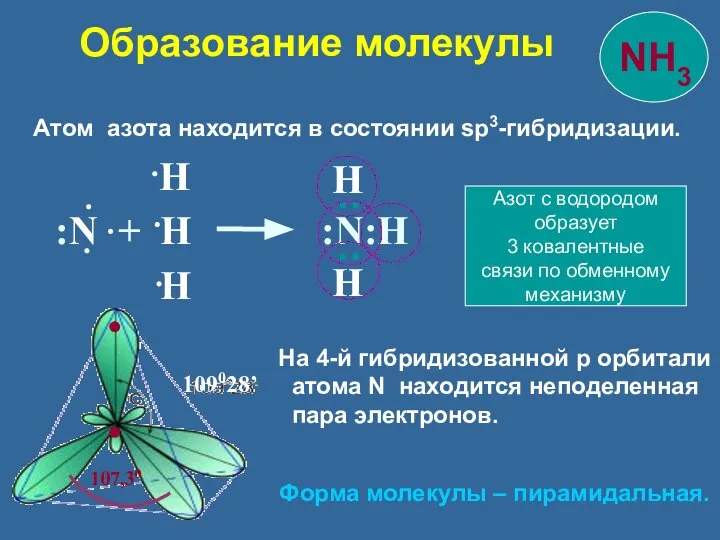
- 10. Атом азота находится в состоянии sp3-гибридизации. 109028’ :N + H :N:Н Н Н Н : :
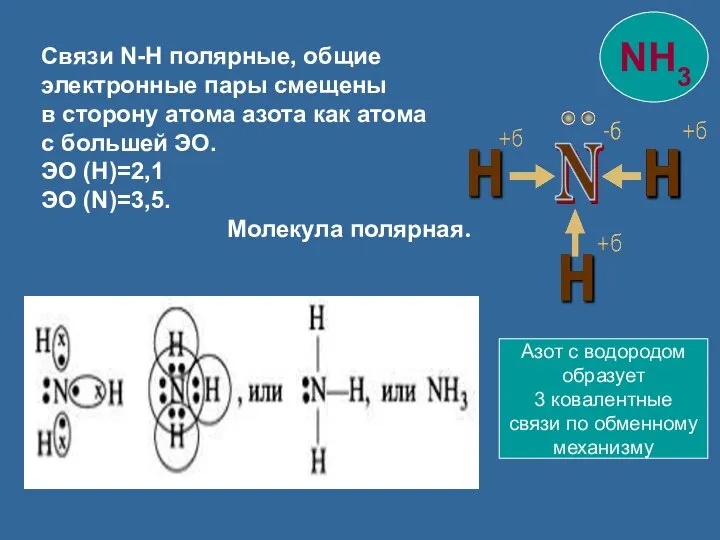
- 11. Связи N-H полярные, общие электронные пары смещены в сторону атома азота как атома с большей ЭО.
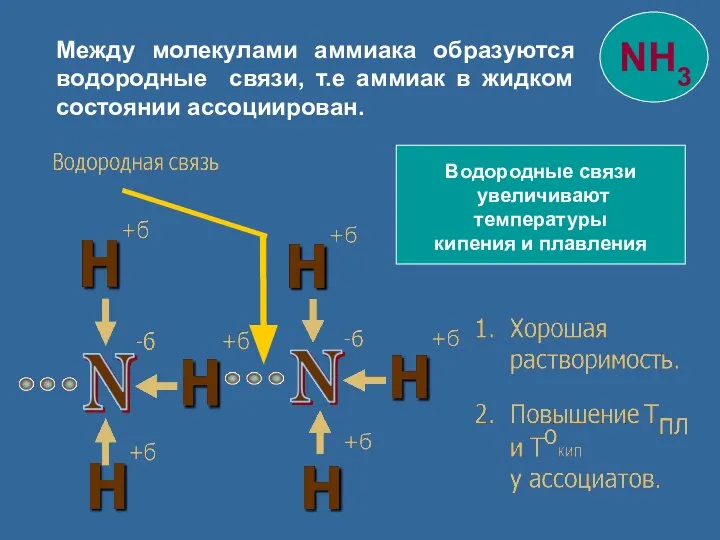
- 12. Водородные связи увеличивают температуры кипения и плавления Между молекулами аммиака образуются водородные связи, т.е аммиак в
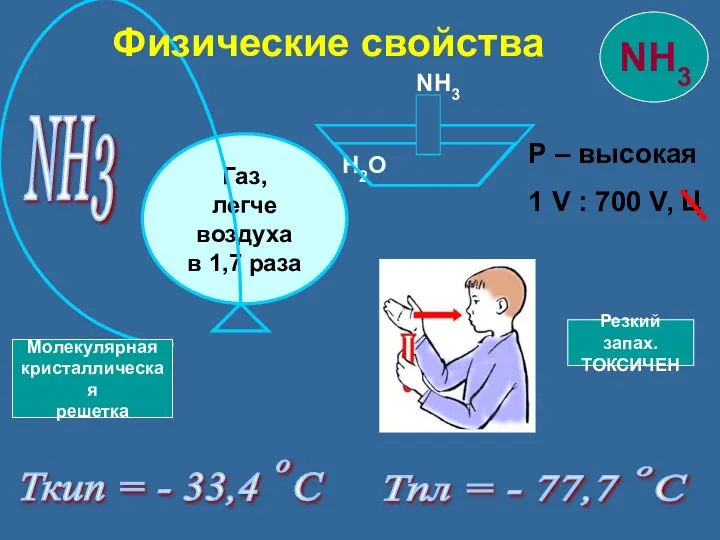
- 13. NH3 Р – высокая 1 V : 700 V, Ц Ткип = - 33,4 С Тпл
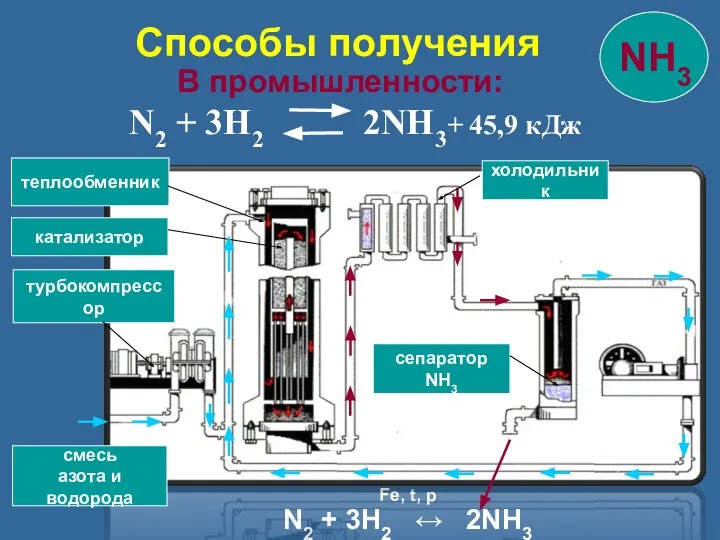
- 14. В промышленности: N2 + 3H2 2NH3+ 45,9 кДж смесь азота и водорода турбокомпрессор катализатор теплообменник холодильник
- 15. В лаборатории: 1. Действием щелочей на соли аммония: 2. Гидролиз нитридов:
- 16. NH3 – низшая степень окисления азота. -3 Аммиак – восстановитель 2. Основные свойства (неподеленная пара электронов)
- 17. Реакция горения аммиака (до N2): 4NH3 + 3O2 = 2N2+ 6H2O = Аммиак-восстановитель
- 18. Каталитическое окисление аммиака (до NO): 4NH3 + 5O2 = 4NO + 6H2O Аммиак-восстановитель
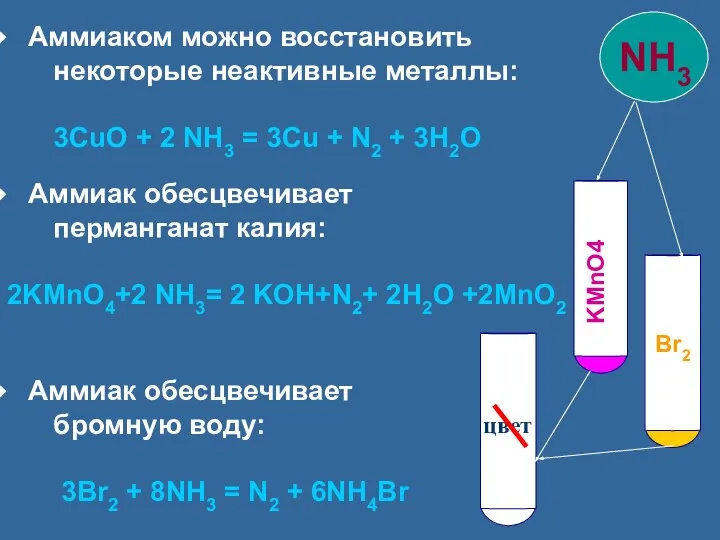
- 19. Аммиаком можно восстановить некоторые неактивные металлы: 3CuO + 2 NH3 = 3Cu + N2 + 3H2O
- 20. Аммиак реагирует с водой, образуя гидрат аммиака (аммиачная вода): NH3 + H2O =NH4OH Изменяет окраску индикаторов:
- 21. NH3 + HCl → NH4Cl хлорид аммония (нашатырь) 2 NH3 + H2SO4 → (NH4)2 SO4 сульфат
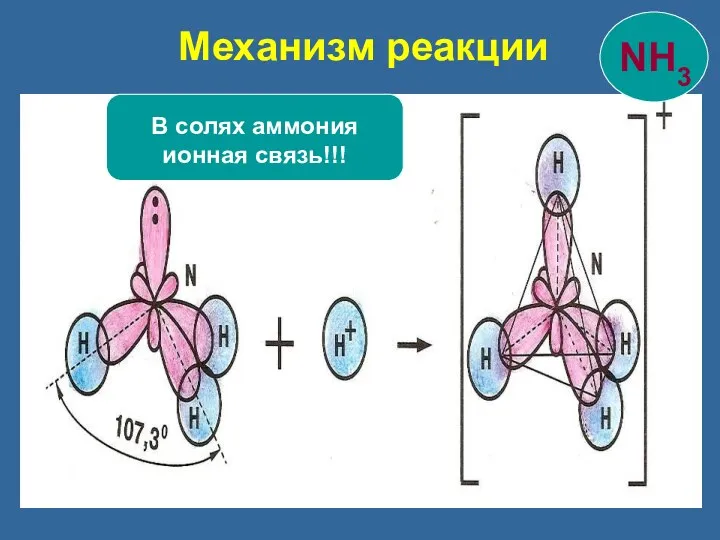
- 22. Механизм реакции В солях аммония ионная связь!!!
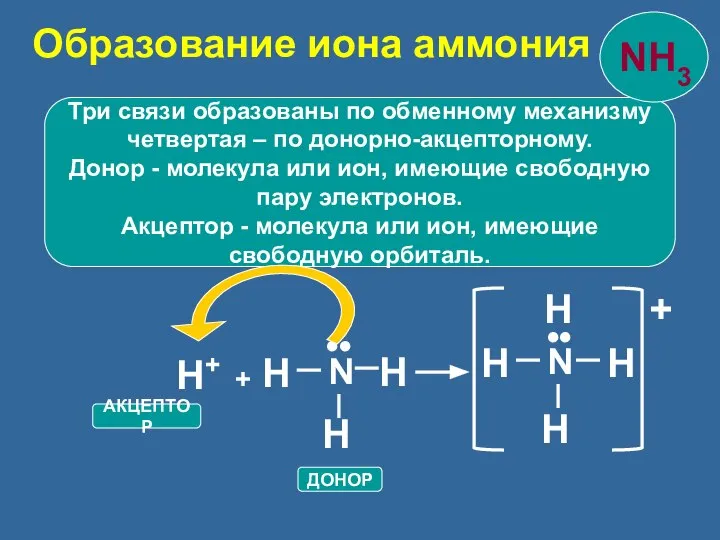
- 23. Три связи образованы по обменному механизму четвертая – по донорно-акцепторному. Донор - молекула или ион, имеющие
- 24. Специфические свойства 1. Взаимодействие с гипохлоритом натрия (образование гидразина): 2NH3 + NaClO = N2H4 + NaCl+H2O
- 25. Специфические свойства 2. Взаимодействие с активными металлами (образование амидов): 2NH3 + 2К = 2KNH2 + Н2
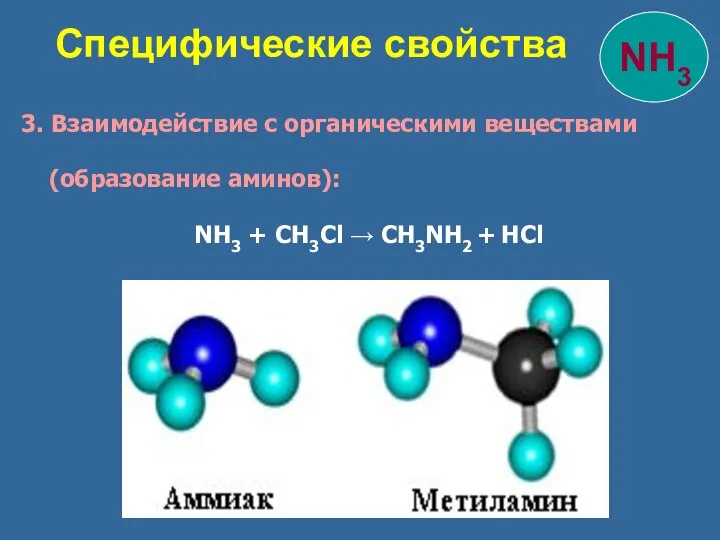
- 26. 3. Взаимодействие с органическими веществами (образование аминов): NH3 + CH3Cl → CH3NH2 + HCl Специфические свойства
- 27. 4. Комплексообразование: CuSO4 + 4NH3 → [Cu(NH3)4]SO4 Cu(OH)2+ 4NH3 → [Cu(NH3)4](OH)2 Специфические свойства Благодаря своим электронодонорным
- 28. Обобщение
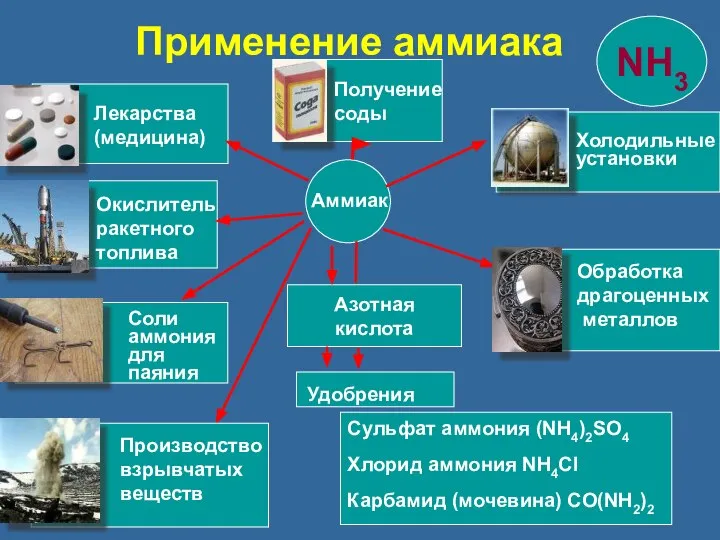
- 29. Азотная кислота Сульфат аммония (NH4)2SO4 Хлорид аммония NH4Cl Карбамид (мочевина) CO(NH2)2 Аммиак Удобрения Лекарства (медицина) Окислитель
- 30. Техногенные катастрофы
- 31. 1. Нельзя прикасаться к разлитому веществу, это может вызвать болезненный ожог кожных покровов. 2. При отравлении
- 32. Правильно! Ошибка Ошибка Ошибка 1 кислот солей оксидов оснований 2 Ошибка Правильно! Ошибка Ошибка щелочами кислотами
- 33. 1. 2. 3. 4. Ответы оснований кислотами синий С оксидами металлов
- 34. Осуществите цепочку превращений: N2?NH3?(NH4)2SO4?NH4Cl?NH3 ?N2 ? Li3N ? NH3 Готовимся к экзамену Запишите уравнения реакций. Где
- 35. Решите задачи: Уровень А: Какой объем аммиака можно получить при нагревании 7,4 г. гидроксида кальция с
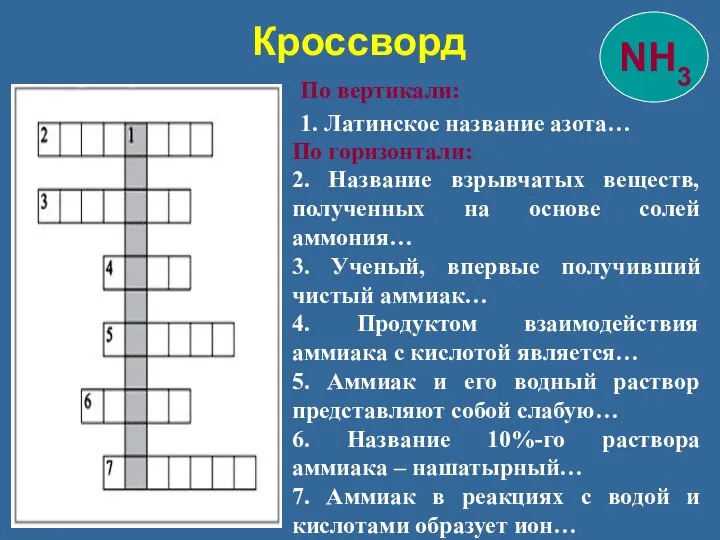
- 36. Кроссворд По вертикали: 1. Латинское название азота… По горизонтали: 2. Название взрывчатых веществ, полученных на основе
- 38. Скачать презентацию















![4. Комплексообразование: CuSO4 + 4NH3 → [Cu(NH3)4]SO4 Cu(OH)2+ 4NH3 → [Cu(NH3)4](OH)2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/748107/slide-26.jpg)






 Металлические элементы группы IA. ЛИТИЙ. Работу выполнила: Ученица 11 класса Иванова Ксения
Металлические элементы группы IA. ЛИТИЙ. Работу выполнила: Ученица 11 класса Иванова Ксения Муниципальное общеобразовательное учреждение «Средняя общеобразовательная школа п. Соцземледельский Балашовского района Сарат
Муниципальное общеобразовательное учреждение «Средняя общеобразовательная школа п. Соцземледельский Балашовского района Сарат Явище ізомерії. Структурна ізомерія Близнюки органічного світу
Явище ізомерії. Структурна ізомерія Близнюки органічного світу  Презентация по Химии "Каучук" - скачать смотреть
Презентация по Химии "Каучук" - скачать смотреть  Галогенопохідні ароматичних вуглеводнів
Галогенопохідні ароматичних вуглеводнів Гетерофункциональные органические соединения. Таутомерия. Стереоизомерия
Гетерофункциональные органические соединения. Таутомерия. Стереоизомерия Оксиды. Классификация. Номенклатура. Физические и химические свойства. Получение. Применение
Оксиды. Классификация. Номенклатура. Физические и химические свойства. Получение. Применение ГИА по химии
ГИА по химии Ароматические углеводороды. (Лекция 7)
Ароматические углеводороды. (Лекция 7) Месторождения железистых кварцитов
Месторождения железистых кварцитов Вода. Растворы. Растворение
Вода. Растворы. Растворение Мышьяк (лат. аrsenicum)
Мышьяк (лат. аrsenicum) Способ вызвать быструю, но контролируемую коррозию железа
Способ вызвать быструю, но контролируемую коррозию железа Ионообменная хроматография
Ионообменная хроматография Драгоценные камни
Драгоценные камни Кремний (Silicium). Химические свойства
Кремний (Silicium). Химические свойства Кремнийорганическая гипотеза
Кремнийорганическая гипотеза ИЗВЕСТНЫЕ УЧЕНЫЕ – ХИМИКИ Немного из истории химии
ИЗВЕСТНЫЕ УЧЕНЫЕ – ХИМИКИ Немного из истории химии Теория химического строения Бутлерова. Предмет органической химии. Первое положение теории Бутлерова
Теория химического строения Бутлерова. Предмет органической химии. Первое положение теории Бутлерова Полисахариды
Полисахариды Материаловедение. Теория сплавов
Материаловедение. Теория сплавов Титриметрические методы анализа
Титриметрические методы анализа Магматические горные породы
Магматические горные породы Электронное и пространственное строение молекул органических соединений – основа их биологической активности
Электронное и пространственное строение молекул органических соединений – основа их биологической активности Растворы. Теория электролитической диссоциации (лекция 6)
Растворы. Теория электролитической диссоциации (лекция 6) Методы исследования химического состава нефти и продуктов ее переработки
Методы исследования химического состава нефти и продуктов ее переработки Синтетический каучук и его применение
Синтетический каучук и его применение Презентация по Химии "Химический КВН" - скачать смотреть
Презентация по Химии "Химический КВН" - скачать смотреть