Содержание
- 2. Химической кинетикой называют учение о скорости химических реакций и зависимости ее от различных условий – природы
- 3. Скоростью гетерогенной реакции называется количество вещества, вступающего в реакцию или образующегося при реакции за единицу времени
- 6. Влияние концентрации. Скорость гомогенной реакции, протекающей при постоянной температуре, прямо пропорциональна произведению концентраций реагирующих веществ. υ
- 7. Влияние температуры Согласно правилу Вант-Гоффа, при повышении температуры на каждые 10оС скорость реакции увеличивается в 2-4
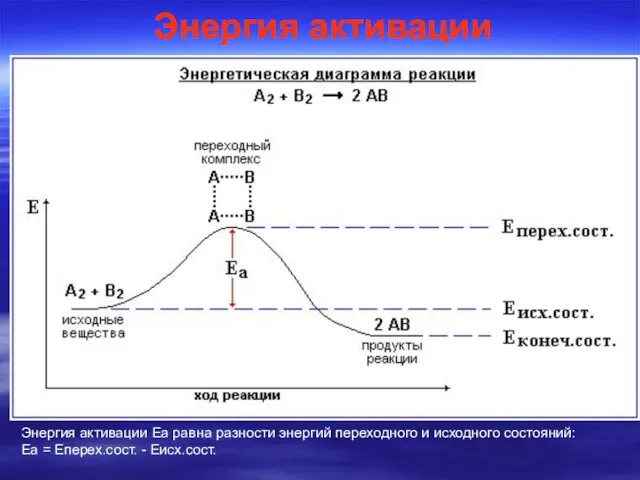
- 8. Избыточная энергия, которой должны обладать молекулы для того, чтобы их столкновение могло привести к образованию нового
- 9. Энергия активации Энергия активации Еа равна разности энергий переходного и исходного состояний: Еа = Еперех.сост. -
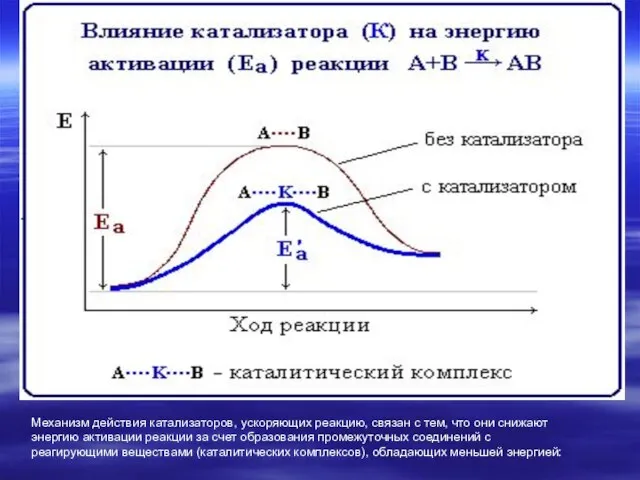
- 10. Влияние катализатора Катализаторы – вещества, которые могут активизировать реакцию или изменять ее скорость, но не изменяют
- 11. Механизм действия катализаторов, ускоряющих реакцию, связан с тем, что они снижают энергию активации реакции за счет
- 12. Селективность катализатора Cпособность ускорять одну из возможных при данных условиях параллельных реакций. Благодаря этому можно, применяя
- 13. Ингибиторы Механизм действия ингибиторов аналогичен механизму действия катализаторов – они участвуют в промежуточных стадиях процесса. Следствием
- 14. Сложные химические реакции
- 15. Виды сложных реакций Обратимые – реакция идет в двух направлениях: прямом и обратном NH4CNO↔(NH2)2CO (получение карбамида)
- 16. Цепные реакции Цепные – это реакции, состоящие из ряда последовательных стадий, когда активные частицы, образующиеся в
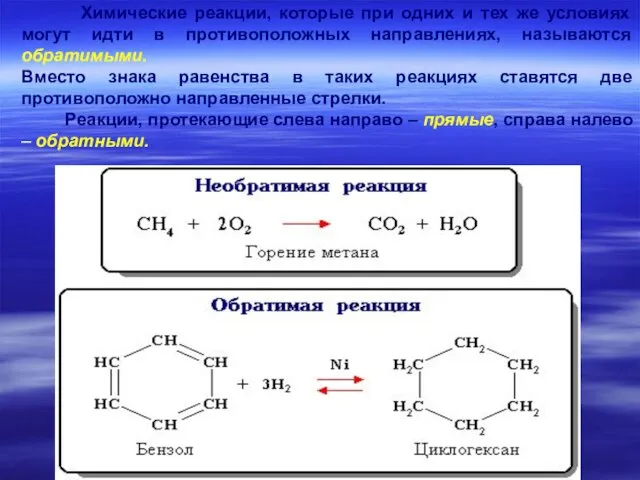
- 17. Химические реакции, которые при одних и тех же условиях могут идти в противоположных направлениях, называются обратимыми.
- 18. Состояние, в котором скорость обратной реакции становится равной скорости прямой реакции, называется химическим равновесием.
- 20. Анри-Луи Ле Шателье (1850—1936) — член Парижской академии наук, президент Французского химического общества — широко известен
- 21. Принцип Ле Шателье Направление сдвига равновесия в общем виде определяется принципом Ле Шателье: Если находящаяся в
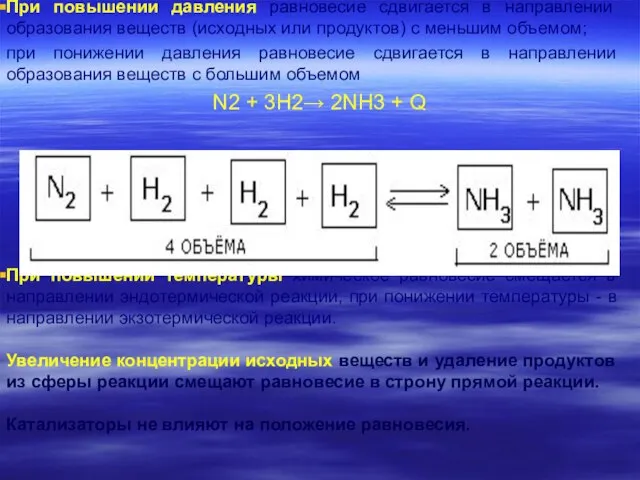
- 22. При повышении давления равновесие сдвигается в направлении образования веществ (исходных или продуктов) с меньшим объемом; при
- 23. Рассмотрим применение принципа Ле Шателье к различным типам воздействия: 1. Увеличение концентрации исходных веществ и удаление
- 25. Список используемых источников Глинка Н.Л. Общая химия: Учебное пособие для вузов/Под ред. А.И. Ермакова. – М.:
- 26. Скорость химической реакции не зависит от: а) концентрации реагирующих веществ; б) температуры ; в) концентрации продуктов
- 27. Какой из законов является основополагающим в области химической кинетики: а) закон постоянства состава; б) закон объемных
- 28. На состояние химического равновесия, как правило, не влияет: а) изменение давления; б) изменение температуры; в) использование
- 29. На сколько градусов надо повысить температуру, чтобы скорость реакции возросла в 625 раз при температурном коэффициенте
- 30. В каком случае система приходит в состояние химического равновесия: а) при оптимальном давлении в системе; б)
- 31. Чем объясняется повышение скорости реакции при введении в систему катализатора: а) уменьшением энергии активации; б) увеличением
- 32. Назовите вещества, снижающие скорость химической реакции: а) катализаторы; б) окислители; в) ингибиторы; г) красители.
- 34. Скачать презентацию



























 Аварії з викидом хімічних небезпечних речовин та їх класифікація
Аварії з викидом хімічних небезпечних речовин та їх класифікація Бескислородные керамические материалы
Бескислородные керамические материалы Основания. Определение. Номенклатура
Основания. Определение. Номенклатура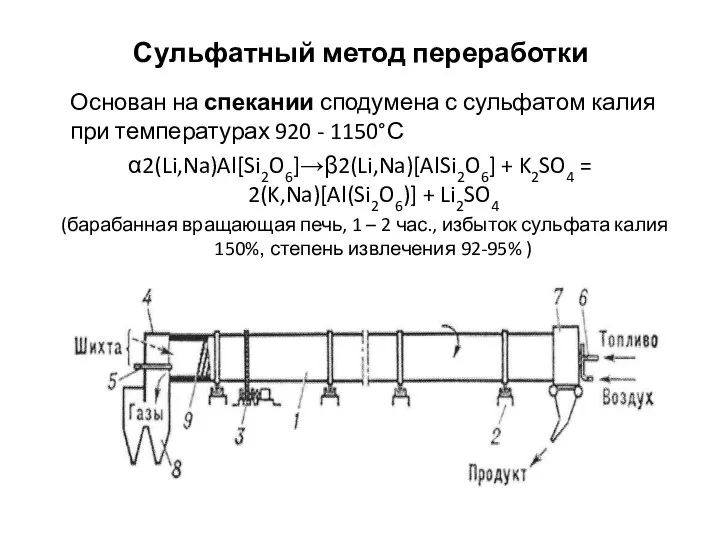 Сульфатный метод переработки
Сульфатный метод переработки Азот
Азот Кадмий (Cadmium)
Кадмий (Cadmium) Терпены и стероиды
Терпены и стероиды Гетерогенное ионное равновесие. Реакции обмена
Гетерогенное ионное равновесие. Реакции обмена Властивості газів
Властивості газів Растворы. Процесс растворения
Растворы. Процесс растворения Стеклянные товары. Основные сырьевые материалы для производства стекла
Стеклянные товары. Основные сырьевые материалы для производства стекла Химико-технологические процессы современных производств. Лекция №3
Химико-технологические процессы современных производств. Лекция №3 Растворы. Первичные понятия
Растворы. Первичные понятия Констукционные и функциональные волокнистые композиты
Констукционные и функциональные волокнистые композиты Исследовательский проект. Коллаген
Исследовательский проект. Коллаген Бордос сұйықтығын дайындау және оның сапасын тексеру
Бордос сұйықтығын дайындау және оның сапасын тексеру Презентация по Химии "Фосфор" - скачать смотреть бесплатно_
Презентация по Химии "Фосфор" - скачать смотреть бесплатно_ Установка пиролиза широкой фракции, легких углеводородов
Установка пиролиза широкой фракции, легких углеводородов Коллоидная химия
Коллоидная химия Природные соединения кремния
Природные соединения кремния Строение и свойства комплексных соединений
Строение и свойства комплексных соединений Превращения в нашей жизни: физические и химические
Превращения в нашей жизни: физические и химические Evolution of Isoconversional Methods
Evolution of Isoconversional Methods Металлы
Металлы «Предмет органической химии. Особенности органических веществ». По учебнику О. С. Габриеляна. 9 класс
«Предмет органической химии. Особенности органических веществ». По учебнику О. С. Габриеляна. 9 класс Чугуны. Структура и свойства. Классификация и применение
Чугуны. Структура и свойства. Классификация и применение Гидрокаталитические процессы
Гидрокаталитические процессы Підготувала: Учениця 10-Б класу Іщенко Інна
Підготувала: Учениця 10-Б класу Іщенко Інна