Содержание
- 2. Содержание Гетерогенное равновесие в насыщенном растворе малорастворимого сильного электролита. Произведение растворимости Влияние на растворимость электролита введения
- 3. Произведение растворимости Гетерогенное равновесие в насыщенном водном растворе малорастворимого сильного электролита KmAn между осадком электролита и
- 4. Значения ПР малорастворимых электролитов при 250С В насыщенном растворе сильного малорастворимого электролита произведение равновесных молярных концентраций
- 5. Расчет растворимости СаСО3 Обозначим S – растворимость карбоната кальция , моль/л – растворимость карбоната кальция ,
- 6. Соотношение растворимости и ПР Для малорастворимого электролита KmAn, растворимость которого S KmAn(к) mKn+ + nAm- Концентрации
- 7. Расчет растворимости Сa3(PO4)2 и Ag2S Растворимость Сa3(PO4)2 (m = 3, n = 2) Растворимость Ag2S (m
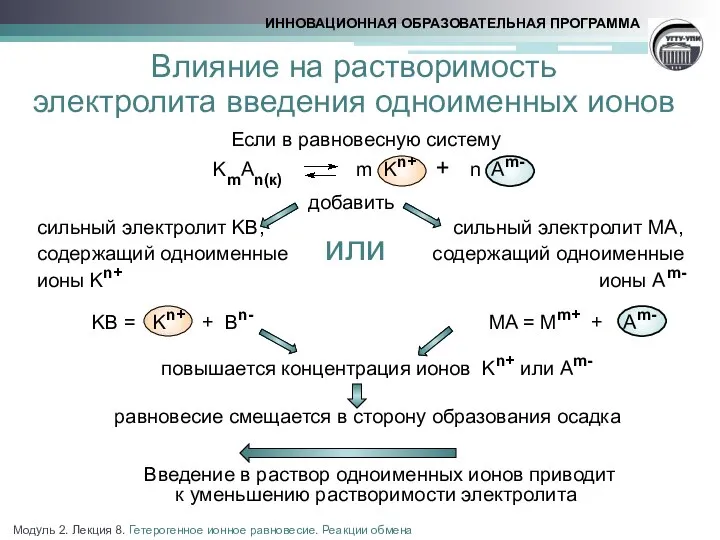
- 8. Если в равновесную систему KmAn(к) m Kn+ + n Am- добавить сильный электролит KB, сильный электролит
- 9. СdСО3(к) Сd2+ + СО32- Растворимость карбоната кадмия Расчет растворимости карбоната кадмия в 0,1М растворе Na2CO3 Концентрация
- 10. Условие выпадения и растворения осадка Используя значение ПР, можно определить возможность образования или растворения осадка в
- 11. Определение возможности образования осадка BaSO4 Определите, образуется ли осадок BaSO4 при сливании равных объемов 0,001 М
- 12. Реакции обмена в растворах электролитов Обменные реакции (реакции обмена) – реакции в растворах электролитов, в ходе
- 13. Примеры необратимых реакций обмена Образование малорастворимого вещества (осадка) Pb(NO3)2 + 2KI = PbI2↓ + 2KNO3 Pb2+
- 14. Направление реакций обмена Реакции, в которых исходные вещества и продукты реакции содержат малорастворимые соединения, должны быть
- 15. Определение направления реакции MnS + 2HCl H2S + MnCl2 MnS + 2H+ H2S + Mn2+ После
- 16. Определение направления реакции CuS + 2HCl H2S + CuCl2 CuS + 2H+ H2S + Cu2+ KC
- 17. Заключение Константу равновесия в насыщенном растворе малорастворимого сильного электролита между осадком электролита и его ионами в
- 19. Скачать презентацию















 Ion exchange
Ion exchange Кристалл Гришина Л.А., учитель физики МКС(К) ОУ С (К) ОШ 37 I II вида г. Новосибирск
Кристалл Гришина Л.А., учитель физики МКС(К) ОУ С (К) ОШ 37 I II вида г. Новосибирск Презентація на тему: “Поняття про полімери на прикладі поліетилену”
Презентація на тему: “Поняття про полімери на прикладі поліетилену”  Соли и классы химических веществ
Соли и классы химических веществ Определение разных форм угольной кислоты
Определение разных форм угольной кислоты Строение углеводородов
Строение углеводородов Классификация углеводов. Глюкоза
Классификация углеводов. Глюкоза Синтез новых аллильных производных семикарбазонов и тиосемикарбазонов Пиррол-2-карбальдегидов
Синтез новых аллильных производных семикарбазонов и тиосемикарбазонов Пиррол-2-карбальдегидов Водород
Водород  Валентність
Валентність  Ферроцен. Свойства, получение и применение
Ферроцен. Свойства, получение и применение Основні характеристики атомних електростанцій (АЕС) та підприємств ядерного паливного циклу
Основні характеристики атомних електростанцій (АЕС) та підприємств ядерного паливного циклу Изотермический распад переохлажденного аустенита
Изотермический распад переохлажденного аустенита Презентация по Химии "«Химические волокна»" - скачать смотреть
Презентация по Химии "«Химические волокна»" - скачать смотреть  Три кити нанохімії
Три кити нанохімії Гiдроксикислоти. Номенклатура
Гiдроксикислоти. Номенклатура Комплексные соединения
Комплексные соединения Виды присадок к моторным топливам. Присадки к дизельному топливу
Виды присадок к моторным топливам. Присадки к дизельному топливу Понятие фазы вещества. Насыщенный пар и его свойства. Влажность воздуха. Приборы для измерения влажности воздуха
Понятие фазы вещества. Насыщенный пар и его свойства. Влажность воздуха. Приборы для измерения влажности воздуха Конструкция ферментатора
Конструкция ферментатора Электролитическая диссоциация. Устойчивость комплексных соединений
Электролитическая диссоциация. Устойчивость комплексных соединений Щелочные металлы
Щелочные металлы Низкомолекулярные биорегуляторы терпены
Низкомолекулярные биорегуляторы терпены Серная кислота H2SO4
Серная кислота H2SO4 Хроматографические методы анализа
Хроматографические методы анализа Металлы и сплавы, Металлы и сплавы, их свойства и применение в радиоэлектронной аппаратуре Подготовил: учащийся гр.7/8 профессия
Металлы и сплавы, Металлы и сплавы, их свойства и применение в радиоэлектронной аппаратуре Подготовил: учащийся гр.7/8 профессия Адсорбция-фазалар бөлу беттерінде жүретін бір компоненттің екінші компонентке сіңуі
Адсорбция-фазалар бөлу беттерінде жүретін бір компоненттің екінші компонентке сіңуі Диаграммы состояния двухкомпонентных систем типа твердое тело – жидкость
Диаграммы состояния двухкомпонентных систем типа твердое тело – жидкость