Содержание
- 2. Основные виды и характеристики химической связи. Ковалентная связь. Методы описания ковалентной связи: 1) метод валентных схем
- 3. Химическая связь – совокупность сил, удерживающих атомы в молекуле, радикале, ионе; – совокупность взаимодействий между электронами
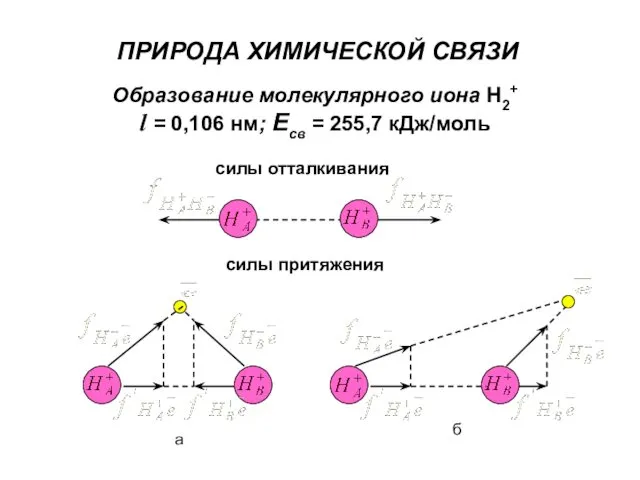
- 4. ПРИРОДА ХИМИЧЕСКОЙ СВЯЗИ Образование молекулярного иона Н2+ l = 0,106 нм; Есв = 255,7 кДж/моль силы
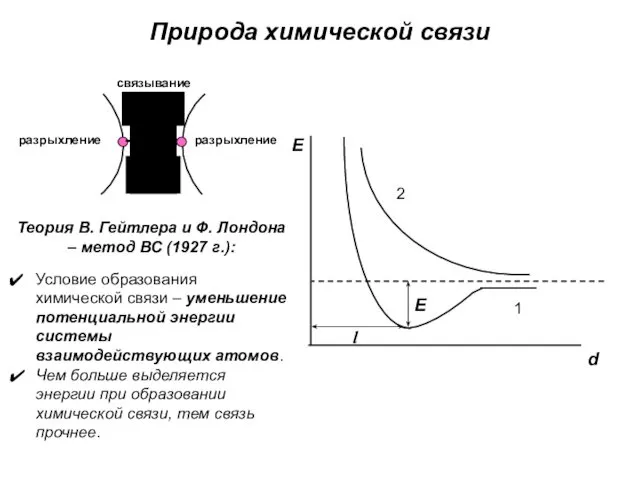
- 5. Природа химической связи Теория В. Гейтлера и Ф. Лондона – метод ВС (1927 г.): Условие образования
- 6. 1. КОВАЛЕНТНАЯ ХИМИЧЕСКАЯ СВЯЗЬ Ковалентная химическая связь – это связь, которая возникает между атомами за счет
- 7. МЕТОД ВАЛЕНТНЫХ СХЕМ (метод ВС) Основные положения: 1. Химическая связь – это результат перекрывания внешних атомных
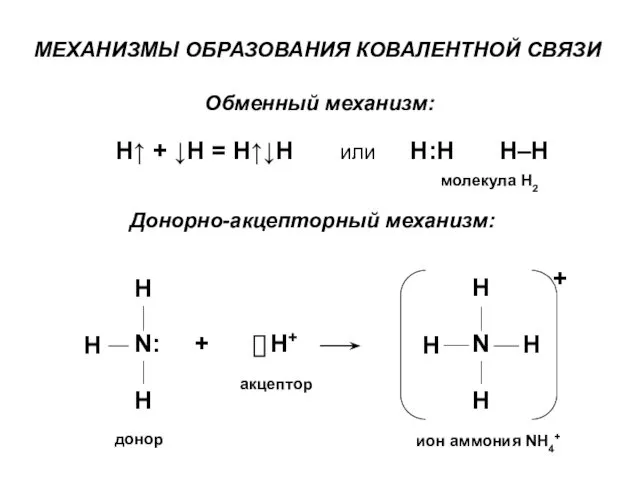
- 8. 5. Образование общей электронной пары связи может происходить за счет: а) обмена неспаренными электронами атомов (обменный
- 10. МЕХАНИЗМЫ ОБРАЗОВАНИЯ КОВАЛЕНТНОЙ СВЯЗИ Донорно-акцепторный механизм: + донор акцептор ион аммония NH4+ молекула Н2
- 11. ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ 1. Длина химической связи (l, м, нм, Ǻ) – межъядерное расстояние между химически
- 12. ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ ***Для двухатомных ковалентных молекул энергия связи (Есв) численно равна энергии диссоциации (Едис) молекул
- 13. ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ Пример: Энергия, поглощаемая в процессе: Н2О = 2Н + О – 924 кДж,
- 14. ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ Энергия химической связи ЕА-В зависит от длины lА-В и от кратности связи 3.
- 15. ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ 5. Валентный угол – угол между воображаемыми линиями, проходящими через ядра химически связанных
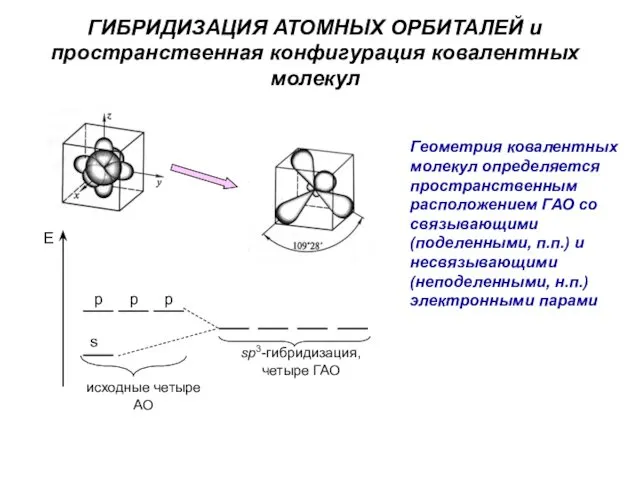
- 16. ГИБРИДИЗАЦИЯ АТОМНЫХ ОРБИТАЛЕЙ и пространственная конфигурация ковалентных молекул Подходы к рассмотрению геометрии (пространственной конфигурации) ковалентных молекул:
- 17. ГИБРИДИЗАЦИЯ АТОМНЫХ ОРБИТАЛЕЙ и пространственная конфигурация ковалентных молекул Геометрия ковалентных молекул определяется пространственным расположением ГАО со
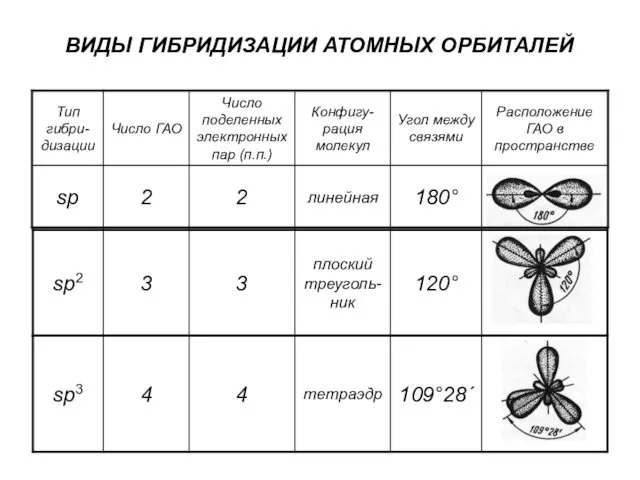
- 18. ВИДЫ ГИБРИДИЗАЦИИ АТОМНЫХ ОРБИТАЛЕЙ
- 20. Скачать презентацию











 Возникновение и развитие понятия «валентность» в период с 1850 по 1865 гг
Возникновение и развитие понятия «валентность» в период с 1850 по 1865 гг Презентация по Химии "Вклад Д.И. Менделеева в развитие агрохимии. Значение его вклада в современном сельском хозяйстве" - скач
Презентация по Химии "Вклад Д.И. Менделеева в развитие агрохимии. Значение его вклада в современном сельском хозяйстве" - скач Презентация по Химии "Презентация Кристаллические и аморфные тела" - скачать смотреть
Презентация по Химии "Презентация Кристаллические и аморфные тела" - скачать смотреть  Любимый Алюминий
Любимый Алюминий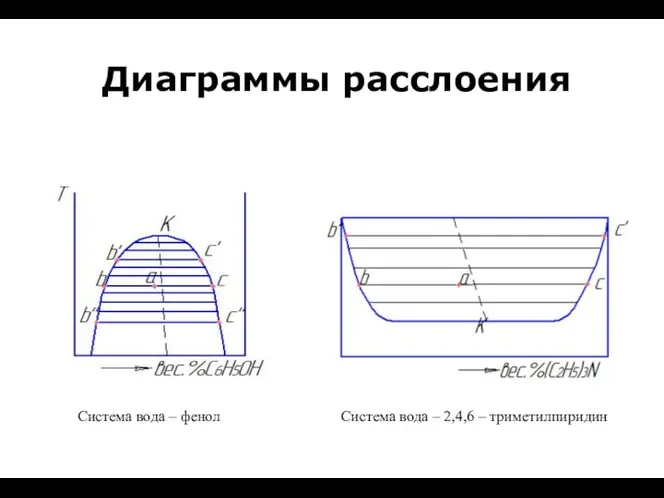 Диаграммы расслоения
Диаграммы расслоения Хімія в побуті
Хімія в побуті Изотопы. (8 класс)
Изотопы. (8 класс) Опал
Опал Состав воды. Минералы + грязь + примеси
Состав воды. Минералы + грязь + примеси Железо и его свойства Алексей | 9 А класс | Школа № 97
Железо и его свойства Алексей | 9 А класс | Школа № 97  Химия: измерения
Химия: измерения Презентация по Химии "Кристаллы вокруг нас" - скачать смотреть
Презентация по Химии "Кристаллы вокруг нас" - скачать смотреть 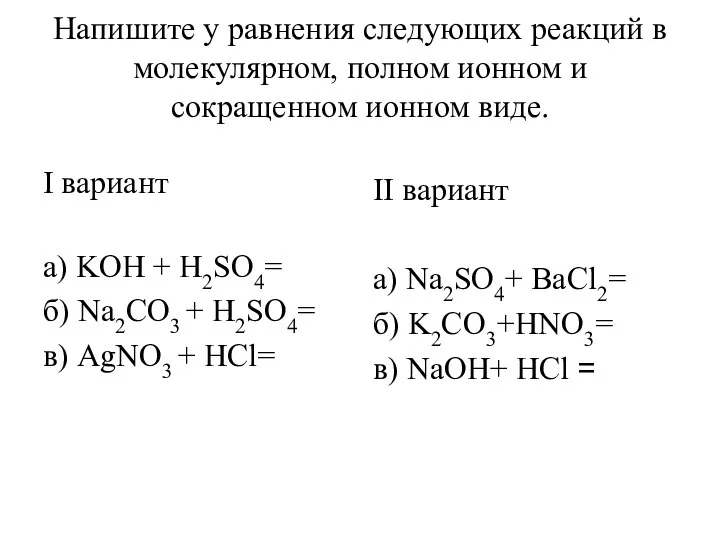 Уравнения реакций в молекулярном, полном ионном и сокращенном ионном виде
Уравнения реакций в молекулярном, полном ионном и сокращенном ионном виде Оксид цинка
Оксид цинка Нуклеиновые кислоты
Нуклеиновые кислоты Лаборатория мирового уровня в области термического анализа и физико-химии процессов тепловых методов добычи
Лаборатория мирового уровня в области термического анализа и физико-химии процессов тепловых методов добычи Камни и Стрелец
Камни и Стрелец Генетика. Лекция 5 Генотип. Геном. Кариотип. Геномные мутации. Генный баланс. Компенсация доз генов. Эволюция генома.
Генетика. Лекция 5 Генотип. Геном. Кариотип. Геномные мутации. Генный баланс. Компенсация доз генов. Эволюция генома.  Кроссворд по теме: Алканы
Кроссворд по теме: Алканы Моделирование электронной структуры и сенсорных свойств наноструктурированных смешанных оксидов
Моделирование электронной структуры и сенсорных свойств наноструктурированных смешанных оксидов Фосфатные породы
Фосфатные породы Окислительно–восстановительные реакции (ОВР)
Окислительно–восстановительные реакции (ОВР) Дать характеристику новому классу органических веществ
Дать характеристику новому классу органических веществ  Химия 1 (1)
Химия 1 (1) Превращение (S)-бутанол-2 в другие соединения
Превращение (S)-бутанол-2 в другие соединения Периодическая система Д.И. Менделеева
Периодическая система Д.И. Менделеева Кислоты и классы химических веществ. 8 класс
Кислоты и классы химических веществ. 8 класс Типы кристаллических структур минералов. Формулы. Классификация
Типы кристаллических структур минералов. Формулы. Классификация