Содержание
- 2. Виды химической связи ковалентная ионная металлическая водородная
- 3. Ковалентная связь и механизмы ее образования Механизмы образования ковалентной связи Выделяют два механизма образования ковалентной связи:
- 4. В случае донорно-акцепторного механизма одна частица (донор) предоставляет собственную неподеленную электронную пару, а вторая частица (акцептор)
- 5. Донорно-акцепторная связь на примере образования молекулы хлорида метиламмония Такая связь образуется между атомом азота в молекуле
- 6. σ-, π-Связи При образовании ковалентной связи в молекулах общая электронная пара заселяет связывающие молекулярные орбитали, имеющие
- 7. Различное строение σ- и π-молекулярных орбиталей определяет характерные особенности σ- и π-связей. σ-Связь прочнее π-связи; по
- 8. Кратность ковалентной связи Кратность ковалентной связи определяется числом общих электронных пар, образующихся между атомами. Каждую общую
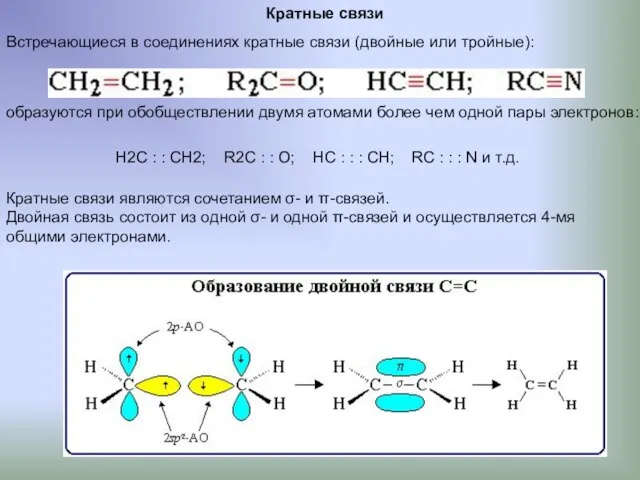
- 9. Кратные связи Встречающиеся в соединениях кратные связи (двойные или тройные): образуются при обобществлении двумя атомами более
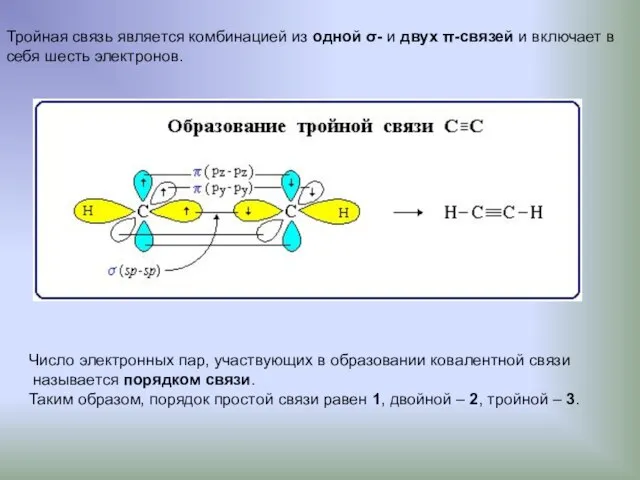
- 10. Тройная связь является комбинацией из одной σ- и двух π-связей и включает в себя шесть электронов.
- 11. Характеристики ковалентной связи Важными количественными характеристиками ковалентной связи являются энергия связи, ее длина и дипольный момент.
- 12. Насыщаемость ковалентной связи Насыщаемость ковалентной связи обусловлена ограниченным числом неспаренных электронов в атоме,ограниченными возможностями атома выступать
- 13. Направленность ковалентной связи Направленность ковалентной связи обусловлена определенным пространственным расположением электронных орбиталей взаимодействующих атомов. Так, угол
- 14. Условия неполярности молекулы высокая симметричность (наличие более двух осей симметрии) отсутствие неподеленных электронных пар у центрального
- 16. Ионная связь Химическая связь, основанная на электростатическом притяжении ионов, называется ионной связью. Иoннaя связь не имеет
- 17. Металлическая связь Атомы металлов отличаются от атомов других элементов тем, что сравнительно слабо удерживают свои внешние
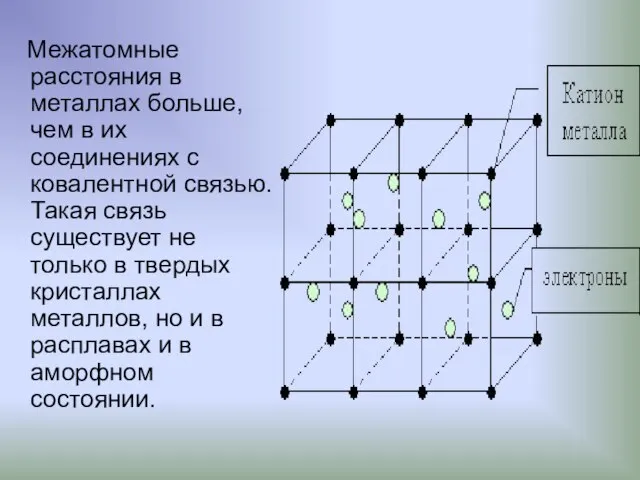
- 18. Межатомные расстояния в металлах больше, чем в их соединениях с ковалентной связью. Такая связь существует не
- 20. Водородные связи
- 21. Водородные связи (Н-связи) Атом водорода, связанный с сильно электроотрицательным элементом (азотом, кислородом, фтором и др.), испытывает
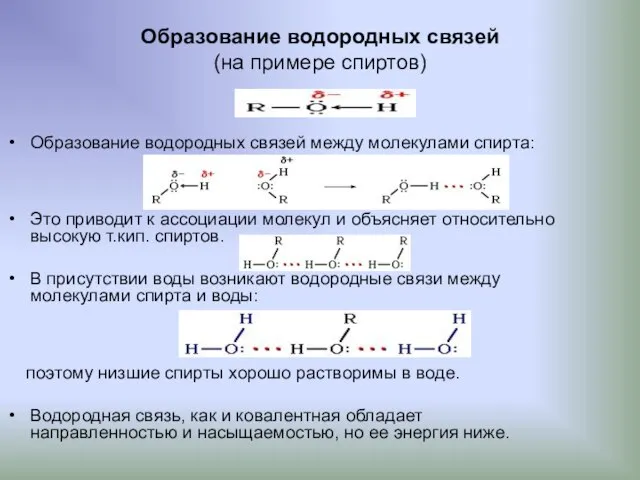
- 22. Образование водородных связей (на примере спиртов) Образование водородных связей между молекулами спирта: Это приводит к ассоциации
- 24. Скачать презентацию

















 Сложные эфиры
Сложные эфиры Фазовое равновесие в насыщенном растворе малорастворимого электролита. (Глава 4. Задача 10)
Фазовое равновесие в насыщенном растворе малорастворимого электролита. (Глава 4. Задача 10) фізичні властивості полімеру спиртів та карбонових кислот
фізичні властивості полімеру спиртів та карбонових кислот  Химические индикаторы
Химические индикаторы Обмен липидов
Обмен липидов Технология производства простых полиэфиров
Технология производства простых полиэфиров Презентация по Химии "Форфор" - скачать смотреть
Презентация по Химии "Форфор" - скачать смотреть  Вода ценный дар природы. Биологическая роль воды
Вода ценный дар природы. Биологическая роль воды Геохимия урана и тория в карбонатитовом процессе
Геохимия урана и тория в карбонатитовом процессе Физическая и коллоидная химия
Физическая и коллоидная химия Физические явления в химии (8 класс)
Физические явления в химии (8 класс) Қабаттағы мұнай
Қабаттағы мұнай Як прості речовини
Як прості речовини  Цинк. Знаходження в періодичній системі і основні характеристики
Цинк. Знаходження в періодичній системі і основні характеристики Адам мен жануар организміне бордың әсері
Адам мен жануар организміне бордың әсері Высокомолекулярные вещества полимеры
Высокомолекулярные вещества полимеры Окислительно-восстановительные процессы. Лекция 8
Окислительно-восстановительные процессы. Лекция 8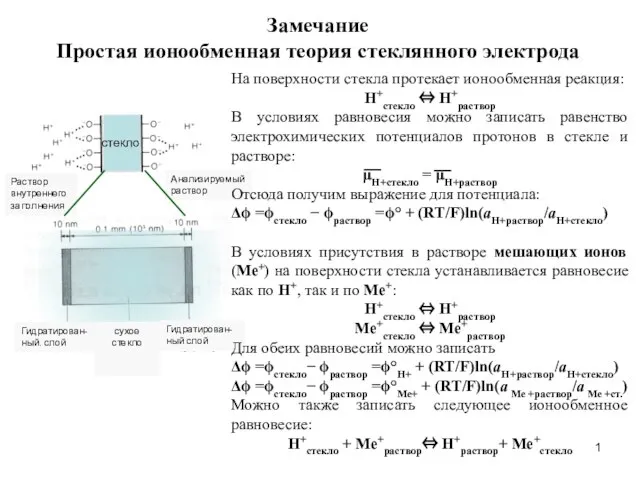 Простая ионообменная теория стеклянного электрода
Простая ионообменная теория стеклянного электрода Биологический метод исследования. Определение патогенности и вирулентности микроорганизмов
Биологический метод исследования. Определение патогенности и вирулентности микроорганизмов Работа выполнена обучающейся 9 «А» класса МОУ «СОШ №2» Мусафировой Анастасией
Работа выполнена обучающейся 9 «А» класса МОУ «СОШ №2» Мусафировой Анастасией Химия, 8. Урок 1
Химия, 8. Урок 1 Биопластики: область применения
Биопластики: область применения Производные карбоновых кислот. Ненасыщенные карбоновые кислоты
Производные карбоновых кислот. Ненасыщенные карбоновые кислоты Caustic Soda
Caustic Soda Презентация по Химии "Неметаллы" - скачать смотреть
Презентация по Химии "Неметаллы" - скачать смотреть  Презентация по Химии "Биополимеры" - скачать смотреть
Презентация по Химии "Биополимеры" - скачать смотреть  Химия в пищевой промышленности
Химия в пищевой промышленности Интересные факты о нефти
Интересные факты о нефти