Содержание
- 2. Термодинамика - это отрасль науки, изучающая взаимные превращения различных видов энергии, связанные с переходом энергии в
- 3. Объектом термодинамического исследования есть термодинамическая система. Система - совокупность объектов отделенных из окружающего мира реально существующими
- 4. По взаимодействию с окружающей средой термодинамические системы делят на: открытые – обмениваются с окружающей средой веществом
- 5. Система называется гетерогенной, если в системе есть реальные поверхности раздела , отделяющие друг от друга части
- 6. Первое начало термодинамики
- 7. Состояние системы – совокупность свойств системы, позволяющих определить систему с точки зрения термодинамики. Свойства и состояние
- 8. Внутренняя энергия Каждая термодинамическая система обладает определенным запасом энергии, которая называется внутренней энергией. Внутренняя энергия системы
- 9. Величина внутренней энергии зависит от природы тела, его массы, химического состава и параметров, которые обусловливают состояние
- 10. Первый закон термодинамики 1. Энергия не исчезает без следа и не возникает ни из чего, а
- 11. Первый закон термодинамики при различных термодинамических процессах: Изохорный - происходит при постоянном объеме (V=const) А=р*(V2-V1); ∆V=0;
- 12. Изобарный процесс (р=const) Q=∆U+p∆V Q=(U2-U1)+p(V2-V1) = U2-U1+pV2-pV1= (U2+pV2)-(U1+pV1) H ≡ U+pV – энтальпия – запас энергии
- 13. Термохимические уравнения: Термохимическими называют уравнения в которых кроме формул исходных веществ и продуктов реакции со стехиометрическими
- 14. Тепловым эффектом химической реакции называют максимальное количество теплоты, которая выделяется или поглощается при постоянном объеме или
- 15. Закон Гесса: Тепловой эффект химической реакции не зависит от пути (механизма) ее течения, а только определяется
- 16. Самостоятельно повторить пять следствий закона Гесса
- 17. Второе начало термодинамики
- 18. Процессы могут быть: Термодинамически обратимым называется процесс, который можно реализовать в прямом и обратном направлениях при
- 19. Теплота не может сама собой переходить от холодного тела к горячему, не оставляя изменений в окружающей
- 21. 3) Энтропия- мера беспорядка, хаоса в системе. Чем больше ∆T, тем беспорядочнее тепловое движение частиц, следовательно
- 22. В изолированной системе процесс протекает самопроизвольно только, если энтропия возрастает: ∆S≥0 В открытых и закрытых системах
- 23. Свободная энергия Гиббса – функция состояния при изобарно-изотермическом процессе – это та часть энергии, которая может
- 24. Химическое равновесие Обратимая реакция - химическая реакция, которая при одних и тех же условиях может идти
- 25. В состоянии химического равновесия ∆G = 0 Существует полезное соотношение, связывающее изменение свободной энергии Гиббса ∆G
- 27. Скачать презентацию























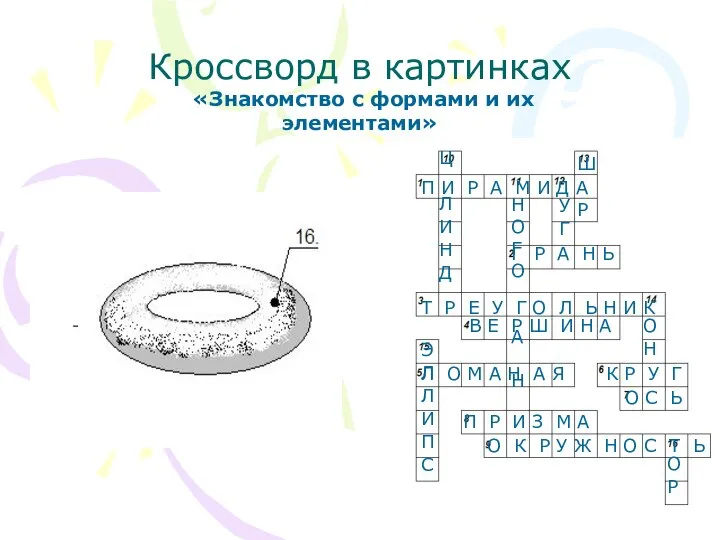 Кроссворд в картинках. Знакомство с формами и их элементами
Кроссворд в картинках. Знакомство с формами и их элементами Презентация к уроку по теме: «Алканы» Учитель химии Колесникова Г.Т.
Презентация к уроку по теме: «Алканы» Учитель химии Колесникова Г.Т. IVA группа С, Si, Ge, Sn, Pb (подгруппа титана)
IVA группа С, Si, Ge, Sn, Pb (подгруппа титана) Зависимость свойств веществ от их строения. Химическая связь. Основные виды химической связи
Зависимость свойств веществ от их строения. Химическая связь. Основные виды химической связи Определение химического состава почвы пришкольного участка
Определение химического состава почвы пришкольного участка Илік заттар. Тітіркендіруші заттар. Қапталғыш заттар, адсорбциялаушы заттар
Илік заттар. Тітіркендіруші заттар. Қапталғыш заттар, адсорбциялаушы заттар Алкены. Пропилен
Алкены. Пропилен Каталіз: каталітичне гідрування
Каталіз: каталітичне гідрування Класифікація, будова та номенклатура органічних сполук
Класифікація, будова та номенклатура органічних сполук Газификация тяжёлых нефтяных остатков. Конверсия природного газа
Газификация тяжёлых нефтяных остатков. Конверсия природного газа Основы химической термодинамики
Основы химической термодинамики Азотистая кислота
Азотистая кислота Кислоты, основания, соли в свете ТЭД подготовила: Мартынова Е.Ю._
Кислоты, основания, соли в свете ТЭД подготовила: Мартынова Е.Ю._ Непредельные углеводороды: этилен
Непредельные углеводороды: этилен Понятие об адсорбционной влаге
Понятие об адсорбционной влаге Пиримидин (шестичленный гетероцикл с двумя атомами азота)
Пиримидин (шестичленный гетероцикл с двумя атомами азота) Викторина на тему: «Щелочные и щелочноземельные металлы в гомеопатии»
Викторина на тему: «Щелочные и щелочноземельные металлы в гомеопатии» Коллоидная химия
Коллоидная химия Изоморфизм, изоморфизмнің түрлері. Полиморфизм. Сульфидтер класының жалпы сипаттамасы
Изоморфизм, изоморфизмнің түрлері. Полиморфизм. Сульфидтер класының жалпы сипаттамасы Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки
Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки Полимеры и их использование
Полимеры и их использование Важнейшие минералы
Важнейшие минералы Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химическая кинетика
Химическая кинетика Презентация по Химии "Изотопы" - скачать смотреть
Презентация по Химии "Изотопы" - скачать смотреть  Презентация по Химии "Д.И. Менделеев – основоположник русской агрохимии" - скачать смотреть
Презентация по Химии "Д.И. Менделеев – основоположник русской агрохимии" - скачать смотреть  Кристалічні та аморфні тіла. Рідкі кристали та їх властивості. Підготувала учениця 10 класу Стрельчук Катерина
Кристалічні та аморфні тіла. Рідкі кристали та їх властивості. Підготувала учениця 10 класу Стрельчук Катерина  Полипропилен
Полипропилен