Содержание
- 2. СОз2- + HCl выделение газа CO32-+2H+=CO2+H2O CO32-+Ca2+=CaCO3 CO32-+Ba2+=BaCO3
- 3. Si032- + NH3 *Н2О осадок геля кремниевой кислоты.
- 4. SO32- + HCL SO32-+2H+=SO2+H2O выделение газа + КМп04 + H2SO4 2KMnO4 + 5Na2SO3 + 3H2SO4 →
- 5. SO32- + АgNОз SO32-+2Ag+=Ag2SO3 белый кристаллический осадок, растворимый в избытке реагента. При кипячении полученного раствора -
- 6. SO42- + ВаСl2 белый осадок, нерастворимый в кислотах и щелочах SO42-+Ba2+=BaSO4
- 7. CL- + АgNОз CI-+ Ag+= AgCI осадок белого цвета, растворяется в избытке раствора аммиака.
- 8. Br- + АgNОз Br-+ Ag+= AgCI осадок желтоватого цвета. Плохо растворяется в избытке раствора аммиака. Растворим
- 9. I- + АgNОз I-+ Ag+= AgCI осадок желтого цвета.Не растворяется в избытке раствора аммиака. Растворим в
- 10. I- + КМn04+ H2SO4обесцвечивание раствора 10KI + 2KMnO4 + 8H2SO4 = 2MnSO4 + 6K2SO4 + 5I2
- 11. S2- + КМn04+ H2SO4 обесцвечивание раствора 2KMnO4 + 5H2S + 3H2SO4 → 2MnSO4 + 5S +
- 12. N03- + Си + раствор H2SO4 при нагревании бурый газ, образование зеленовато-голубоватого раствора образование бурого раствора,
- 13. N02- +HCl выделение бурого газа + KI + H2SO4 выделение бурого газа 2NaNO2 + 2NaI +
- 14. N02- +АgNОз бесцветные игольчатые кристаллы, растворимые при нагревании + FeSO4 в слабокислой среде выделение бурового газа,
- 15. Р043- + АgNОз желтый осадок. Количественное осаждение только в нейтральной среде + ВаСl2 белый аморфный осадок,
- 16. Р043- + молибденовая жидкость желтый осадок + ацетат свинца белый осадок + белок нет изменений
- 17. S2O32- + АgNОз белый осадок, растворимый в избытке осадителя + ВаСl2 белый осадок, растворимый в горячей
- 18. S2O32- + H2SO4 выделение желтого осадка и газа + раствор иода обесцвечивание + К2СГ2О7 + H2SO4
- 19. Бораты (в том числе бура) + АgNОз белый осадок АgВО2, при нагревании образующий бурый осадок оксида
- 21. Скачать презентацию


















 Выращивание кристалла медного купороса CuSO4*5Н2О в разных условиях
Выращивание кристалла медного купороса CuSO4*5Н2О в разных условиях Презентация по Химии "Нитраты в овощах" - скачать смотреть
Презентация по Химии "Нитраты в овощах" - скачать смотреть  Химия и производство
Химия и производство Коррозия железа и его сплавов в различных средах
Коррозия железа и его сплавов в различных средах Силикатное производство
Силикатное производство Компоненты, попадающие в продукты питания из минеральных и других удобрений
Компоненты, попадающие в продукты питания из минеральных и других удобрений Гидролиз
Гидролиз Химическое сопротивление пластмасс
Химическое сопротивление пластмасс Презентация для класса Способы получения натрия
Презентация для класса Способы получения натрия  Насыщенные (предельные) углеводороды. Алканы (парафины)
Насыщенные (предельные) углеводороды. Алканы (парафины) Қалдық мөлшерлер. Бромды метил буының концентрациясын анықтау тәсілдемесі
Қалдық мөлшерлер. Бромды метил буының концентрациясын анықтау тәсілдемесі Ароматы, запахи, флюиды
Ароматы, запахи, флюиды Гліцерин (Гліцерол)
Гліцерин (Гліцерол) Забезпечення радіаційної безпеки на АЕС. Оцінка радіаційної обстановки
Забезпечення радіаційної безпеки на АЕС. Оцінка радіаційної обстановки Теплова теорія припинення горіння. Вогнегасні засоби
Теплова теорія припинення горіння. Вогнегасні засоби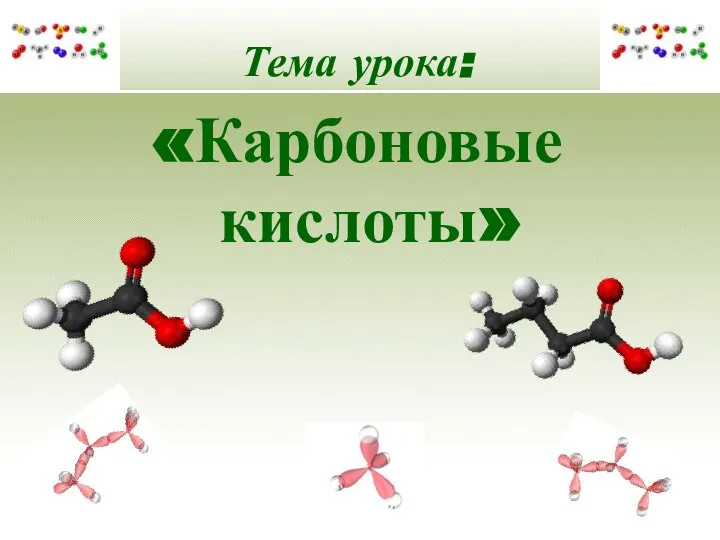 Карбоновые кислоты
Карбоновые кислоты Методы химического анализа. Классификации методов анализа
Методы химического анализа. Классификации методов анализа Презентация по Химии "Липиды" - скачать смотреть
Презентация по Химии "Липиды" - скачать смотреть  Роль розчинiв
Роль розчинiв Изооктан. Получение. Октановое число и степень сжатия
Изооктан. Получение. Октановое число и степень сжатия Dmitri Ivanovich Mendeleev
Dmitri Ivanovich Mendeleev Производные углеводородов с одновалентной функцией
Производные углеводородов с одновалентной функцией Емдік өсімдіктерден жасалған экстракттың химиялық құрамы мен қасиеттері
Емдік өсімдіктерден жасалған экстракттың химиялық құрамы мен қасиеттері Теорія сильних і слабких електролітів. Рівновага в розчинах малорозчинних електролітів
Теорія сильних і слабких електролітів. Рівновага в розчинах малорозчинних електролітів Способы получения полимеров (Лекция 3)
Способы получения полимеров (Лекция 3) ПОРТФОЛІО вчителя хімії та біології Турбівської загальноосвітньої школи І – ІІІ ступенів 2014 рік
ПОРТФОЛІО вчителя хімії та біології Турбівської загальноосвітньої школи І – ІІІ ступенів 2014 рік Комбинированные задачи. 11 класс. Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.
Комбинированные задачи. 11 класс. Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С. 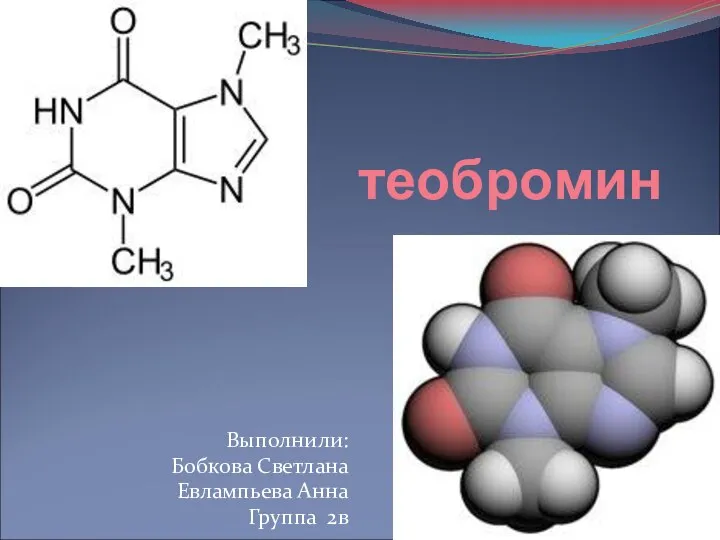 Теобромин
Теобромин