Содержание
- 2. Литература Основная литература 1. Семенова, И. В. Коррозия и защита от коррозии [Текст]: учеб. пособие /
- 3. Литература Методическая литература 1. Лихачев В.А., Горева Т.В. Практикум по курсу «Химическое сопротивление материалов» [Текст]: учеб.
- 4. Тема 1 Коррозия железа и его сплавов в различных средах
- 5. рH 3 6 9 12 Рис. 1.3 Зависимость скорости коррозии железа от рН среды Влияние рН
- 6. Кислотная коррозия Переход в область кислотной коррозии сопровождается существенным увеличением скорости коррозии за счет: 1. растворения
- 7. Кислотная коррозия Слабые кислоты (борная, щавелевая, лимонная) при рН 5-6 достаточно концентрированные и способны растворить пленку
- 8. Влияние вида кислоты на коррозию железа Vкор 1 – НNO3 2- H2SO4 3 - HCl 1
- 9. Коррозия железа в наиболее распространенных кислотах Рассмотрим область низких и средних концентраций (до 37%). Такие кислоты
- 10. Травление сталей в растворах кислот Несмотря на самую высокую скорость коррозии железа в HNO3 и высокую
- 11. Травление сталей в различных кислотах H2SO4 плохо растворяет оксиды, но хорошо травит железо, поэтому травление в
- 12. Коррозия железа в HNO3 Азотная кислота (HNO3): максимальная скорость коррозии при 30% (Семенова 50%); далее пассивация
- 13. Коррозия железа в H2SO4 Максимальная скорость коррозии при концентрации 50-60% (Семенова 47-50%), далее начинает падать. Пассивация
- 14. Коррозия железа в H3РO4 Влияние концентрации кислоты сходно с влиянием ее в H2SO4 Максимальная скорость коррозии
- 15. Коррозия железа в HF До 50% углеродистые и низколегированные стали растворяются очень активно; При более высоких
- 16. Влияние температуры Чем выше температура, тем выше скорость коррозии. Особенно сильно это влияние проявляется в НCl,
- 17. Влияние на коррозию сталей примесей 1000 500 S P Si 0,1N HCl Кm г/м2сутки 0,05 0,1
- 18. Влияние на коррозию стали вида обработки % HCl 0,02 0,08 Кm г/м2сутки 50 100 150 Прокат
- 19. Коррозия в нейтральных средах 1)Fe+ 2e+ H20 Fe(OH)2 + 2H+; Fe(OH)2 Fe(OH)3 2)O2+2H2O+4e 4OH- Вначале смесь
- 20. При наличии в атмосфере газов СО2, Н2S, SO2 в состав продуктов коррозии включаются соли FeSO4, FeCO3,
- 21. Влияние меди на коррозию стали в условиях открытой атмосферы 10Г2С1Д, 10ХСН2Д 09Г2Д, 15ГФ(Д)
- 22. Влияние ионов при подводной коррозии 1.Анионы: СО 3 -2, SO4-3 , SiO3-2 ,Cl- SO4-2 За счёт
- 23. Влияние концентрации соли и вида аниона на скорость коррозии.
- 24. Влияние ионов 2.Катионы: NH4+ -является комплексообразователем, NO3- - может работать как дополнительный окислитель, а иногда пассиватор
- 25. Влияние температуры Скорость коррозии удваивается при изменении температуры на 30оС в открытой системе. Открытая система Закрытая
- 26. Коррозия в щелочах рН 11,5-13 Fe- 2e+ OH- Fe(OH)2 Fe(OH)3 Железо пассивируется, но пассивация идёт не
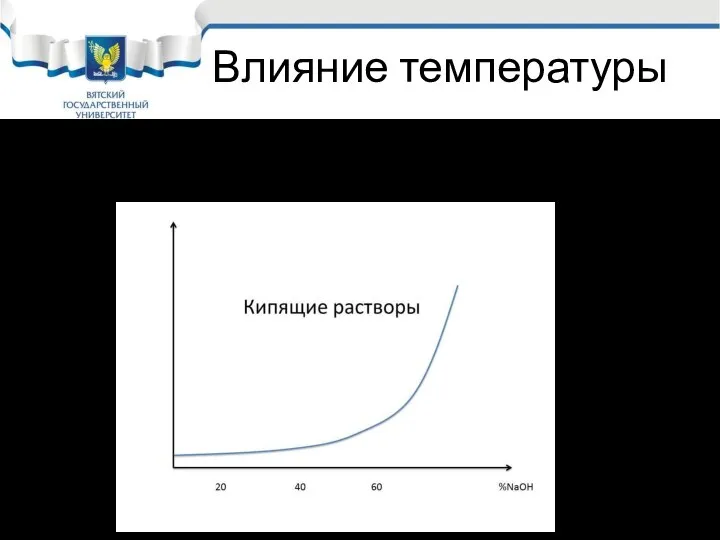
- 27. Влияние температуры Влияние температуры очень велико, особенно опасны кипящие растворы щелочи.
- 28. Наиболее опасными считаются кипящие растворы с концентрацией щелочи более 60%. Но за счёт двух реакций происходит
- 29. Щелочное коррозионное растрескивание Особенностью коррозии в концентрированных щелочах является появление в них коррозионного растрескивания под напряжением
- 30. Виды нержавеющих сталей Коррозионностойкие (нержавеющие) стали и сплавы делят на 5 групп: 1. Стали для слабоагрессивных
- 31. Вторая группа коррозионностойких (нержавеющих) сталей применяется в солевых средах при невысоких температурах, в частности при морской
- 32. Под средами со средней коррозионной агрессивностью понимают растворы солей при разных температурах, а также слабые растворы
- 33. Стали для применения в средах с повышенной коррозионной агрессивностью Эти стали разрабатывались с целью повышения химического
- 35. Скачать презентацию































 Спирти та їх види
Спирти та їх види Подготовка к ГИА. Тренажер по химии
Подготовка к ГИА. Тренажер по химии Жесткость воды и способы ее устранения
Жесткость воды и способы ее устранения Презентация СПЛАВЫ МЕТАЛЛОВ
Презентация СПЛАВЫ МЕТАЛЛОВ  Отрицательное влияние азотных минеральных удобрений на почву
Отрицательное влияние азотных минеральных удобрений на почву Катализ органических реакций. (Лекция 15)
Катализ органических реакций. (Лекция 15) Термический анализ
Термический анализ Физическая и коллоидная химия
Физическая и коллоидная химия Технический контроль химических соединений в производстве каустика
Технический контроль химических соединений в производстве каустика Углеводороды. Алкены
Углеводороды. Алкены Продукты переработки жиров. Жироподобные вещества. Заменители жиров в косметическом производстве
Продукты переработки жиров. Жироподобные вещества. Заменители жиров в косметическом производстве Вакуумное фильтрование
Вакуумное фильтрование Введение в хемоинформатику
Введение в хемоинформатику Кремнийорганикалық қосылыстар
Кремнийорганикалық қосылыстар Контроль в процессе обучения химии на старшей ступени школы
Контроль в процессе обучения химии на старшей ступени школы Составление электронных формул и электронно-графических схем строения атома
Составление электронных формул и электронно-графических схем строения атома Урок повторения по химии за курс 8 класса
Урок повторения по химии за курс 8 класса Азотная кислота
Азотная кислота Анилин. Строение. Физические и химические свойства
Анилин. Строение. Физические и химические свойства Композиционные материалы, состав и классификация композиционных материалов
Композиционные материалы, состав и классификация композиционных материалов Простые вещества – металлы. Общие физические свойства металлов.
Простые вещества – металлы. Общие физические свойства металлов. Распространение ПВО в приземном слое атмосферы
Распространение ПВО в приземном слое атмосферы Строение атома. (Лекция 2-3)
Строение атома. (Лекция 2-3) Типы кристаллических решеток. Вещества молекулярного и немолекулярного строения
Типы кристаллических решеток. Вещества молекулярного и немолекулярного строения Веселый химический КВН
Веселый химический КВН Соли
Соли Горные породы
Горные породы Леция 1. Природа сил взаимодействия. Методы исследования комплексообразования:
Леция 1. Природа сил взаимодействия. Методы исследования комплексообразования: