Содержание
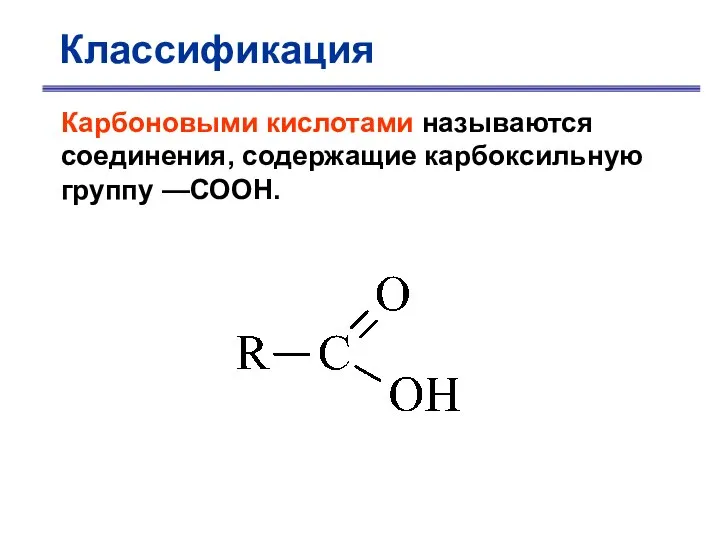
- 2. Классификация Карбоновыми кислотами называются соединения, содержащие карбоксильную группу —СООН.
- 3. 1. По числу карбоксильных групп : моно- , дикарбоновые кислоты и т.д. 2. В зависимости от
- 4. МОНОКАРБОНОВЫЕ КИСЛОТЫ
- 5. ПОВТОРИТЬ!
- 6. ХИМИЧЕСКИЕ СВОЙСТВА
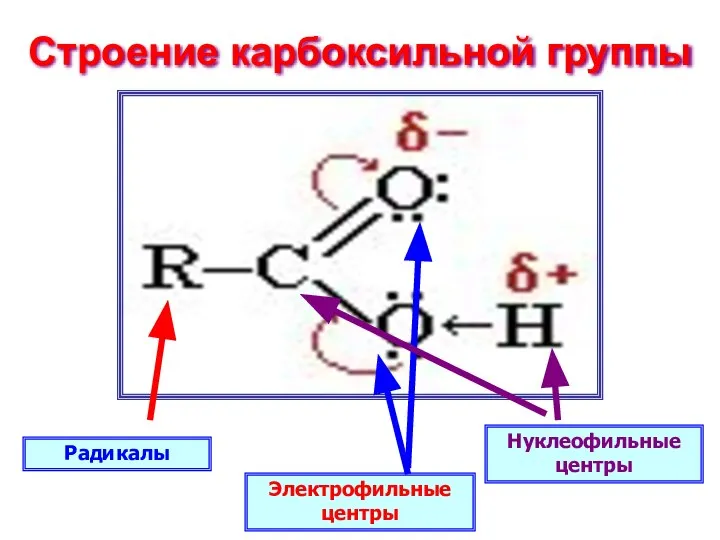
- 7. Строение карбоксильной группы Радикалы Нуклеофильные центры Электрофильные центры
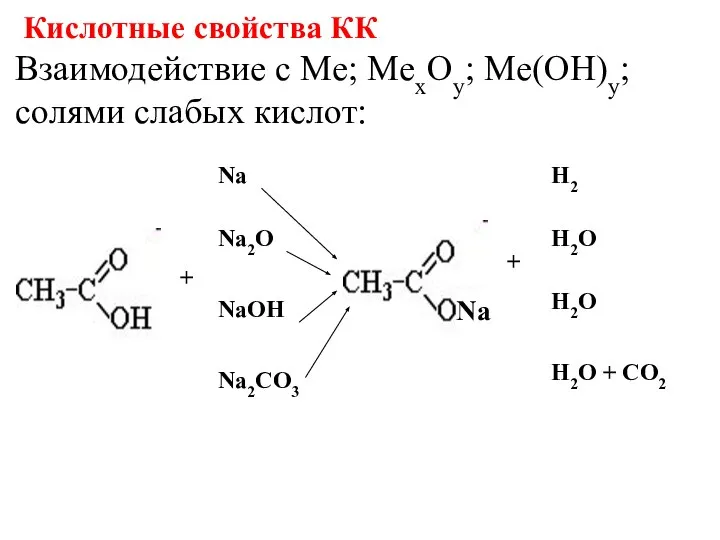
- 9. Взаимодействие с Me; MeхOy; Me(OH)y; солями слабых кислот: Кислотные свойства КК
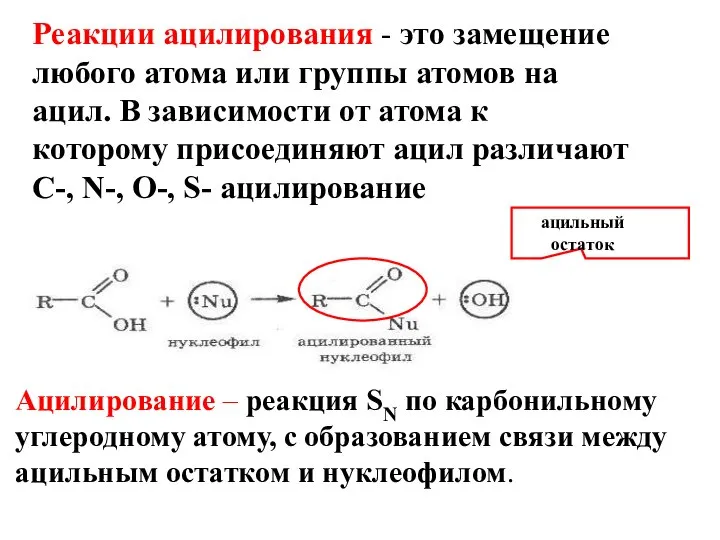
- 10. Реакции ацилирования - это замещение любого атома или группы атомов на ацил. В зависимости от атома
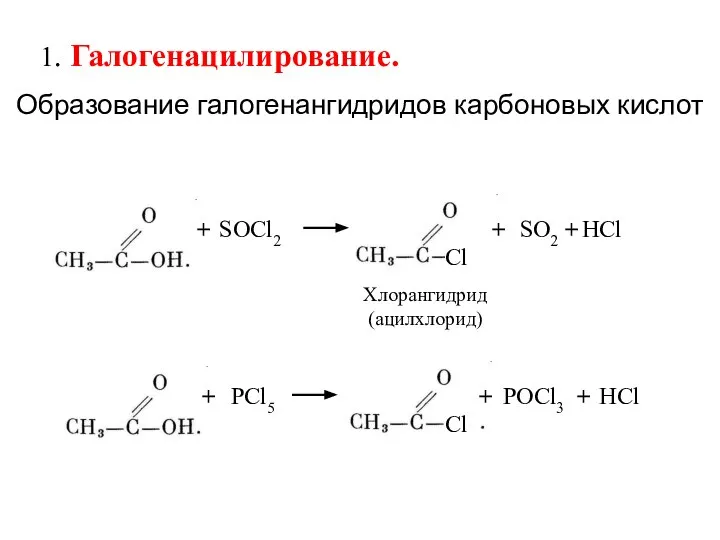
- 11. 1. Галогенацилирование. Образование галогенангидридов карбоновых кислот
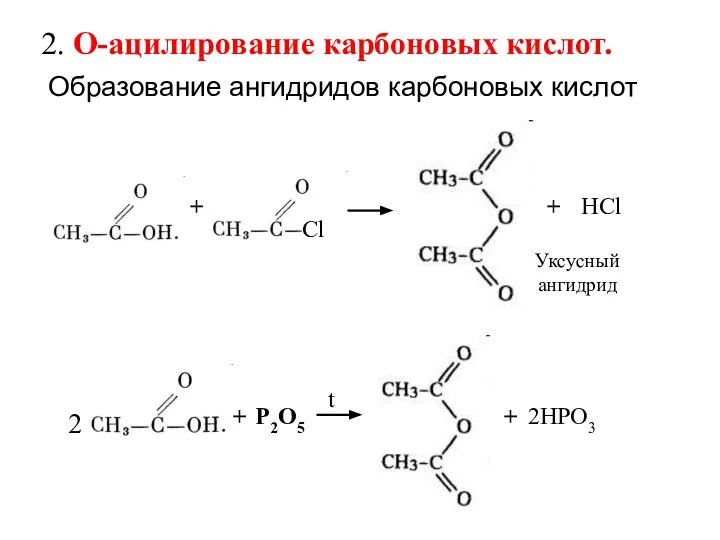
- 12. 2. О-ацилирование карбоновых кислот. Образование ангидридов карбоновых кислот
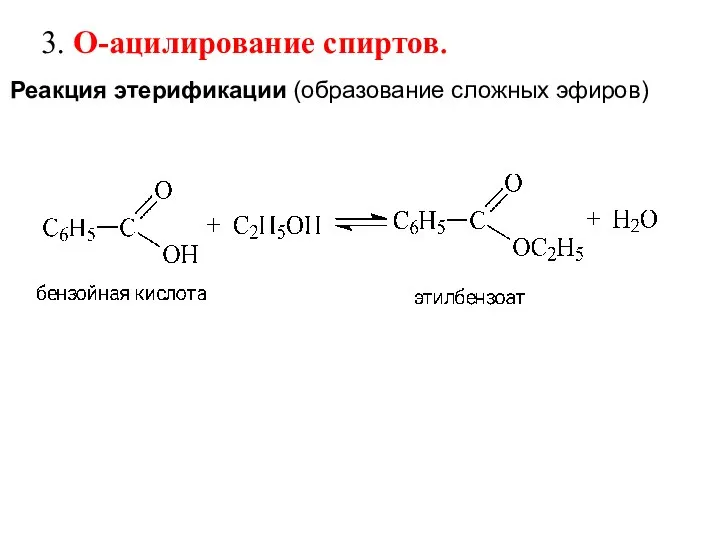
- 13. Реакция этерификации (образование сложных эфиров) 3. О-ацилирование спиртов.
- 14. Образование амидов карбоновых кислот 4. N-ацилирование аминов. Реакция образования амидов играет большую роль в организме: за
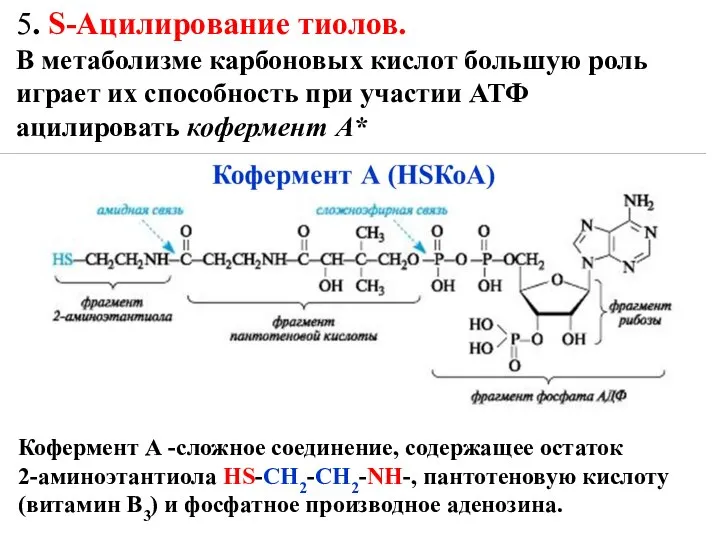
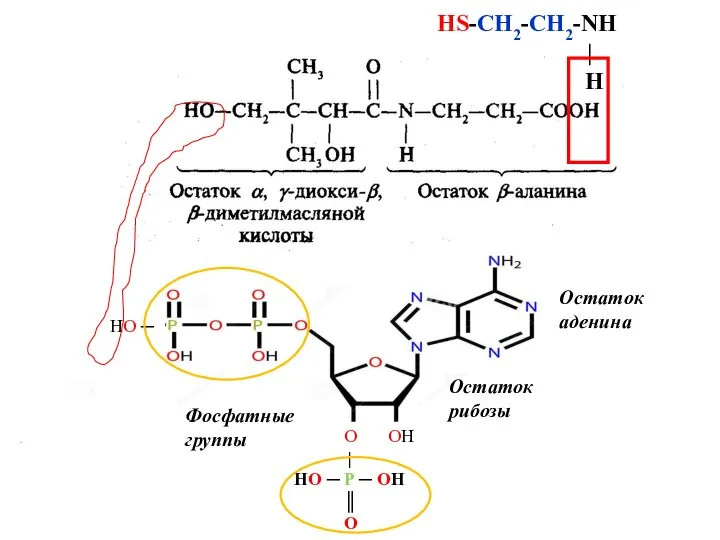
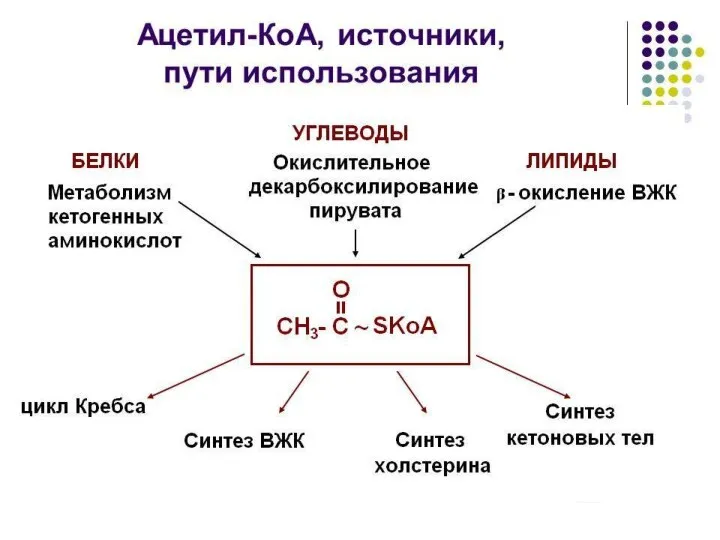
- 15. 5. S-Ацилирование тиолов. В метаболизме карбоновых кислот большую роль играет их способность при участии АТФ ацилировать
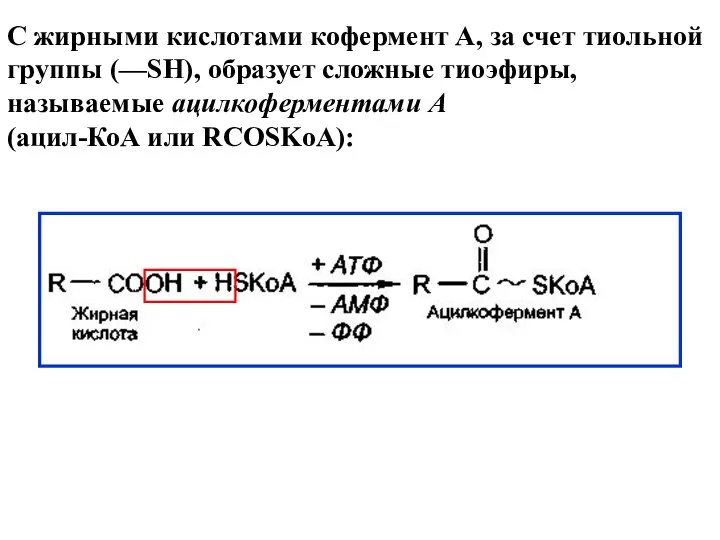
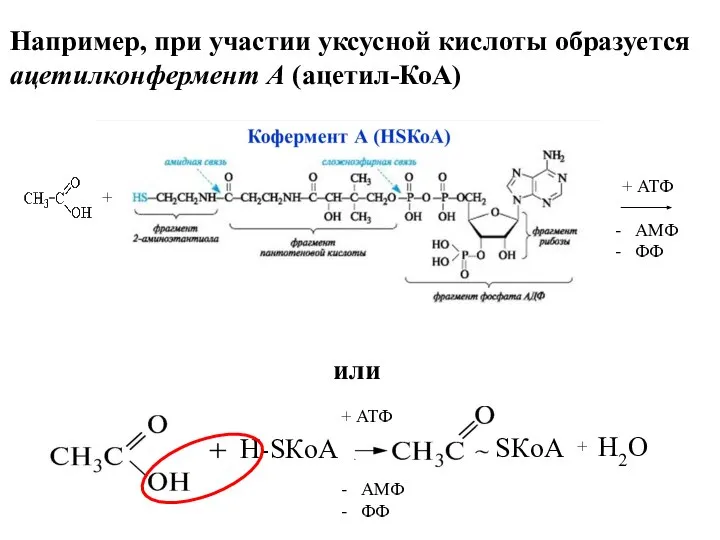
- 17. С жирными кислотами кофермент А, за счет тиольной группы (—SH), образует сложные тиоэфиры, называемые ацилкоферментами А
- 19. Например, при участии уксусной кислоты образуется ацетилконфермент А (ацетил-КоА) или
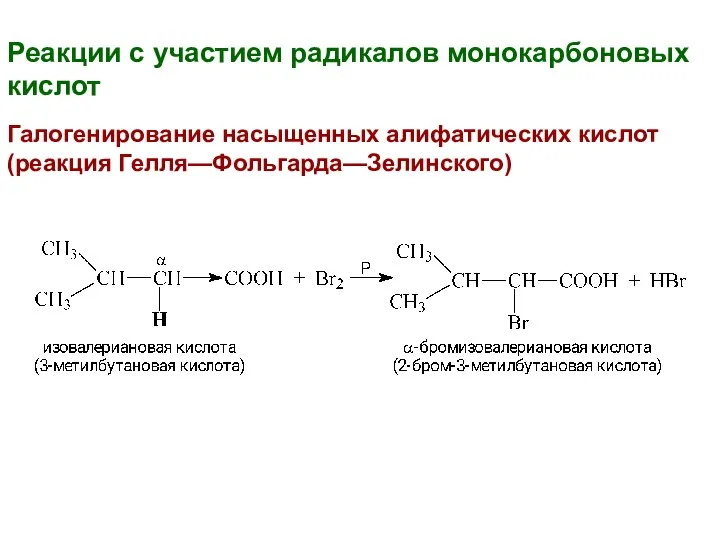
- 21. Реакции с участием радикалов монокарбоновых кислот Галогенирование насыщенных алифатических кислот (реакция Гелля—Фольгарда—Зелинского)
- 22. ДИКАРБОНОВЫЕ КИСЛОТЫ
- 23. В живом мире наибольшее значение имеют: Диссоциируют ступенчато. Сила уменьшается Кислотные свойства значительно выше, чем монокарбоновых,
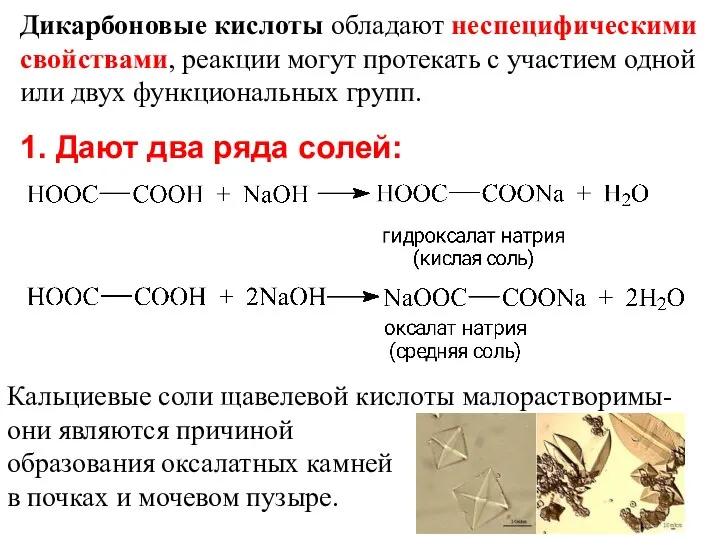
- 24. 1. Дают два ряда солей: Дикарбоновые кислоты обладают неспецифическими свойствами, реакции могут протекать с участием одной
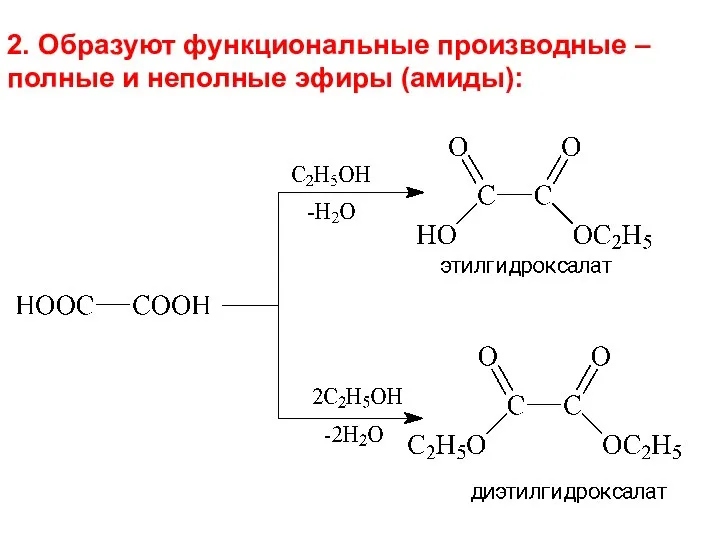
- 25. 2. Образуют функциональные производные – полные и неполные эфиры (амиды):
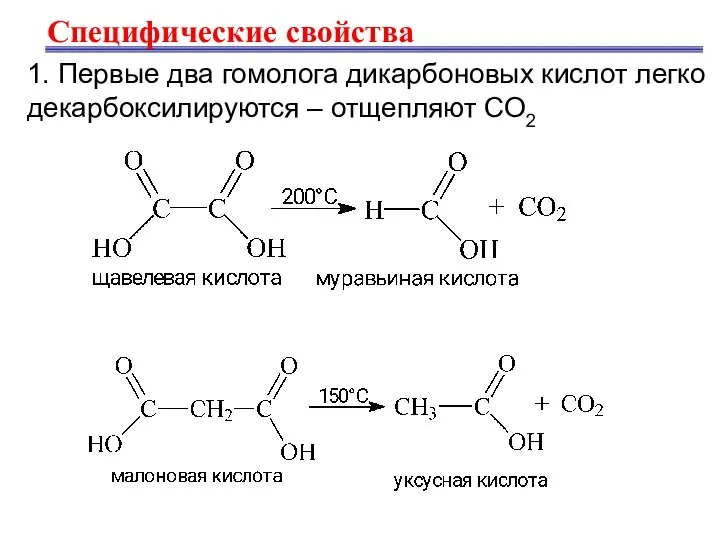
- 26. Специфические свойства 1. Первые два гомолога дикарбоновых кислот легко декарбоксилируются – отщепляют СО2
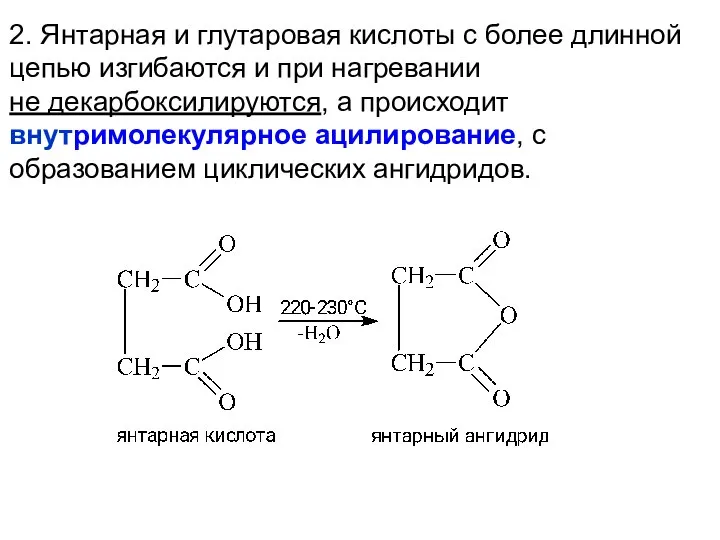
- 27. 2. Янтарная и глутаровая кислоты с более длинной цепью изгибаются и при нагревании не декарбоксилируются, а
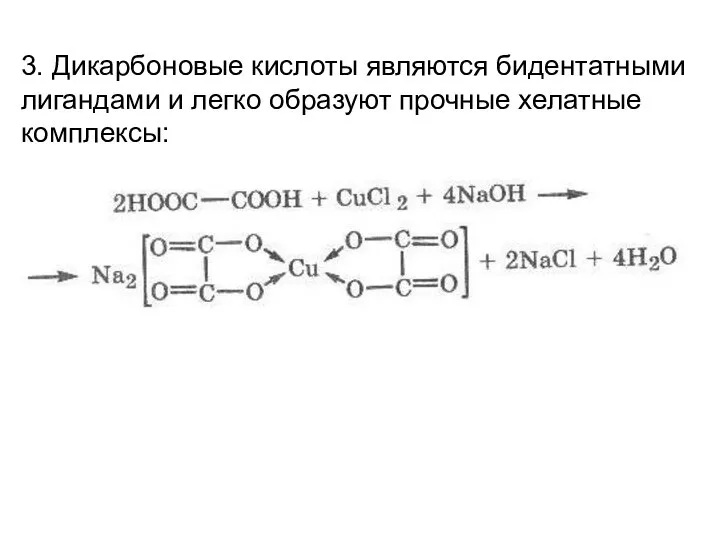
- 28. 3. Дикарбоновые кислоты являются бидентатными лигандами и легко образуют прочные хелатные комплексы:
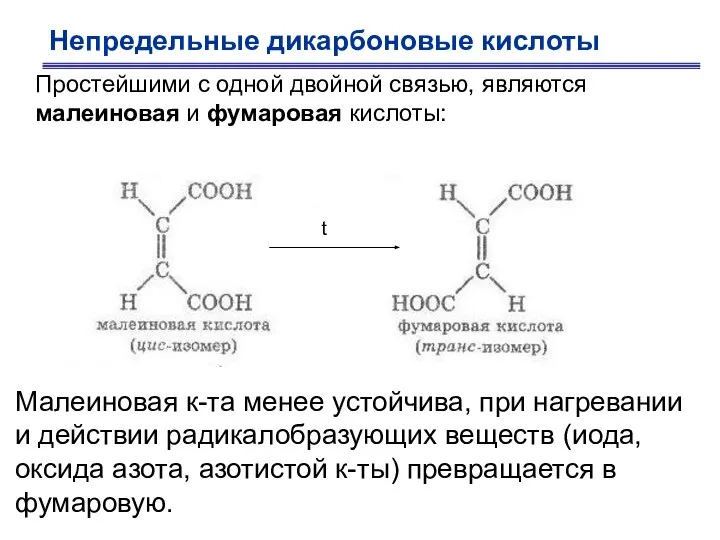
- 29. Непредельные дикарбоновые кислоты Простейшими с одной двойной связью, являются малеиновая и фумаровая кислоты: Малеиновая к-та менее
- 31. Скачать презентацию






 Алканы. Циклоалканы
Алканы. Циклоалканы Стелс-материалы
Стелс-материалы Мыс айналымы
Мыс айналымы Биосинтез инвертазы при ферментации гидролизата помола зерна ржи штаммом Aspergillus niger Л-4
Биосинтез инвертазы при ферментации гидролизата помола зерна ржи штаммом Aspergillus niger Л-4 Теоретические основы неорганического синтеза
Теоретические основы неорганического синтеза Chemical bonds
Chemical bonds Ферменты 3. Медицинская энзимология. (Лекция 3)
Ферменты 3. Медицинская энзимология. (Лекция 3) Чистые вещества и смеси. Способы разделения смесей. Загадка
Чистые вещества и смеси. Способы разделения смесей. Загадка Сульфиты. Сульфаты. Кислотные дожди
Сульфиты. Сульфаты. Кислотные дожди Презентация по Химии "Этот многоликий Кальцит" - скачать смотреть
Презентация по Химии "Этот многоликий Кальцит" - скачать смотреть  Металлы побочных подгрупп. Марганец. Хром. (Лекция 15)
Металлы побочных подгрупп. Марганец. Хром. (Лекция 15) Редкие химические элементы
Редкие химические элементы Анаболические стероиды
Анаболические стероиды Физико-химические методы исследования биополимеров: Структурная формула соединения
Физико-химические методы исследования биополимеров: Структурная формула соединения Спекание порошковых систем
Спекание порошковых систем Характеристика элемента по его положению в периодической системе химических элементов Д.И.Менделеева
Характеристика элемента по его положению в периодической системе химических элементов Д.И.Менделеева ПРЕЗЕНТАЦИЯ по биологии на тему: «Гормоны и механизм их реализации» Подготовил: ученик лицея №1580 класса 11-4А Попов Алексей Уч
ПРЕЗЕНТАЦИЯ по биологии на тему: «Гормоны и механизм их реализации» Подготовил: ученик лицея №1580 класса 11-4А Попов Алексей Уч КРИСТАЛЛЫ Проект выполнил: Худин Вячеслав ученик 2 «В» класса МОУ «Лицей № 26» Московской области Г. Подольска
КРИСТАЛЛЫ Проект выполнил: Худин Вячеслав ученик 2 «В» класса МОУ «Лицей № 26» Московской области Г. Подольска Взрывчатые вещества. Пероксид ацетона и пикриновая кислота
Взрывчатые вещества. Пероксид ацетона и пикриновая кислота Презентация по Химии "Краткий очерк истории развития химии." - скачать смотреть бесплатно
Презентация по Химии "Краткий очерк истории развития химии." - скачать смотреть бесплатно Презентация по Химии "Колообіг Оксигену, Нітрогену, Карбону в природі" - скачать смотреть бесплатно
Презентация по Химии "Колообіг Оксигену, Нітрогену, Карбону в природі" - скачать смотреть бесплатно Предельные углеводороды
Предельные углеводороды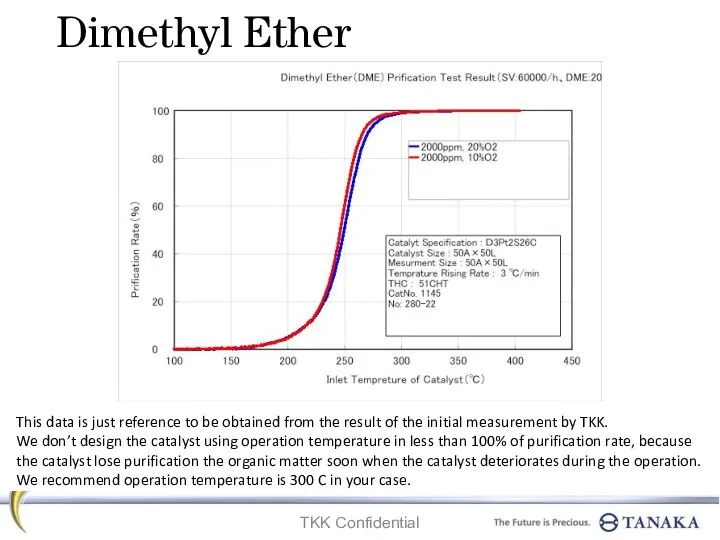 Dimethyl ether. Prification test result
Dimethyl ether. Prification test result Основные законы химии
Основные законы химии Правила безпечного використання засобів побутової хімії.
Правила безпечного використання засобів побутової хімії.  Аренкарбонільні комплекси металів у реакціях перфлюороалкілювання та деароматизації
Аренкарбонільні комплекси металів у реакціях перфлюороалкілювання та деароматизації Битумы и материалы на основе битумов
Битумы и материалы на основе битумов Расчет необходимого объема удобрения для внесения
Расчет необходимого объема удобрения для внесения