Содержание
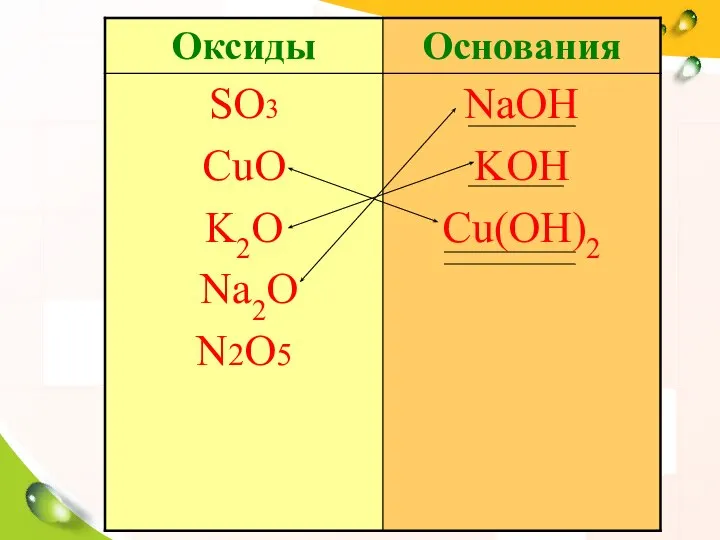
- 2. Распределите эти формулы по классам в таблицу SO3 , HCl,CuO,H2SO4, NaOH, K2O, N2O5, Na2 o, KOH,
- 4. Кислоты — это сложные вещества, состоящие из атомов водорода и кислотного остатка.
- 5. Название кислот: HCI H2SO4 H3PO4 HNO3 H2S НNO2 H 2SO3 H2CO3 Н2SiO4 Соляная кислота Серная кислота
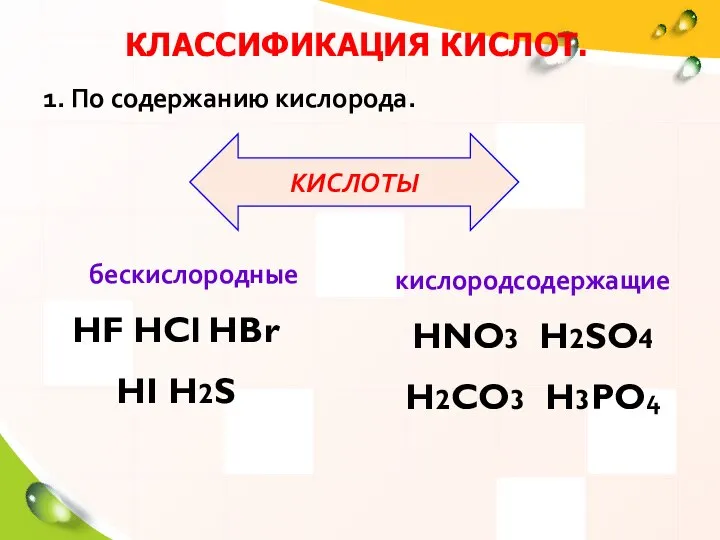
- 6. КЛАССИФИКАЦИЯ КИСЛОТ. бескислородные HF HCl HBr HI H2S 1. По содержанию кислорода. кислородсодержащие HNO3 H2SO4 H2CO3
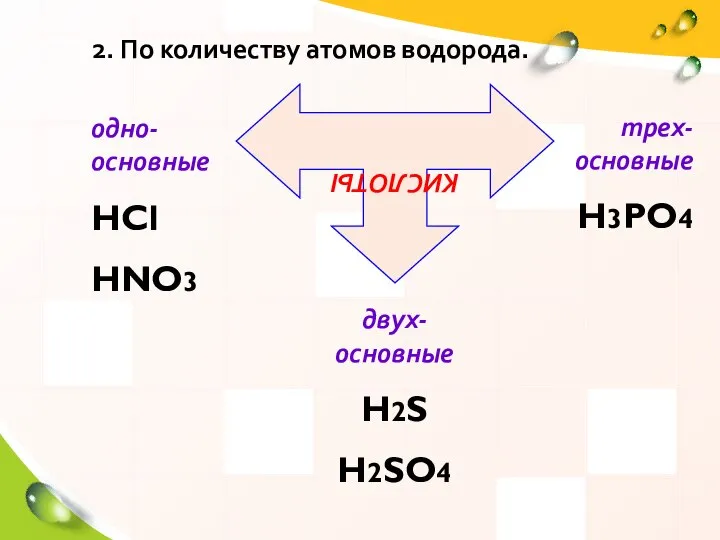
- 7. 2. По количеству атомов водорода. КИСЛОТЫ одно-основные HCl HNO3 двух-основные H2S H2SO4 трех-основные H3PO4
- 8. Физические свойства кислот При обычных условиях кислоты могут быть твердыми и жидкими. Кислоты –едкие жидкости (кроме
- 9. Кислый вкус лимону придает лимонная кислота, яблоку — яблочная кислота, скисшему молоку — молочная кислота. Щавель
- 10. ПРАВИЛА БЕЗОПАСНОСТИ Едкое вещество—кислота! Разрушает и раздражает кожу, слизистые оболочки. Попавшие на кожу капли раствора кислоты
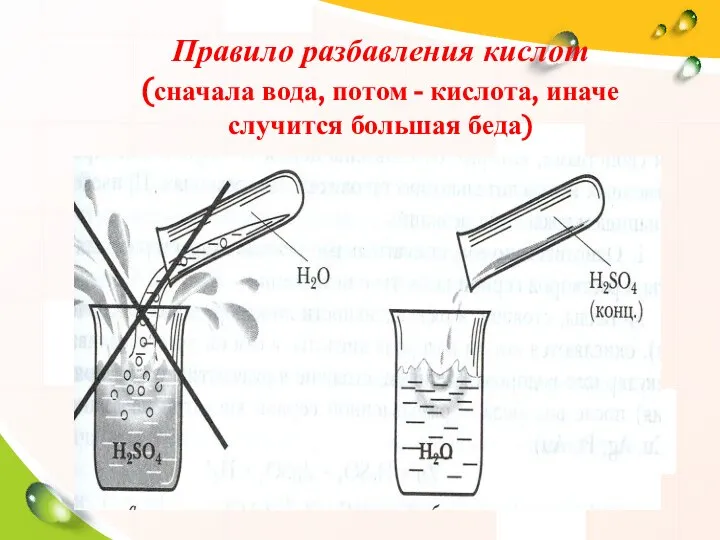
- 11. Правило разбавления кислот (сначала вода, потом - кислота, иначе случится большая беда)
- 12. Взаимодействие с индикаторами Помни! Нерастворимые кислоты не меняют окраску индикаторов.
- 14. Скачать презентацию







 Тесты по неорганической химии
Тесты по неорганической химии Автор презентации: Короткова Екатерина Викторовна, учитель биологии и химии МОУ «Горютинская СОШ» Биология 9 класс
Автор презентации: Короткова Екатерина Викторовна, учитель биологии и химии МОУ «Горютинская СОШ» Биология 9 класс Классификация химических реакций Маланина Елена Алексеевна Учитель химии МОУ Большевяземская гимназия, р.п. Большие Вяземы,
Классификация химических реакций Маланина Елена Алексеевна Учитель химии МОУ Большевяземская гимназия, р.п. Большие Вяземы,  Карбоновые кислоты
Карбоновые кислоты Сверхразветвленные полимеры: типы, получение, применение
Сверхразветвленные полимеры: типы, получение, применение Хлоропласты. Митохондрии
Хлоропласты. Митохондрии V група періодичної системи Менделєєва
V група періодичної системи Менделєєва Расчетная ячейка при МД моделировании. Граничные условия. Элементарная ячейка для атомов аргона
Расчетная ячейка при МД моделировании. Граничные условия. Элементарная ячейка для атомов аргона Состояние электронов в атоме
Состояние электронов в атоме Значение воды. Роль водного фактора в формировании здоровья населения
Значение воды. Роль водного фактора в формировании здоровья населения Презентация по Химии "Кристалл душы" - скачать смотреть
Презентация по Химии "Кристалл душы" - скачать смотреть  Презентация по Химии "Фосфор" - скачать смотреть бесплатно_
Презентация по Химии "Фосфор" - скачать смотреть бесплатно_ Кальций(Ca)
Кальций(Ca) Нафта, вугілля, природний газ як вуглеводнева сировина Підготувала учениця 11 класу Дерев’янко Ірина
Нафта, вугілля, природний газ як вуглеводнева сировина Підготувала учениця 11 класу Дерев’янко Ірина  Информационные технологии в обучении химии
Информационные технологии в обучении химии Углеводы
Углеводы Тема : Спирты Презентация по химии Ученицы 11 «Б» класса ЗОШ №41 Зануды Татьяны
Тема : Спирты Презентация по химии Ученицы 11 «Б» класса ЗОШ №41 Зануды Татьяны  Факторы, влияющие на скорость химической реакции
Факторы, влияющие на скорость химической реакции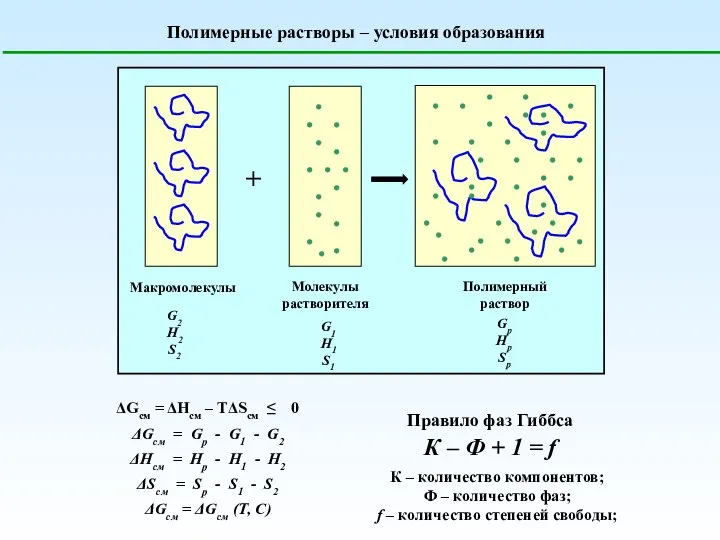 Полимерные растворы – условия образования
Полимерные растворы – условия образования Коррозия металлов
Коррозия металлов «ШАРИКИ СЧАСТЬЯ» Неустроева Светлана Габдульхатовна, учитель I категории, МБОУ «СОШ №31», г.Нижнекамск
«ШАРИКИ СЧАСТЬЯ» Неустроева Светлана Габдульхатовна, учитель I категории, МБОУ «СОШ №31», г.Нижнекамск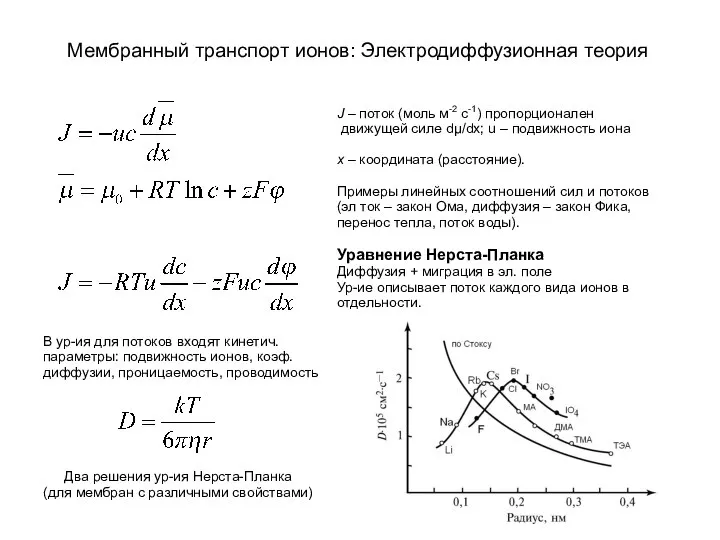 Мембранный транспорт ионов: электродиффузионная теория
Мембранный транспорт ионов: электродиффузионная теория Химико-фармацевтические препараты
Химико-фармацевтические препараты Презентация по химии Олигосахариды ПОЛИСАХАРИДЫ.
Презентация по химии Олигосахариды ПОЛИСАХАРИДЫ. 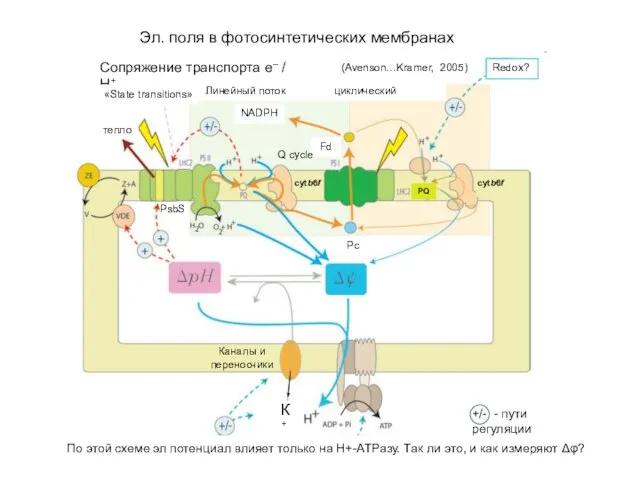 Электрические поля в фотосинтетических мембранах
Электрические поля в фотосинтетических мембранах Введение в термические процессы вторичной переработки нефти
Введение в термические процессы вторичной переработки нефти Закономірності протікання хімічних реакцій
Закономірності протікання хімічних реакцій Термореактивные и термопластичные пластмассы
Термореактивные и термопластичные пластмассы