Содержание
- 2. План Енергетика хімічних реакцій. Загальні поняття І- закон термодинаміки. Ентальпія. Закон Гесса і наслідки з закону.
- 3. Тепловий ефект хімічної реакції – Q – це кількість теплоти , що виділяється або поглинається під
- 4. Види систем Відкриті Закриті Ізольовані Гомогенні Гетерогенні Ізобарні Ізохорні Ізотермічні Система – це будь-яка обмежена яким-небудь
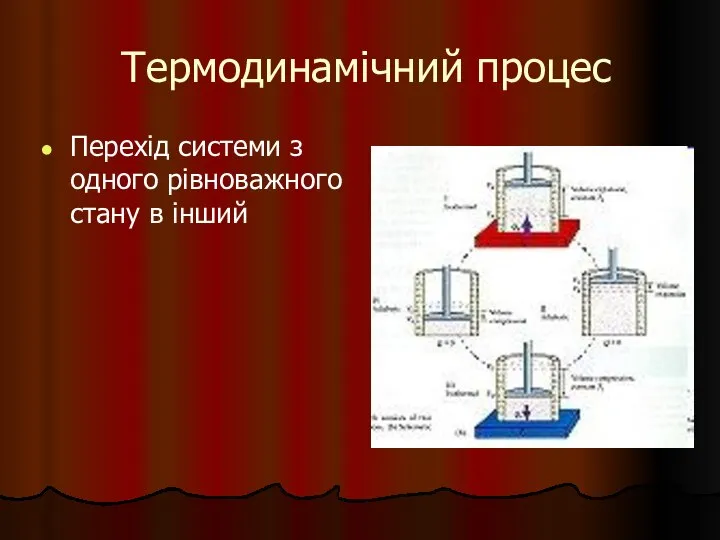
- 5. Термодинамічний процес Перехід системи з одного рівноважного стану в інший
- 6. Параметри систем Параметри – це показники, що характеризують стан системи: температура, тиск, об'єм, густина та ін.
- 7. Функції стану системи Внутрішня енергія системи (U)– це загальний запас енергії системи, що складається з енергії
- 8. Ізохорні системи (V = const, A=0) екзотермічна реакція(+Q) ∆U = U2-U1 ∆U ендотермічна реакція (-Q) ∆U
- 9. ЕНТАЛЬПІЯ U + P∙ V = H – ентальпія – тепловмість системи Q = - ΔH
- 10. Ізобарні системи (Р = const, A≠0) Перший закон термодинаміки (1847 Г.Гельмгольц) Теплота, яку отримує система витрачається
- 11. Закони термохімії Закон Лавуазьє-Лапласа: Ентальпія утворення даної сполуки чисельно дорівнює ентальпії її розкладання з протилежним знаком.
- 12. Закон Гесса Тепловий ефект залежить тільки від стану вихідних і кінцевих продуктів, і не залежить від
- 13. Наслідки з закону Гесса ΔHх.р. = ∑ nΔHутв. продуктів - ∑nΔHутв. поч. речовин 2 H2S +
- 14. Залежність теплового ефекту від температури Теплоємність (середня) системи дорівнює кількості теплоти, яку необхідно підвести або відвести
- 15. Залежність теплоємності від температури При сталому тиску теплота отримана системою йде на зміну ентальпії CP=ΔH/ΔT СP=
- 16. Залежність Кірхгофа інтегрування рівняння теплоємності від Т1 до Т2 отримаємо залежність ентальпії від температури (Залежність Кірхгофа)
- 17. Принцип Бертло (1867р.): принцип самочинного перебігу хімічних реакцій: Самочинно протікають лише ті процеси, що супроводжуються виділенням
- 18. Термодинамічна імовірність W Кількість мікростанів, з яких складається макроскопічний стан системи, називається термодинамічною імовірністю W. Термодинамічна
- 19. Ентропія (S Дж/моль⋅К) При фазових переходах типу: т - р (плавлення), р - г (випар), S
- 20. Ентропія (S Дж/моль⋅К) Кількісною мірою ймовірності стану, невпорядкованості, безладдя – є ентропія S. S = klnW,
- 21. ІІ – закон термодинаміки (1850 Р.Клаузиус ) Будь-яка ізольована система представлена сама собі змінюється в напрямку
- 22. Енергія Гіббса
- 23. Енергія Гіббса а) – оборотний процес; б) необоротний процес
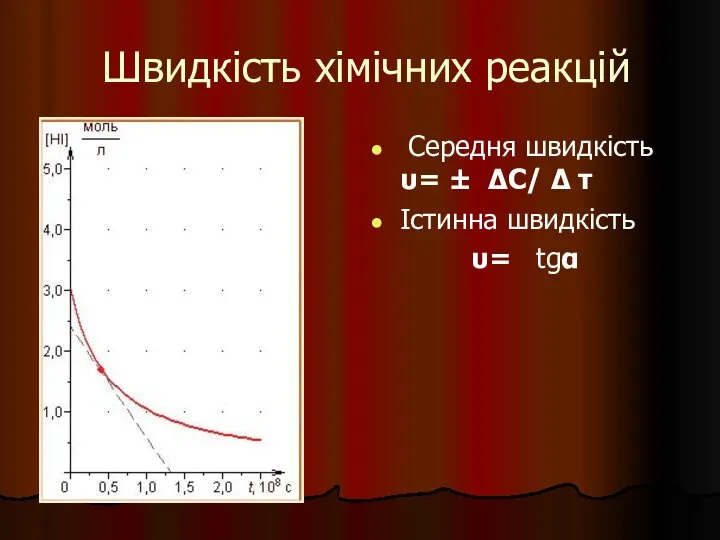
- 24. Швидкість хімічних реакцій Середня швидкість υ= ± ΔC/ Δ τ Істинна швидкість υ= tgα
- 25. Закон діючих мас (Гульдберг і Вааге, 1867р.) При постійній температурі швидкість хімічної реакції пропорційна добутку концентрацій
- 26. Залежність швидкості реакції від температури правило Вант-Гоффа швидкість збільшується приблизно в 2÷4 рази при підвищенні температури
- 27. Енергія активації Еа Енергія, яка дорівнює різниці між середньою енергією молекул системи і енергією, необхідною для
- 28. Рівняння Арреніуса Залежність швидкості реакції від температури й енергії активації визначається рівнянням Арреніуса: де, А –
- 29. Каталіз Каталіз – це прискорення хімічної реакції речовиною каталізатором. Каталізатор – речовина, що прискорює хімічні реакції,
- 30. Рівновага Стан системи коли швидкість прямої та зворотної реакції однакові і не змінюються називається хімічною рівновагою
- 31. Константа хімічної рівноваги Реакція відбувається за рівнянням: А + В ⇔ D + E υпрям =
- 32. Зміщення рівноваги Принцип Ле-Шательє: Якщо на систему, що знаходиться в стані рівноваги подіяти зовнішнім фактором, то
- 33. Каталізатор Каталізатор – речовина, що прискорює хімічні реакції, але сам якісно і кількісно не змінюється Механізм
- 34. Ферменти (ензими) В 1902 р. в лабораторії І. П. Павлова були одержані докази білкової природи ферменту
- 35. Склад ферментів Білкова частина – апофермент; Небілкова частина – кофактор може мати неорганічну природу, наприклад Fe2+,
- 36. Ферменти - це глобулярні білки, значних розмірів, що значно перевищують речовину, яку перетворюють (субстрат). Основна ділянка
- 37. Каталітичну активність компоненти ферменту проявляють не поокремо, а лише в об’єднаній структурі, яка називається холоферментом
- 39. Скачать презентацию

































 Количество вещества
Количество вещества Драгоценные камни
Драгоценные камни Гетерофункциональные соединения, участвующие в процессах жизнедеятельности
Гетерофункциональные соединения, участвующие в процессах жизнедеятельности Классификация химических элементтов
Классификация химических элементтов Кристаллы и правильные многогранники. 11 класс
Кристаллы и правильные многогранники. 11 класс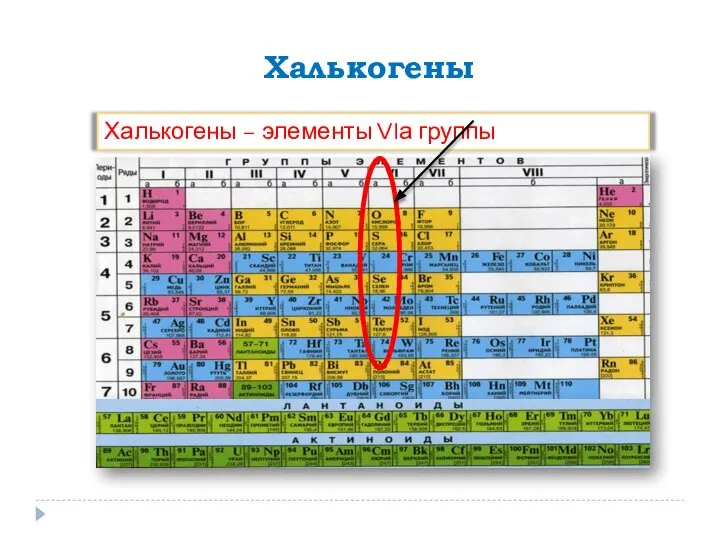 Кислород. Сера
Кислород. Сера Тема урока: «Химический элемент - водород» Подготовила: Михно Валерия 9 «В» класс Учитель: Назаренко Любовь Дмитриевна
Тема урока: «Химический элемент - водород» Подготовила: Михно Валерия 9 «В» класс Учитель: Назаренко Любовь Дмитриевна  Генетика клеточного цикла. Надклеточный контроль клеточного деления, роста и апоптоза. (Глава 5)
Генетика клеточного цикла. Надклеточный контроль клеточного деления, роста и апоптоза. (Глава 5) Амоніак
Амоніак  Atmospheric chemistry
Atmospheric chemistry Презентация по Химии "Презентация Металлы в организме человека" - скачать смотреть
Презентация по Химии "Презентация Металлы в организме человека" - скачать смотреть  ЩЕЛОЧНЫЕ МЕТАЛЛЫ Выполнили: Патренкина Наталия, Иванова Кристина, ученицы 9«А» класса СОШ №6 Руководитель: Овсяникова Мар
ЩЕЛОЧНЫЕ МЕТАЛЛЫ Выполнили: Патренкина Наталия, Иванова Кристина, ученицы 9«А» класса СОШ №6 Руководитель: Овсяникова Мар Дисциплина: Химия. Лекция 1. Растворы
Дисциплина: Химия. Лекция 1. Растворы Общие пути обмена аминокислот. (Лекция 11)
Общие пути обмена аминокислот. (Лекция 11) Коллоидные растворы
Коллоидные растворы Введение. Предмет и содержание фармацевтической химии, её связи с другими науками
Введение. Предмет и содержание фармацевтической химии, её связи с другими науками Ионная химическая связь
Ионная химическая связь Углеводы: моносахариды, олиго- и полисахариды
Углеводы: моносахариды, олиго- и полисахариды Основи процесів горіння. Полум’я. Процеси, що відбуваються у полум’ї. (Розділ 1.1.2)
Основи процесів горіння. Полум’я. Процеси, що відбуваються у полум’ї. (Розділ 1.1.2) Металлы: общая характеристика
Металлы: общая характеристика Итоговая консультация. Формульный диктант
Итоговая консультация. Формульный диктант Металлы и их активность
Металлы и их активность Химиялық элемент алюминий
Химиялық элемент алюминий Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки
Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки Ориентационная вытяжка полимеров
Ориентационная вытяжка полимеров Применение алканов Работа Гончаровой Натальи Ученицы 11 «А» класса Учитель: Попова И.В.
Применение алканов Работа Гончаровой Натальи Ученицы 11 «А» класса Учитель: Попова И.В. Углеводы. Моносахариды, олигосахариды (дисахариды)
Углеводы. Моносахариды, олигосахариды (дисахариды) Сера. Строение атома, аллотропия, свойства и применение серы
Сера. Строение атома, аллотропия, свойства и применение серы