Классификация дисперсных систем. Коллигативные свойства растворов. Растворимость газов в воде. Термодинамика
Содержание
- 2. Химия в медицинском вузе — фундаментальная общетеоретическая естественно-научная дисциплина Задача химии – заложить физико-химическую основу и
- 3. химия РОССИЙСКИЙ НАЦИОНАЛЬНЫЙ ИССЛЕДОВАТЕЛЬСКИЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ им. Н.И.ПИРОГОВА Лекция 1 Классификация дисперсных систем Коллигативные свойства растворов
- 4. 1. Классификация дисперсных систем Дисперсность (раздробленность) — степень измельчения вещества. Дисперсная фаза — часть системы, которая
- 5. Нанодисперсные системы (коллоидные дисперсные системы, ультрамикрогетерогенные системы, золи) — размеры частиц дисперсной фазы от 1 до
- 6. г) По агрегатному состоянию: д) По взаимодействию между дисперсной фазой и дисперсионной средой: Лиофильные (гидрофильные) системы
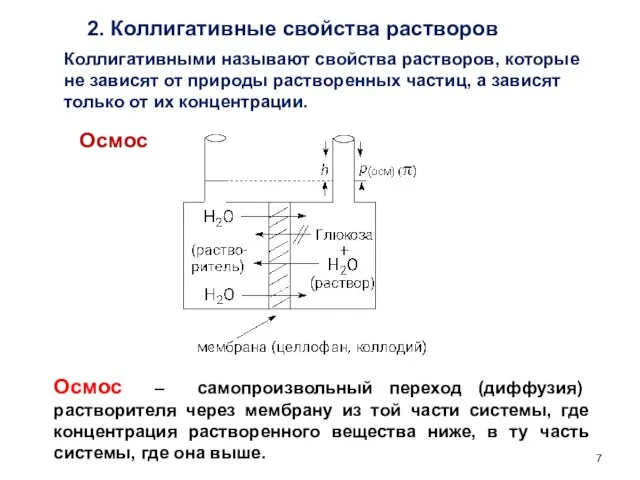
- 7. 2. Коллигативные свойства растворов Коллигативными называют свойства растворов, которые не зависят от природы растворенных частиц, а
- 8. Осмотическое давление раствора (π ) – давление, которое нужно приложить к раствору, чтобы предотвратить проникновение в
- 9. Для раствора, содержащего несколько растворенных веществ: Осмолярность (осмомолярность) — суммарная концентрация кинетически независимых частиц в растворе
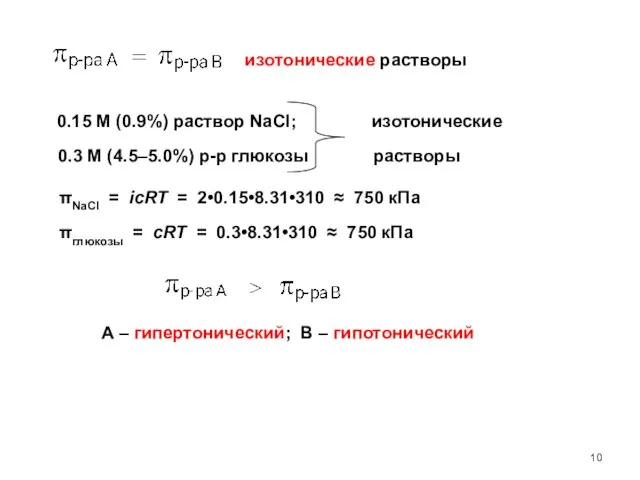
- 10. изотонические растворы 0.15 М (0.9%) раствор NaCl; 0.3 M (4.5–5.0%) р-р глюкозы изотонические растворы πNaCl =
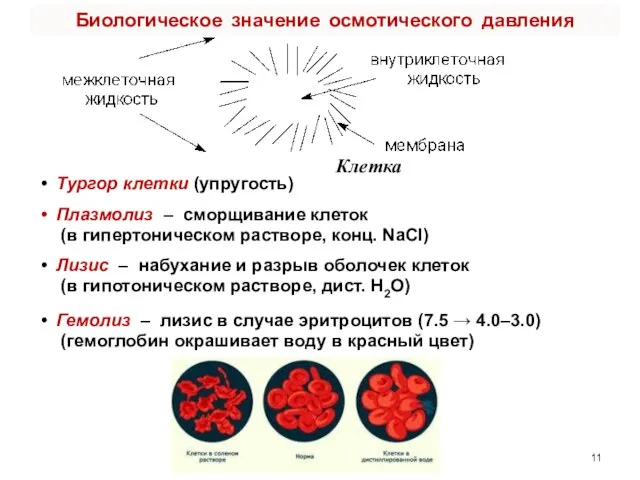
- 11. Клетка Тургор клетки (упругость) Плазмолиз – сморщивание клеток (в гипертоническом растворе, конц. NaCl) Лизис – набухание
- 12. — понижение температуры замерзания растворов по сравнению с чистым растворителем (температура замерзания плазмы крови – 0,55
- 13. 3. Растворимость газов в жидкостях Закон Генри (применим, если отсутствует химическое взаимодействие между газом и растворителем)
- 14. (для раствора газа в растворе электролита) Растворимость газов в жидкостях в присутствии электролитов понижается. c (Х)
- 15. изменение растворимости газов в крови при изменении давления; кессонная болезнь; гипербарическая оксигенация; Биологическое значение законов Генри
- 16. Введение в химическую термодинамику Термодинамика – учение о взаимных переходах различных форм энергии Основные понятия химической
- 17. Изолированная система – система, которая не обменивается со своим окружением ни энергией (теплотой или работой), ни
- 18. Гомогенная система – однородна и не имеет внутри себя поверхностей раздела между частями, отличающимися по физико‑химическим
- 19. Термодинамические параметры (измеряемые величины) подразделяют на: Экстенсивные – прямо пропорциональные количеству вещества системы, т.е. складывающиеся при
- 20. Типы состояния системы: – стационарное (непрерывный обмен веществом и энергией с окружающей средой). Параметры системы не
- 21. Процесс – переход системы из одного состояния в другое, характеризующийся изменением хотя бы одного параметра. Самопроизвольный
- 22. Наиболее важные функции состояния: Внутренняя энергия (U) – общий запас энергии, обусловленный всеми видами движений и
- 23. Энтальпия (Н) – H = U + pV Абсолютное значение энтальпии также определить невозможно. Изменение энтальпии
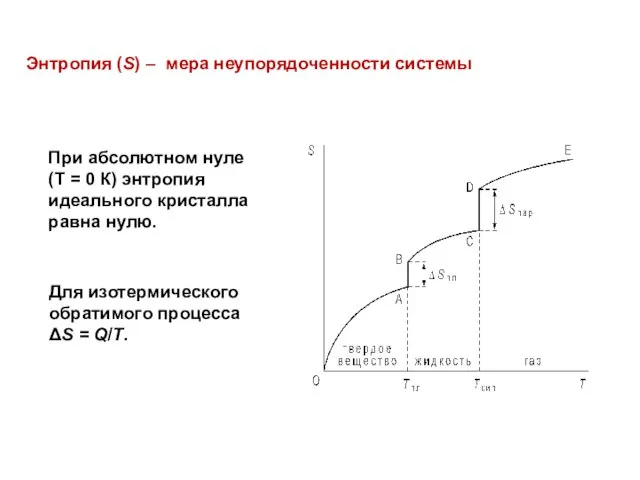
- 24. Энтропия (S) – мера неупорядоченности системы При абсолютном нуле (T = 0 К) энтропия идеального кристалла
- 25. Качественная оценка энтропии С(алмаз) твердое тело При объединении нескольких одинаковых систем их энтропии складываются При объединении
- 26. Энергия Гиббса (свободная энергия) (G) – G = H - TS позволяет судить о возможности самопроизвольного
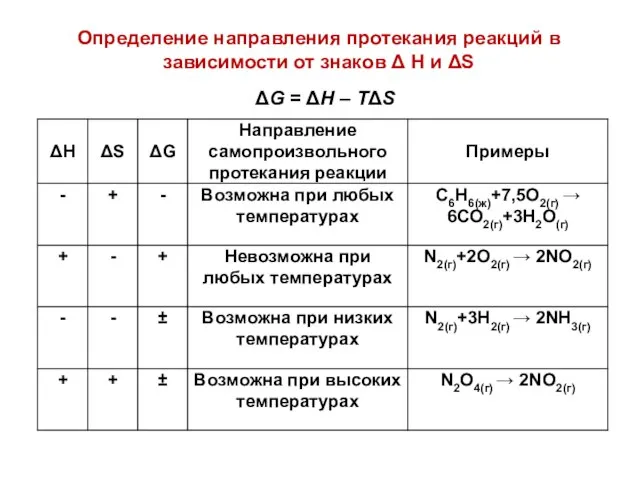
- 27. Определение направления протекания реакций в зависимости от знаков Δ H и ΔS ΔG = ΔH –
- 28. Термодинамические расчеты Стандартные условия: все вещества являются химически чистыми и соответствуют приводимой химической формуле; твердые и
- 29. Таблицы с термодинамическими данными Теплота образования вещества – тепловой эффект реакции образования 1 моль из простых
- 30. ЗАКОН ГЕССА — тепловой эффект реакции зависит только от природы и состояния исходных веществ и конечных
- 31. ΔреакцииH0T = – 2-e следствие: расчет теплового эффекта реакции по теплотам сгорания Ai — исходные вешества,
- 32. Термодинамическое сопряжение — протекание эндэргонической реакции (ΔG > 0) за счет энергии другой (экзэргонической) реакции (ΔG
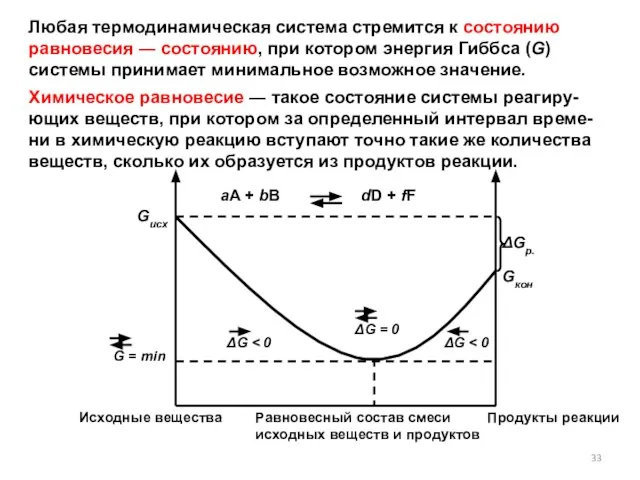
- 33. Любая термодинамическая система стремится к состоянию равновесия ― состоянию, при котором энергия Гиббса (G) системы принимает
- 34. Особенности равновесного состояния 1. Динамический характер: прямая и обратная реакции не прекращаются, а идут с равными
- 35. Константа химического равновесия ― количественная характеристика положения химического равновесия В общем виде для обратимой реакции aA
- 36. Значение константы данного химического равновесия опреде-ляется природой реагирующих веществ, зависит только от тем-пературы и не зависит
- 37. При движении химической системы к равновесию Пс → Кс Качественная оценка направления реакции при заданных концентрациях,
- 38. Уравнение изотермы химической реакции ΔGр-ции = – RT lnКс + RT lnПс или ΔGр-ции = RT
- 40. Скачать презентацию































 Методы трансформации карбоновых кислот и их производных
Методы трансформации карбоновых кислот и их производных Серная кислота
Серная кислота Галогены. История открытия галогенов
Галогены. История открытия галогенов Роль хімічних знань у пізнанні природи
Роль хімічних знань у пізнанні природи Классификация неорганических веществ
Классификация неорганических веществ Метаболизм липидов. Липолиз. Окисление жирных кислот и глицерола
Метаболизм липидов. Липолиз. Окисление жирных кислот и глицерола 8 класс. РЕШЕНИЕ ЗАДАЧ ПО УРАВНЕНИЯМ ХИМИЧЕСКИХ РЕАКЦИЙ
8 класс. РЕШЕНИЕ ЗАДАЧ ПО УРАВНЕНИЯМ ХИМИЧЕСКИХ РЕАКЦИЙ Водородная и донорно-акцепторная связи. (Лекция 15)
Водородная и донорно-акцепторная связи. (Лекция 15) «Гидролиз солей» Тема урока:
«Гидролиз солей» Тема урока: Титан. История открытия титана
Титан. История открытия титана Открытие водорода
Открытие водорода Хлор. Способы получения хлора
Хлор. Способы получения хлора Вязкость жидкости
Вязкость жидкости Объемная доля газа в смеси. (Урок 16. 7 класс)
Объемная доля газа в смеси. (Урок 16. 7 класс) Тосол. Гликолевые антифризы
Тосол. Гликолевые антифризы Нефть, как одна из основ жизни
Нефть, как одна из основ жизни Химия. Дисперсные системы. Растворы
Химия. Дисперсные системы. Растворы КОРОЗІЯ МЕТАЛІВ ЗАХИСТ ВІД КОРОЗІЇ Робота учениці 10-Б Єлісєєвої Марії
КОРОЗІЯ МЕТАЛІВ ЗАХИСТ ВІД КОРОЗІЇ Робота учениці 10-Б Єлісєєвої Марії  Щелочные металлы. Натрий. Выполнила: Ученица 9 Б класса МОУ СОШ №172 Мошкова Любовь. 2011 год.
Щелочные металлы. Натрий. Выполнила: Ученица 9 Б класса МОУ СОШ №172 Мошкова Любовь. 2011 год. Презентация по Химии "«Нитраты - минеральные удобрения»" - скачать смотреть
Презентация по Химии "«Нитраты - минеральные удобрения»" - скачать смотреть  Решение заданий ЕГЭ на составление окислительно-восстановительных реакций
Решение заданий ЕГЭ на составление окислительно-восстановительных реакций Азо-, диазосоединения
Азо-, диазосоединения Химическая кинетика
Химическая кинетика Нечаев 18
Нечаев 18 Графен. Силицен
Графен. Силицен Введение в химию органических соединений
Введение в химию органических соединений Автомобильные пластичные смазки
Автомобильные пластичные смазки Конструкционные материалы на основе легких металлов: сплавы алюминия
Конструкционные материалы на основе легких металлов: сплавы алюминия