Содержание
- 2. Засновником координаційної теорії комплексних сполук є швейцарський хімік Альфред Вернер (1866 - 1919); за роботи в
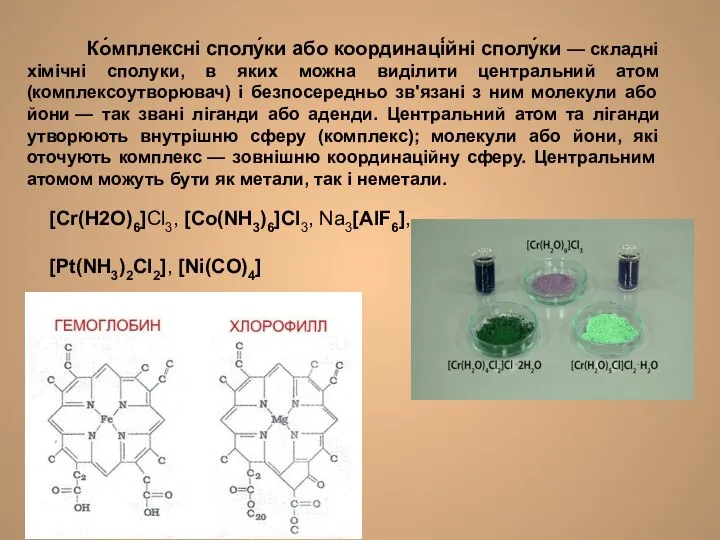
- 3. Ко́мплексні сполу́ки або координаці́йні сполу́ки — складні хімічні сполуки, в яких можна виділити центральний атом (комплексоутворювач)
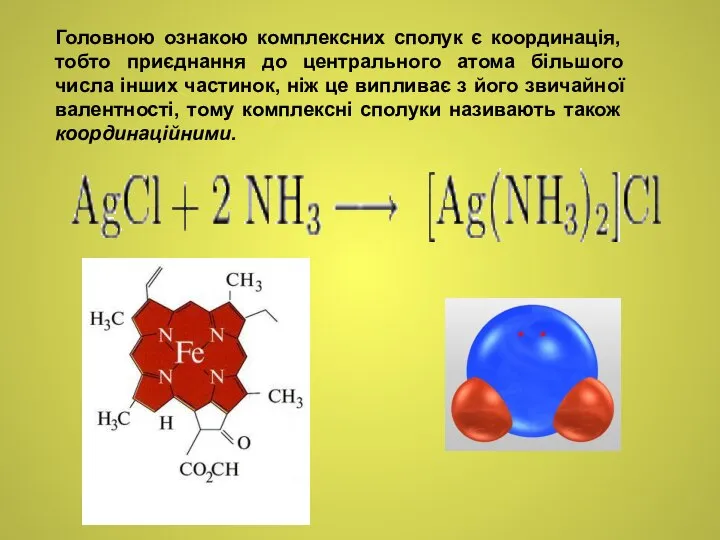
- 4. Головною ознакою комплексних сполук є координація, тобто приєднання до центрального атома більшого числа інших частинок, ніж
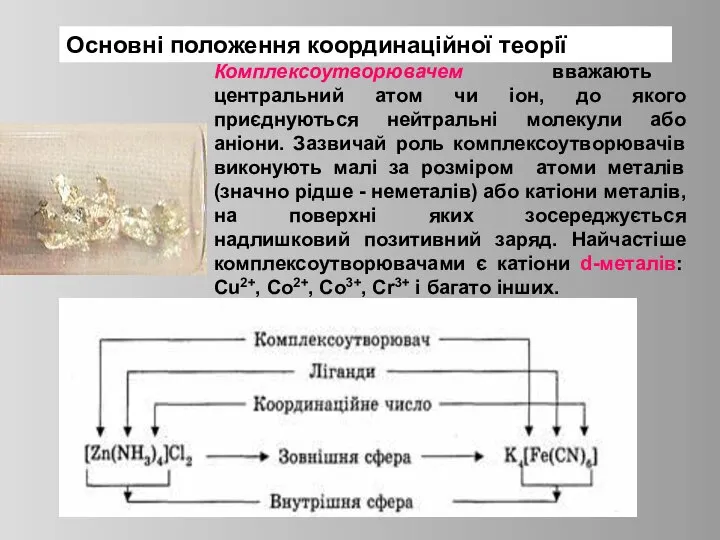
- 5. Основні положення координаційної теорії Комплексоутворювачем вважають центральний атом чи іон, до якого приєднуються нейтральні молекули або
- 6. Лігандами (приєднаними частинками) називають молекули або іони, які координуються навколо комплексоутворювача. Разом з останнім вони утворюють
- 7. Внутрішню координаційну сферу комплексної сполуки складають комплексоутворювач разом з лігандами, які приєдналися відповідно до координаційного числа
- 8. Координаційне число визначається числом місць у просторі, які може надавати комплексоутворювач для приєднання лігандів. Координаційне число
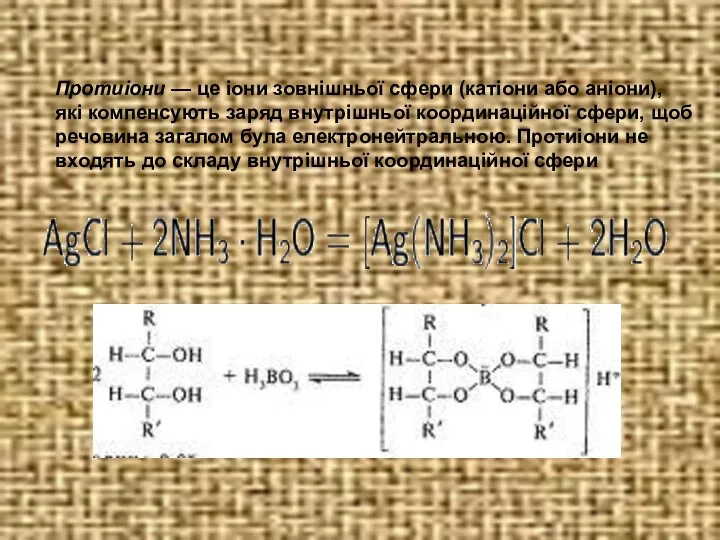
- 9. Протиіони — це іони зовнішньої сфери (катіони або аніони), які компенсують заряд внутрішньої координаційної сфери, щоб
- 10. Заряд внутрішньої координаційної сфери визначається сумою зарядів комплексоутворювача й усіх лігандів. Заряд внутрішньої координаційної сфери дорівнює
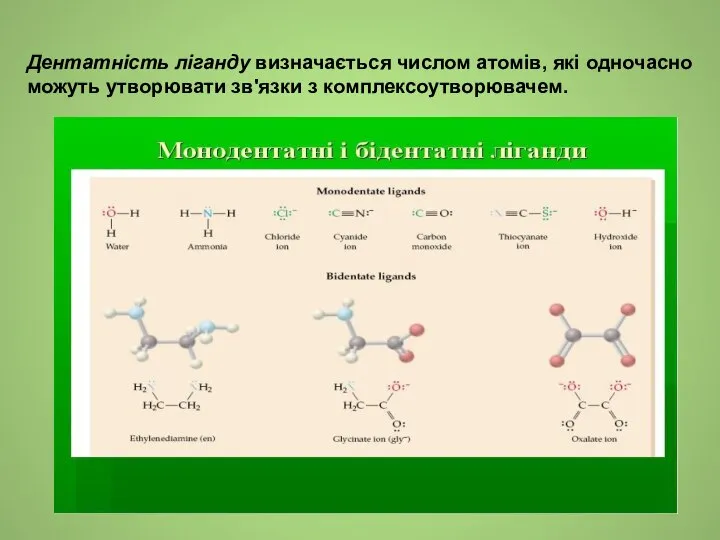
- 11. Дентатність ліганду визначається числом атомів, які одночасно можуть утворювати зв'язки з комплексоутворювачем.
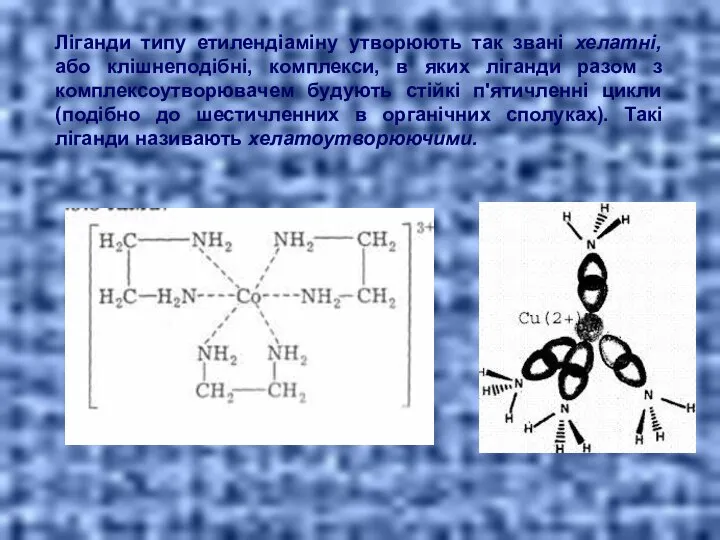
- 12. Ліганди типу етилендіаміну утворюють так звані хелатні, або клішнеподібні, комплекси, в яких ліганди разом з комплексоутворювачем
- 13. Розглянемо комплекс складу K4 [Fe (CN) 6] - гексаціаноферрат (II) калію (ферроціанід калію, жовта кров'яна сіль).
- 14. Класифікація комплексних сполук 1. За зарядом внутрішньої координаційної сфери: а) КС з комплексним катіоном (роль лігандів
- 15. 2. За природою лігандів: а) сполуки, що містять воду, амоніак, оксид карбону: аквакомплекси [Mg(H2O)6](ClO4)2; аміакати [Ag(NH3)2]
- 16. Просторова будова комплексних сполук Залежно від координаційного числа комплексні сполуки мають різну просторову будову. Якщо координаційне
- 17. Якщо координаційне число дорівнює 6, то внутрішня координаційна сфера має октаедричну або біпірамідальну просторову будову з
- 18. Ізомерія комплексних сполук Гідратна ізомерія полягає в різному розміщенні молекул води у внутрішній і зовнішній координаційних
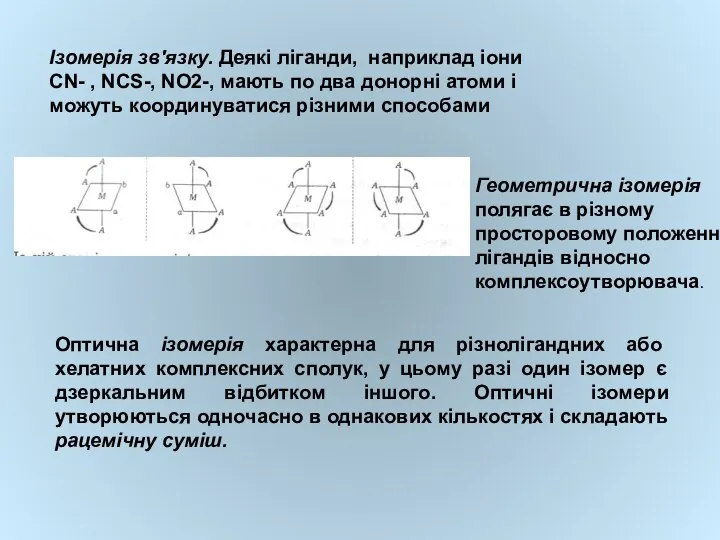
- 19. Ізомерія зв'язку. Деякі ліганди, наприклад іони СN- , NCS-, NO2-, мають по два донорні атоми і
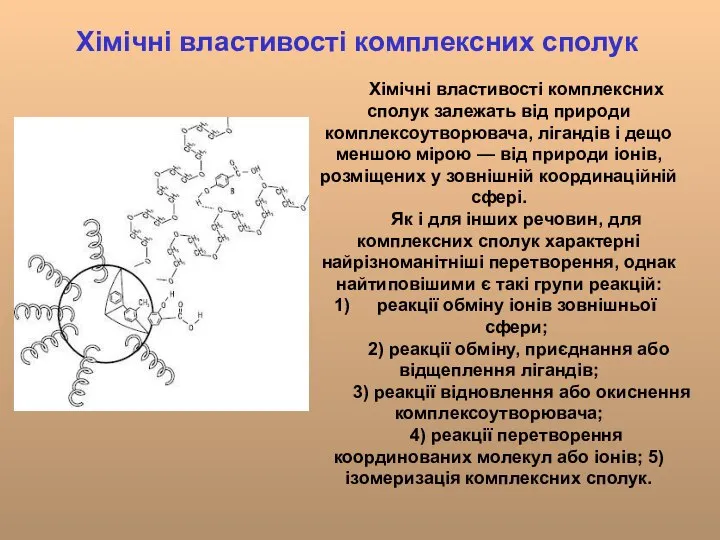
- 20. Хімічні властивості комплексних сполук Хімічні властивості комплексних сполук залежать від природи комплексоутворювача, лігандів і дещо меншою
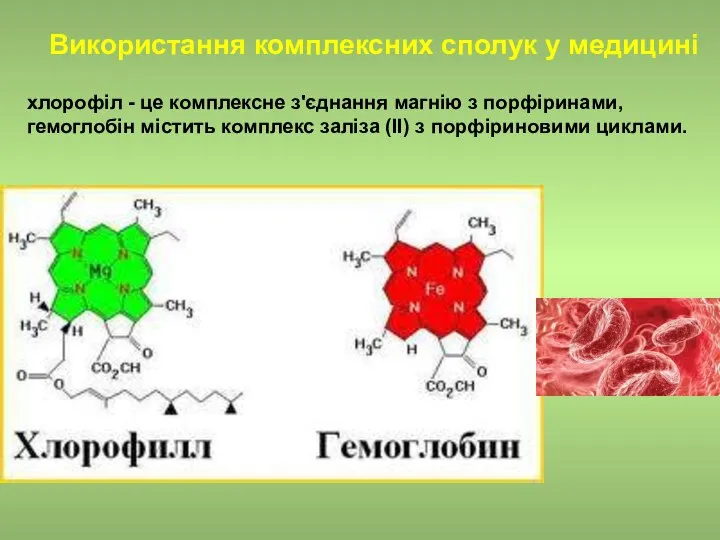
- 21. Використання комплексних сполук у медицині хлорофіл - це комплексне з'єднання магнію з порфіринами, гемоглобін містить комплекс
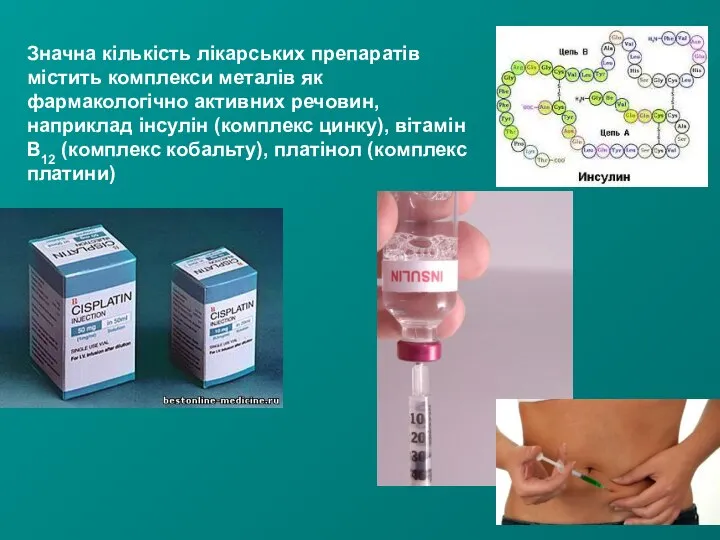
- 22. Значна кількість лікарських препаратів містить комплекси металів як фармакологічно активних речовин, наприклад інсулін (комплекс цинку), вітамін
- 25. КОМПЛЕКСОНОМЕТРІЯ (трилонометрія, хелатометрія) — титриметричний метод аналізу, що базується на реакціях утворення розчинних, дуже міцних комплексів
- 26. Стійкість комплексів катіонів металів з трилоном Б значною мірою залежить від рН-середовища. Більшість катіонів у кислому
- 27. Твердість води. Її види. Тве́рдість води́ — якщо вода містить значні кількості солей кальцію і магнію,
- 28. Загальна твердість води являє собою суму тимчасової і сталої твердості. Твердість води оцінюють у мг-екв/дм3. Воду
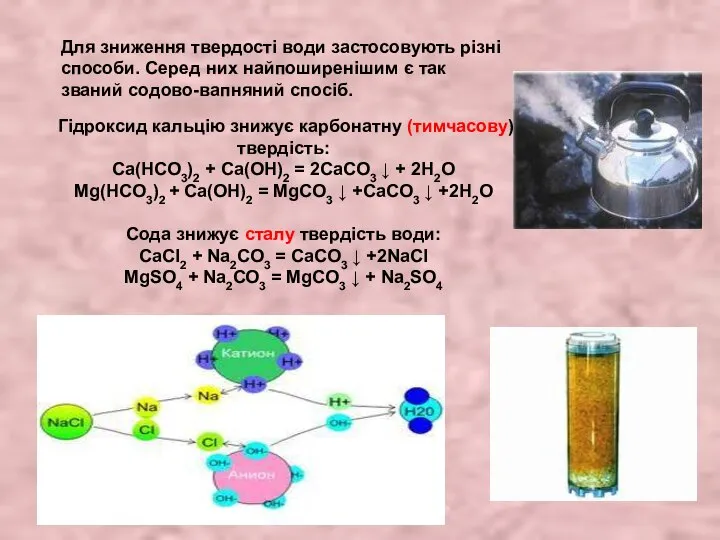
- 29. Для зниження твердості води застосовують різні способи. Серед них найпоширенішим є так званий содово-вапняний спосіб. Гідроксид
- 31. Скачать презентацию





![Розглянемо комплекс складу K4 [Fe (CN) 6] - гексаціаноферрат (II) калію](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397540/slide-12.jpg)










 Кристаллическая решетка
Кристаллическая решетка Муравьиная и уксусная кислоты
Муравьиная и уксусная кислоты Получение водорода в промышленности и его применение Химия 8 класс
Получение водорода в промышленности и его применение Химия 8 класс  Конструкционные полимеры: классификация, достижения и проблемы
Конструкционные полимеры: классификация, достижения и проблемы Оксид углерода-С
Оксид углерода-С Алкіни
Алкіни 20151216_udivitelnyy_mir_kamney_chast_1_0
20151216_udivitelnyy_mir_kamney_chast_1_0 Исследование структуры и электронного состояния оптически активных центров в алмазе, связанных с вхождением кремния и германия
Исследование структуры и электронного состояния оптически активных центров в алмазе, связанных с вхождением кремния и германия Значение органической химии Кондрашов Алексей | 9 А класс
Значение органической химии Кондрашов Алексей | 9 А класс  Химический элемент кислород
Химический элемент кислород Основы коррозии и защиты металлов
Основы коррозии и защиты металлов Природный и синтетический каучуки
Природный и синтетический каучуки Гидроксилпроизводные углеводородов
Гидроксилпроизводные углеводородов Презентация по Химии "Уран" - скачать смотреть
Презентация по Химии "Уран" - скачать смотреть  Массовая доля растворенного вещества
Массовая доля растворенного вещества Природные источники углеводородов
Природные источники углеводородов Презентация на тему «Биография Д.И. Менделеева» Работа Ученицы 9 – «А» класса СОШ № 1 Давыдовой Полины Под руководством Конд
Презентация на тему «Биография Д.И. Менделеева» Работа Ученицы 9 – «А» класса СОШ № 1 Давыдовой Полины Под руководством Конд Алканы. Пропан
Алканы. Пропан Математический аппарат квантовой механики
Математический аппарат квантовой механики Сорбционные процессы
Сорбционные процессы Бензол и его свойства
Бензол и его свойства Обмен веществ и энергии
Обмен веществ и энергии Розроблення моделі легування квантової точки InAs в матриці GaAs в хлоридній системі
Розроблення моделі легування квантової точки InAs в матриці GaAs в хлоридній системі Химическая связь. Типы кристаллических решеток
Химическая связь. Типы кристаллических решеток Алканы «Гексан»
Алканы «Гексан» Непредельные углеводороды: алкены
Непредельные углеводороды: алкены Моделирование деформаций углеродных слоёв при функционализации технического углерода
Моделирование деформаций углеродных слоёв при функционализации технического углерода Классификация химических реакций по типу взаимодействия
Классификация химических реакций по типу взаимодействия