Содержание
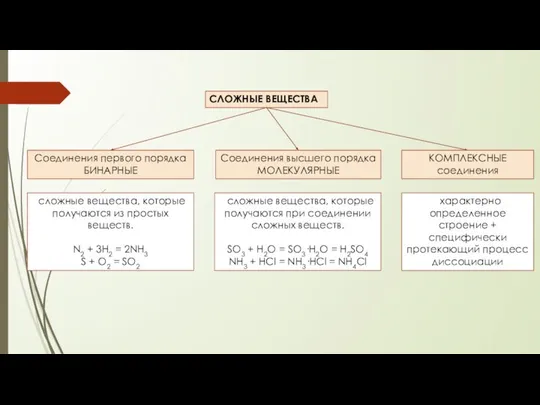
- 2. СЛОЖНЫЕ ВЕЩЕСТВА Соединения первого порядка БИНАРНЫЕ Соединения высшего порядка МОЛЕКУЛЯРНЫЕ сложные вещества, которые получаются из простых
- 3. Строение комплексных соединений
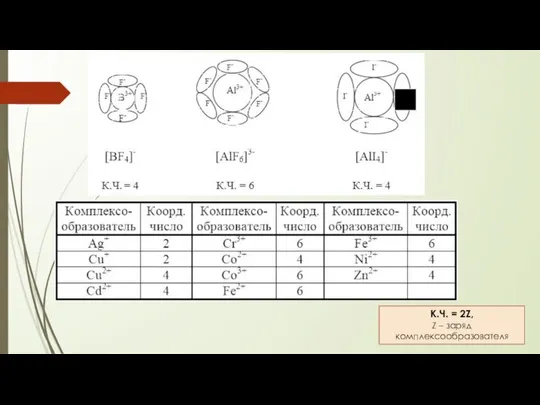
- 4. КОМПЛЕКСООБРАЗОВАТЕЛЬ положительно заряженные ионы d-элементов - чаще всего ионы р-элементов - иногда f-элементы - редко s-элементы
- 5. К.Ч. = 2Z, Z – заряд комплексообразователя
- 6. Классификация комплексных соединений Аквакомплексы Лигандами в этих соединениях являются молекулы воды (H2O) [Ti(H2O)6]Cl3 Аммиакатные комплексы Лигандами
- 7. Номенклатура комплексных соединений Сначала указывают название аниона, а затем катиона, то есть действует то же правило,
- 8. примеры [Cr(H2O)6]Cl3 – хлорид гексааква хрома (III); [Cu(NH3)4]SO4 – сульфат тетрааммин меди; K4[Zn(OH)4] – тетрагидроксоцинкат калия;
- 9. Признаки образования комплексных соединений ИЗМЕНЕНИЕ ЦВЕТА РАСТВОРА CuSO4 + 4NH3 = [Cu(NH3)4]SO4 бледно-голубой бесцветный ярко-синий РАСТВОРЕНИЕ
- 10. ДИССОЦИАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ Все растворимые комплексные соединения – сильные электролиты, полностью диссоциирующие в растворах на комплексный
- 12. Константа нестойкости Константа нестойкости (Кн): - характеризует прочность комплексного иона - по сути является константой диссоциации
- 14. Скачать презентацию




![примеры [Cr(H2O)6]Cl3 – хлорид гексааква хрома (III); [Cu(NH3)4]SO4 – сульфат тетрааммин](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396805/slide-7.jpg)




 Полиметилметакрилат
Полиметилметакрилат Алканы «Гексан»
Алканы «Гексан» Кислородсодержащие классы органических соединений. Гидроксисоединения. Карбонильные соединения. (Лекция 3)
Кислородсодержащие классы органических соединений. Гидроксисоединения. Карбонильные соединения. (Лекция 3) Презентация по Химии "Теория Витализма" - скачать смотреть бесплатно
Презентация по Химии "Теория Витализма" - скачать смотреть бесплатно Каталитический риформинг
Каталитический риформинг Кислоты в природе: состав, классификация, значение
Кислоты в природе: состав, классификация, значение Основные понятия и законы химии
Основные понятия и законы химии Применение спиртов
Применение спиртов Решение заданий С1 вариантов ЕГЭ учитель химии – Новикова Е.В. Окислительно-восстановительные реакции
Решение заданий С1 вариантов ЕГЭ учитель химии – Новикова Е.В. Окислительно-восстановительные реакции Полимеры. Классификация, применение
Полимеры. Классификация, применение Стекло — твердое неорганическое вещество
Стекло — твердое неорганическое вещество Строение атома. Опыты Резерфорда
Строение атома. Опыты Резерфорда Массовая доля элемента в веществе Задачи урока: 1. Познакомиться с понятием «массовая доля элемента в веществе» 2. Научиться рассч
Массовая доля элемента в веществе Задачи урока: 1. Познакомиться с понятием «массовая доля элемента в веществе» 2. Научиться рассч Полімери. Їх властивості та застосування
Полімери. Їх властивості та застосування Биоэнергетика. Современное представление о биологическом окислении
Биоэнергетика. Современное представление о биологическом окислении Выделение урана из растворов (пульп)
Выделение урана из растворов (пульп) Классификация полимеров по способу получения
Классификация полимеров по способу получения Нарушения окисления жирных кислот
Нарушения окисления жирных кислот Хімія запаху і смаку
Хімія запаху і смаку Свойства идеального газа на примере воздуха
Свойства идеального газа на примере воздуха Пантотен қышқылы (В3 дәрумені)
Пантотен қышқылы (В3 дәрумені) Геология и геохимия нефти и газа
Геология и геохимия нефти и газа Етери. Ізомерія та номенклатура
Етери. Ізомерія та номенклатура Особенности строения, реакционной способности и методы синтеза гидроксилсодержащих соединений
Особенности строения, реакционной способности и методы синтеза гидроксилсодержащих соединений Оксид кальция (СаО)
Оксид кальция (СаО) Radioimmunoassay& enzyme linked immunosorbent
Radioimmunoassay& enzyme linked immunosorbent Технология кварцевого стекла
Технология кварцевого стекла Чистые вещества и смеси
Чистые вещества и смеси