Содержание
- 2. в аналитической химии; при выделении химических элементов; в гальванотехнике; в борьбе с коррозией металлов; в производстве
- 3. Координационные (комплексные) соединения (КС) до 1893 г. строение КС не было известно название присваивались именами известных
- 4. По своему содержанию химические соединения делятся на простые (Н2, Cl2, O2 и т.д.) и сложные (H2O,
- 5. Координационные (комплексные) соединения (КС) Нобелевская премия по химии Швейцарский химик Альфред Вернер (1866-1919)
- 6. Координационные (комплексные) соединения координационная теория Вернера – основа для создания номенклатуры и прорыв в теории строения
- 7. [Co(NH3)6]3+ - комплекс [Co(NH3)6]Cl3 – комплексное соединение. [Fe(CO)5] – комплекс и комплексное соединение Комплекс - центральный
- 8. Лиганд – ион или нейтральная молекула, которые связаны с центральным атомом. Донорный атом – атом в
- 9. Донорно-акцепторный механизм: лиганд предоставляет электронную пару (основание Льюиса), а центральный атом вакантную орбиталь (кислота Льюиса). Координационные
- 10. ЛИГАНДЫ Амбидентатные лиганды – содержат несколько различных донорных атомов Роданид анион SCN-: если донорный атом S
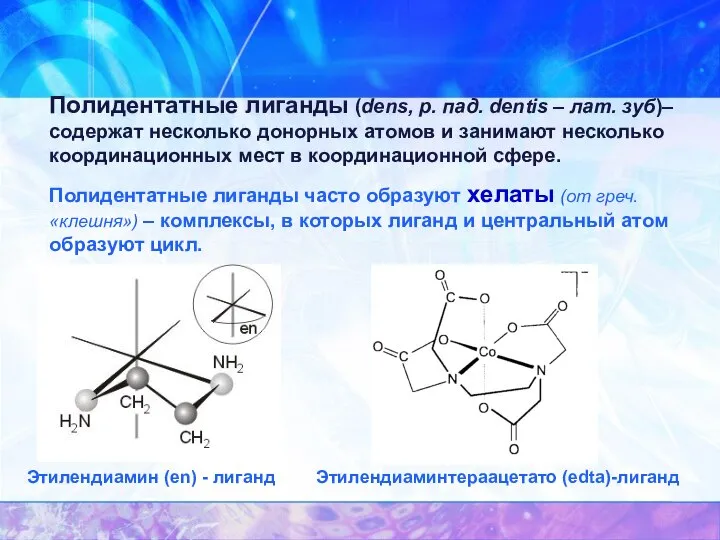
- 11. Полидентатные лиганды (dens, р. пад. dentis – лат. зуб)– содержат несколько донорных атомов и занимают несколько
- 12. Примеры лигандов Анионы бескислородных кислот F-, Cl-, Br-, I- (фторо-лиганд и т.д.) Пример: K2[HgI4] – тетраиодомеркурат(II)
- 13. Донорный атом O OH- - гидроксо-лиганд O2- - оксо-лиганд O22- - пероксо-лиганд K2[Zn(OH)4] – тетрагидроксоцинкат(II) калия
- 14. Электоронейтральные молекулы с донорными атомами N NH3 – аммин (лиганд) Пиридин (Py) Этилендиамин (en) [Pt(en)2]Cl2 –
- 15. КООРДИНАЦИОННЫЕ ЧИСЛА И КООРДИНАЦИОННЫЕ ПОЛИЭДРЫ Низкие КЧ = 2, 3 – встречаются редко КЧ = 2
- 16. НОМЕНКЛАТУРА (ИЮПАК) КС Построение формул: Сначала записывают катион, затем анион: X+ [MLn]− или [MLn]+ X− ,
- 17. НОМЕНКЛАТУРА (ИЮПАК) КС Построение формул: Если в состав внутренней сферы входят несколько одинаковых по заряду лигандов:
- 18. НОМЕНКЛАТУРА (ИЮПАК) КС Построение названий: Названия "читаются" слева направо по правильно составленной формуле: с н а
- 19. НОМЕНКЛАТУРА (ИЮПАК) КС Названия лигандов: Названия отрицательных лигандов: корень + -о- Br− – бромо; O2− –
- 20. НОМЕНКЛАТУРА (ИЮПАК) КС Названия отрицательных лигандов: корень + -о- OH− – гидроксо; NO− – нитрозо; CN−
- 21. НОМЕНКЛАТУРА (ИЮПАК) КС Названия отрицательных лигандов: корень + -о- CO32− – карбонато; NO3− – нитрато; NO2−
- 22. НОМЕНКЛАТУРА (ИЮПАК) КС Названия отрицательных лигандов: корень + -о- HCOO− – формиато; СН3СОО− – ацетато; СН3СН2СН2СОО−
- 23. НОМЕНКЛАТУРА (ИЮПАК) КС Названия отрицательных органических углеводородов: без соединительной гласной C6Н5− – фенил; C5Н5− – циклопентадиенил;
- 24. НОМЕНКЛАТУРА (ИЮПАК) КС Названия положительных лигандов: корень + -ий- NO+ – нитрозилий; NO2+ – нитроилий; N2Н5+
- 25. НОМЕНКЛАТУРА (ИЮПАК) КС Названия нейтральных лигандов: без изменений N2 – диазот; SO2 – диоксосера; СS2 –
- 26. Названия нейтральных лигандов: без изменений NН3 – аммин; CH3NH2 – метиламин; NH2CH2CH2NH2 – этилендиамин (en); С5Н5N
- 27. НОМЕНКЛАТУРА (ИЮПАК) КС [Co(en)3]Cl3 – хлорид трис(этилендиамин)кобальта(III) [(NH3)5 Cr O Cr(NH3)5]Cl4 – хлорид (μ-оксо)бис(пентаамминхрома(III))
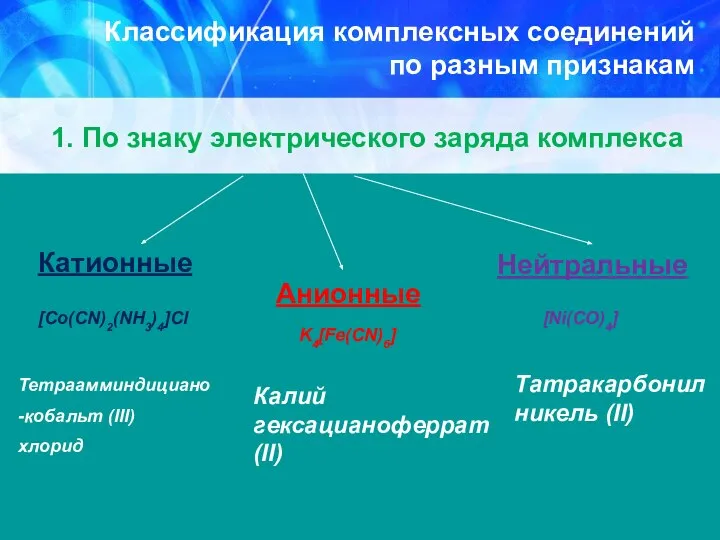
- 28. Классификация комплексных соединений по разным признакам 1. По знаку электрического заряда комплекса 2. Принадлежности к определённому
- 29. 2. По принадлежности к определённому классу соединений комплексные диамминсеребро(I) гидрооксид кислоты основания соли H[AuCl4] [Ag(NH3)2]OH K2[HgI4]
- 30. 3. По природе лигандов Аммиакаты [Ni(NH3)6]Cl2 Аквакомплексы [Co(H2O)6]SO4 Ацидокомплексы K[Cu(CN)2] Карбонилы [Fe(CO)5] Гидроксокомплексы K3[Al(OH)6 ] Цианидные
- 31. 4. По внутренней структуре комплексного соединения Моноядерные 4.2. По наличию циклов 4.1. По числу ядер Полиядерные
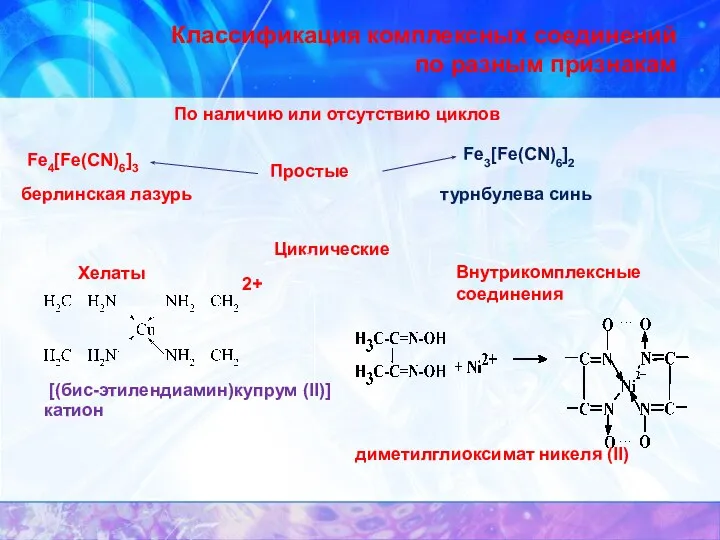
- 32. Классификация комплексных соединений по разным признакам По наличию или отсутствию циклов Простые Fe4[Fe(CN)6]3 берлинская лазурь Fe3[Fe(CN)6]2
- 33. Изомерия координационных соединений Координационная изомерия заключается в различном распределении лигандов во внутренних координационных сферах. По-разному взаимодействуют
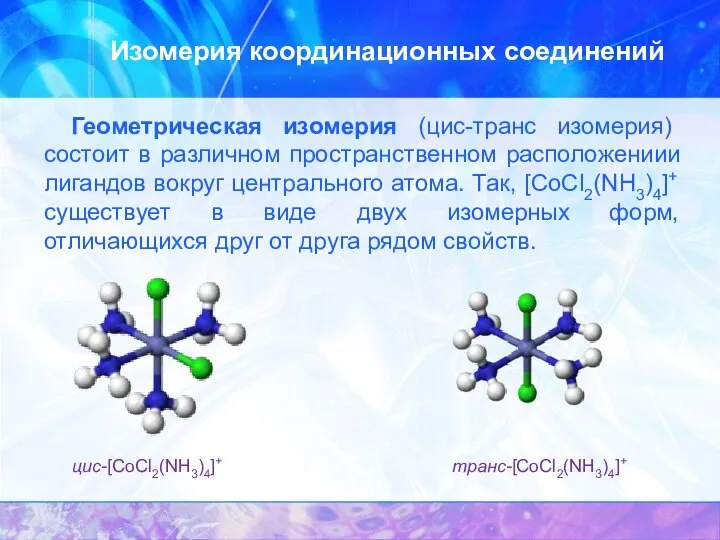
- 34. Изомерия координационных соединений Геометрическая изомерия (цис-транс изомерия) состоит в различном пространственном расположениии лигандов вокруг центрального атома.
- 35. Изомерия координационных соединений Оптическая изомерия. Оптическая изомерия характеризуется способностью вращать плоскость поляризации плоско-поляризованного света. Два изомера
- 36. Изомерия координационных соединений Структурная изомерия Гидратная (сольватная) изомерия заключается в различном распределении молекул растворителя между внутренней
- 37. 2. Реакции комплексных соединений. Устойчивость комплексных соединений и константа нестойкости
- 38. K3[Fe(CN)6] 3K+ + [Fe(CN)6]3- [Ag(NH3)2]Cl [Ag(NH3)2]+ + Cl- Диссоциация КС по внешней сфере (первичная диссоциация)
- 39. Реакции комплексных соединений по внешней сфере 2K3[Fe(CN)6] + 3FeSO4 = Fe3[Fe(CN)6]2↓ + 3K2SO4 [CoCl2(NH3)4]Cl + AgNO3
- 40. Константы комплексообразования Присоединение лиганда L к иону (атому) – комплексообразователю М с образованием координационного соединения ML
- 41. [Ag(NH3)2]+ [Ag(NH3)]+ + NH3 [Ag(NH3)2]+ Ag+ + 2 NH3 Диссоциация КС по внутренней сфере (вторичная диссоциация)
- 42. Реакции комплексных соединений с разрушением комплекса 1.Образование более прочного комплекса Fe3+ + 6 SCN- = [Fe(SCN)6]3-
- 43. 3. Разбавление K[AgCl2] = KCl + AgCl↓ 5. Окислительно-восстановительные реакции 2K3[Cr(ОH)6] + 3Сl2 + 4KOH =
- 44. хлорофилл
- 45. Гемоглобин
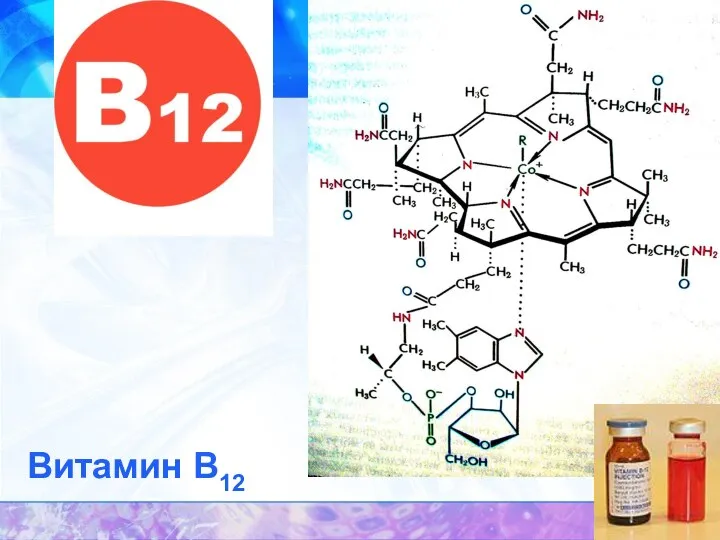
- 46. Витамин В12
- 47. ПРИМЕНЕНИЕ КОМПЛЕКСОВ В МЕДИЦИНЕ Вещества, устраняющие последствия воздействия ядов на биологические структуры и инактивирующие яды, посредством
- 48. -антидоты: (унитиол) ЭДТА, Na2ЭДТА, Na2CaЭДТА Меркаптидная связь
- 49. ПРИМЕНЕНИЕ КОМПЛЕКСОВ В МЕДИЦИНЕ Для выведения свинца используют препараты на основе ЭДТА. Введение в организм в
- 51. противоопухолевый препарат: цис-изомер дихлородиамминплатины (цис-платин) цис- [Pt(NH3)2Cl2]
- 52. создание новых катализаторов
- 54. Скачать презентацию





![[Co(NH3)6]3+ - комплекс [Co(NH3)6]Cl3 – комплексное соединение. [Fe(CO)5] – комплекс и](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1404223/slide-6.jpg)

















![НОМЕНКЛАТУРА (ИЮПАК) КС [Co(en)3]Cl3 – хлорид трис(этилендиамин)кобальта(III) [(NH3)5 Cr O Cr(NH3)5]Cl4 – хлорид (μ-оксо)бис(пентаамминхрома(III))](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1404223/slide-26.jpg)

![3. По природе лигандов Аммиакаты [Ni(NH3)6]Cl2 Аквакомплексы [Co(H2O)6]SO4 Ацидокомплексы K[Cu(CN)2] Карбонилы](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1404223/slide-29.jpg)





![K3[Fe(CN)6] 3K+ + [Fe(CN)6]3- [Ag(NH3)2]Cl [Ag(NH3)2]+ + Cl- Диссоциация КС по внешней сфере (первичная диссоциация)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1404223/slide-37.jpg)
![Реакции комплексных соединений по внешней сфере 2K3[Fe(CN)6] + 3FeSO4 = Fe3[Fe(CN)6]2↓](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1404223/slide-38.jpg)

![[Ag(NH3)2]+ [Ag(NH3)]+ + NH3 [Ag(NH3)2]+ Ag+ + 2 NH3 Диссоциация КС по внутренней сфере (вторичная диссоциация)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1404223/slide-40.jpg)

![3. Разбавление K[AgCl2] = KCl + AgCl↓ 5. Окислительно-восстановительные реакции 2K3[Cr(ОH)6]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1404223/slide-42.jpg)






![противоопухолевый препарат: цис-изомер дихлородиамминплатины (цис-платин) цис- [Pt(NH3)2Cl2]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1404223/slide-50.jpg)

 Обзор основных методов исследования супрамолекулярных объектов
Обзор основных методов исследования супрамолекулярных объектов Презентация по Химии "Многоатомные спирты" - скачать смотреть
Презентация по Химии "Многоатомные спирты" - скачать смотреть  Родючість ґрунтів , можливості її регулювання. Учень 9-Г класу Юрчак Владислав Керівник Садовська Т.Я.
Родючість ґрунтів , можливості її регулювання. Учень 9-Г класу Юрчак Владислав Керівник Садовська Т.Я. Симметрия в химии. Кристаллы
Симметрия в химии. Кристаллы Количественное определение лекарственных средств
Количественное определение лекарственных средств Электронные конфигурации атомов
Электронные конфигурации атомов Презентація З хімії На тему : ” Майбутнє альтернативного палива” Виконала учениця 11-А класу Твердохліб Анжеліка
Презентація З хімії На тему : ” Майбутнє альтернативного палива” Виконала учениця 11-А класу Твердохліб Анжеліка  Кислоты органические и неорганические.
Кислоты органические и неорганические. Синтетические моющие средства.(СМС) Подготовила Живулько Елена.
Синтетические моющие средства.(СМС) Подготовила Живулько Елена.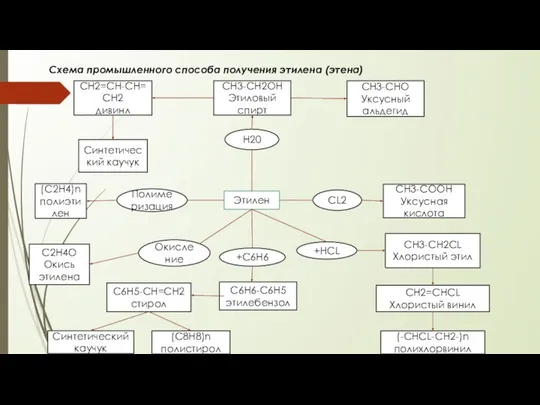 Промышленній способ получения этилена (этена)
Промышленній способ получения этилена (этена) Сложные эфиры
Сложные эфиры Растворы. Способы выражения концентрации растворенного вещества
Растворы. Способы выражения концентрации растворенного вещества Титани органічної хімії
Титани органічної хімії Энергетика химических процессов
Энергетика химических процессов Презентация по химии Химические уравнения Реакции обмена
Презентация по химии Химические уравнения Реакции обмена  Выращивание кристаллов в домашних условиях
Выращивание кристаллов в домашних условиях Неметаллы. Обобщение. Открытый урок
Неметаллы. Обобщение. Открытый урок Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Биогеохимия Оренбургской области
Биогеохимия Оренбургской области Химия элементов VIA группы. Сера
Химия элементов VIA группы. Сера Кремнийорганическая гипотеза
Кремнийорганическая гипотеза Неметаллы. Положение неметаллов в ПСХЭ
Неметаллы. Положение неметаллов в ПСХЭ Полифункциональды (гетерофункциональды) биоорганикалық қосылыстар: оксиқышқылдар, альдегидо- және кетоқышқылдар
Полифункциональды (гетерофункциональды) биоорганикалық қосылыстар: оксиқышқылдар, альдегидо- және кетоқышқылдар - Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового
- Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового  Задачи по теме Энергетический обмен
Задачи по теме Энергетический обмен Горение паро-газо-воздушного облака
Горение паро-газо-воздушного облака Ковалентная полярная связь
Ковалентная полярная связь Нітратна кислота. Нітрати Підготувала:Рибальчук Вікторія
Нітратна кислота. Нітрати Підготувала:Рибальчук Вікторія